Nung 1 tấn CaCO3 trong lò vôi, tính khối lượng CaO thu được biết hiệu suất của phản ứng đạt 90%.
(m.n giúp mik vs ạ . Mik cảm ơn)
nung đá vôi thu được 8,4 tấn vôi sống . Tính khối lượng đá vôi cần dùng biết trong đá vôi CaCO3 chiếm 85% về khối lượng và hiệu suất phản ứng đạt 90%
CaCO3 -----to---> CaO + CO2
mcaco3 = 100.8,4/56 = 15 tấn
khối lượng đá vôi thực tế cần là:
15:85% :90% = 19,61 tấn
CaCO3 ---> CaO+CO2
100 56
(8,4.100)/56 8,4
=> mCaCO3(lt) = 15 tấn
Do khối lượng đá vôi cần dùng cứa 85% là CaCO3
=> mCaCO3 = (15.85)/100= 12,75 tấn
do H% =90
=> mCaCO3 (Tt) = 12,75.90/100=11,475
Nhiệt phân CaCO3 ở 9000C thu được vôi sống và khí cacbon đioxit
a) Nung 300kg CaCO3 thu được 134,4g CaO.Tính hiệu suất phản ứng xảy ra.
b)Tính khối lượng CaO thu được khi nung 1 tấn CaCO3. Biết hiệu suất phản ứng chỉ đạt 90%.
c)Tính khối lượng CaCO3 đã dùng nếu sau phản ứng thu được 7,84 tấn CaO. Biết hiệu suất phản ứng đạt 70%
a) \(300kg=300000g\)
\(CaCO3-->CaO+CO2\)
\(n_{CaCO3}=\frac{300000}{100}=3000\left(mol\right)\)
\(n_{CaO}=n_{CaCO3}=3000\left(mol\right)\)
\(m_{CaO}=3000.56=168000\left(g\right)=168\left(kg\right)\)
Mk nghĩ đề là 134,4 kg ý
\(H\%=\frac{134,4}{168}.100\%=80\%\)
b) \(CaCO3-->CaO+CO2\)
\(1tấn=1000000g\)
\(n_{CaCO3}=\frac{1000000}{100}=10000\left(mol\right)\)
\(n_{CaO}=n_{CaCO3}=10000\left(mol\right)\)
\(m_{CaO}=10000.56=560000\left(g\right)=0,56\left(tấn\right)\)
Do H%=90%
\(\Rightarrow m_{CaO}=0,56.90\%=0,504\left(tấn\right)\)
c) \(7,84tấn=7840000\left(kg\right)\)
\(n_{CaO}=\frac{78400000}{56}=1400000\left(mol\right)\)
\(CaCO3-->CaO+CO2\)
\(n_{CaCO3}=n_{CaO}=1400000\left(mol\right)\)
\(m_{CaCO3}=1400000.100=140000000\left(g\right)=14tấn\)
a) CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
3 -> 3 -> 3 /mol
nCaCo3 = \(\frac{300}{100}=3\left(mol\right)\)
\(m_{CaOpt}\) = 3.56 = 168 (g)
H = \(\frac{134,4}{168}.100\%=80\%\)
b) Giả sử nung 1 tấn CaCo3 là nung 1g CaCo3
CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
0,01 -> 0,01 -> 0,01 /mol
nCaCo3 = \(\frac{1}{100}=0,01\left(mol\right)\)
mCaOpt = 0,01.56 = 0,56 (g)
mCaOtt = 0,56.90% = 0,504 (g)
Vậy thu được 0,504 tấn CaO khi nung 1 tấn CaCo3 với hiệu suất 90%
c) Giả sử 7,84 tấn CaO là 7,84 g CaO
CaCo3 \(\underrightarrow{t^o}\) CaO + Co2
0,098 <- 0,098 /mol
mCaOpt = 7,84.70% = 5,488 (g)
nCaO = \(\frac{5,488}{56}=0,098\left(mol\right)\)
mCaCo3 = 0,098.100 = 9,8 (g)
Vậy cần dùng 9,8 tấn CaCo3 để sau phản ứng thu đc 7,84 tấn CaO với hiệu suất 70%
\(CaCO_3\underrightarrow{^{to}}CaO+CO_2\)
a, (mình sửa thành 134,4kg)
Theo lí thuyết: 100kg CaCO3 tạo 56kg CaO
\(\Rightarrow\) 300kg CaCO3 tạo 168kg CaO
Thực tế chỉ có 134,4kg CaO
\(\Rightarrow H=\frac{134,4.100}{168}=80\%\)
b,
Nung 100 tấn CaCO3 tạo 56 tấn CaO
\(\Rightarrow\)1 tấn CaCO3 tạo 0,56 tấn CaO
H = 90% nên chỉ thu đc 0,56.90%= 0,504 tấn CaO
c,
Theo lí thuyết:
Nung 100 tấn CaCO3 tạo 56 tấn CaO
\(\Rightarrow\) 7,84 tấn CaO cần 14 tấn CaCO3
H =70% nên thực tế cần 14 : 70% = 20 tấn CaCO3
Một cơ sở sản xuất vôi tiến hành nung 4 tấn đá vôi (CaCO3 )thì thu được 1,68 tấn vôi sống (CaO) và một lượng khí CO2 . Tính hiệu suất của quá trình nung vôi ?
cố gắng giúp mik bằng cách M lý thuyết với M thực tế nha , mik cảm ơn nhìu :))))
PTHH: \(CaCO_3\rightarrow Cao+CO_2\)
\(1mol\rightarrow1mol\)
\(100g\rightarrow65g\)
Theo bài: 4 tấn \(\rightarrow\)m tấn
Khối lượng \(CaO\)được theo lý thuyết là:
\(m_{CaOlt}\)=\(\dfrac{4.56}{100}=2,24\)(tấn)
Hiệu suất phản ứng là:
\(H=\dfrac{1,68}{22,4.}100\%=75\%\)
Tính khối lượng vôi sống ( tấn) thu được khi nung 15 tấn đá vôi có hàm lượng 90% CaCO3. Hiệu suất phản ứng là 85%.
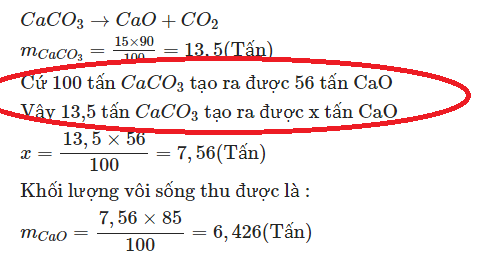
Các bạn chỉ mình chỗ mà khoanh màu đỏ : Cứ 100 tấn CaCO3 tạo ra 56 tấn CaO ( số 100 và số 56 lấy ở đâu ra vậy ạ)
15 tấn = 15 000(kg)
$m_{CaCO_3} = 15000.90\% = 13500(kg)$
$n_{CaCO_3} = \dfrac{13500}{100} = 135(kmol)$
$n_{CaCO_3\ pư} = 135.85\% = 114,75(kmol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
Theo PTHH : $n_{CaO} = n_{CaCO_3} = 114,75(kmol)$
$m_{CaO} = 114,75.56 = 6426(kg)$
Giải đáp thắc mắc :
100 là phân tử khối của $CaCO_3$
56 là phân tử khối của $CaO$
Cách làm như ảnh trên là áp số tỉ lệ về khối lượng theo PTHH
Nung đá vôi CaCO3 thu được vôi sống CaO và khí CO2. Biết hiệu suất chỉ đạt 70% hãy tính khối lượng CaO thu được khi nung 1 tấn đá vôi?
\(CaCO_3\xrightarrow[]{t^0}CaO+CO_2\)
Cứ 100 tấn đá vôi thì nung được 56 tấn vôi
\(\Rightarrow\dfrac{1}{100}=\dfrac{m_{CaO\left(lt\right)}}{56}\\ \Rightarrow m_{CaO\left(lt\right)}=0,56tấn\\ m_{CaO\left(tt\right)}=0,56.70\%=0,392tấn\)
Nung đá vôi thu được 5,6 tấn CaO và khí CO2. Tính khối lượng đá vôi cần dùng biết CaO3 chiếm 90% trên đá vôi và hiệu suất phản ứng là 80% Mong các anh chị giúp đỡ ạ
mCaO=5,6(tấn)= 5600000(g)
=>CaO= 5600000/56=100000(mol)
PTHH: CaCO3 -to-> CaO + CO2
nCaCO3(LT)=nCaO=100000(mol)
Vì H=80% => nCaO(TT)= 100000: 80%= 125000(mol)
=> mCaCO3=125 000 . 100 = 12 500 000(g)= 12,5(tấn)
=>m(đá vôi)=12,5 : 90%=13,889(tấn)
Chúc em học tốt!
để thu đc 11.2 tấn CaO thì cần nung bao nhiêu tấn đá vôi( chứa 90% CaCO3) biết hiệu suất phản ứng đạt 80%
\(n_{CaO} = \dfrac{11,2.1000}{56} = 200(kmol)\\ CaCO_3 \xrightarrow{t^o} CaO + CO_2\\ n_{CaCO_3\ pư} = n_{CaO} = 200(kmol)\\ n_{CaCO_3\ đã\ dùng} = \dfrac{200}{80\%} = 250(kmol)\\ m_{CaCO_3} = 250.100 = 25000(kg)\\ \Rightarrow m_{đá\ vôi} = \dfrac{25000}{90\%} = 27777,78(kg)\)
Nung 1 tấn đá vôi chứa 8% tạp chất. Tính khối lượng vôi sống thu được, nếu hiệu suất phản ứng là 95%? Giúp em vs ạ
\(m_{CaCO_3}=1000\cdot92\%=920\left(g\right)\\ \Rightarrow n_{CaCO_3}=\dfrac{920}{100}=9,2\left(mol\right)\\ PTHH:CaCO_3\rightarrow^{t^0}Cao+CO_2\\ \Rightarrow n_{CaO}=9,2\left(mol\right)\\ \Rightarrow m_{CaO}=9,2\cdot56=515,2\left(g\right)\\ \Rightarrow m_{CaO.thực.tế}=515,2\cdot95\%=489,44\left(g\right)\)
. Người ta điều chế vôi sống bằng cách nung đá vôi CaCO3 thu được vôi sống CaO và khí carbon dioxide CO2. Lượng vôi sống thu được khi nung 1 tấn đá vôi với hiệu suất phản ứng bằng 90% là
\(CaCO_3\xrightarrow[t^0]{}CaO+CO_2\\ \Rightarrow\dfrac{1}{100}=\dfrac{m_{CaO\left(LT\right)}}{56}\\ \Rightarrow m_{CaO\left(LT\right)}=0,56\left(tấn\right)\\ m_{CaO\left(TT\right)}=0,56.90\%=0,504\left(tấn\right)\)