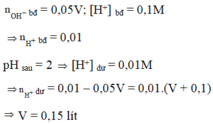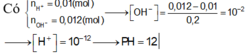tính thể tích dung dịch hcl 0,02M CẦN CHO VÀO 200ML dung dịch BA(0H)2 có pH=11 để thu đc dung dịch có pH=5

Những câu hỏi liên quan
Thể tích dung dịch Ba(OH)2 0,025M cần cho vào 100 ml dung dịch hỗn hợp gồm HNO3 và HCl có pH = 1, để thu được dung dịch có pH = 2 là:
A. 0,224 lít.
B. 0,15 lít.
C. 0,336 lít.
D. 0,448 lít.
Thể tích dung dịch HCl 0,3M cần cho vào l00ml dung dịch hỗn hợp NaOH 0,1M và Ba(OH)2 0,1M để thu được dung dịch có pH 7 là: A. 100 ml. B. 150 ml. C. 200ml. D. 250ml.
Đọc tiếp
Thể tích dung dịch HCl 0,3M cần cho vào l00ml dung dịch hỗn hợp NaOH 0,1M và Ba(OH)2 0,1M để thu được dung dịch có pH = 7 là:
A. 100 ml.
B. 150 ml.
C. 200ml.
D. 250ml.
Tính V lít dung dịch Ba(OH)2 0,025M cần cho vào 100ml dung dịch HNO3 và HCl có pH 1 để thu được dung dịch cuối cùng có pH 2. A. 0,15 B. 0,51 C. 0,2 D. Đ/a khác
Đọc tiếp
Tính V lít dung dịch Ba(OH)2 0,025M cần cho vào 100ml dung dịch HNO3 và HCl có pH = 1 để thu được dung dịch cuối cùng có pH = 2.
A. 0,15
B. 0,51
C. 0,2
D. Đ/a khác
Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là: A. 13 B. 2 C. 12 D. 7
Đọc tiếp
Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:Cho 100ml dung dịch HCl 0,1M vào 100ml dung dịch Ba(OH)2 0,06M thu được 200ml dung dịch X. Giá trị pH của dung dịch X là:
A. 13
B. 2
C. 12
D. 7
Cho m(g) Ba vào H2O thu được 200ml dung dịch X có pH=12.Cần thêm vào 100ml dung dịch X bao nhiêu ml dung dịch H2SO4 0,6M để thu được dung dịch sau phản ứng có pH=1
pH=12=>pOH=2 =>nOH- = 10-2*0,2=2*10-3 mol
OH- + H+ => H2O
0,002 0,002
sau pư, pH=1 => số mol H+ dư = 10-1*(0,2+0,1)=0,03mol
vậy tổng số mol H+ thêm vào= 0,03+0,002=0,032mol => nH2SO4=0,032/2=0,016mol
=>Vdd=0,016/0,6=0,0267l =26,7ml
Đúng 0
Bình luận (0)
Trộn 200 ml dung dịch HCl 0,025M với 300 ml dung dịch Ba(OH)2 0,01M, sau đó thêm vào 500 ml H2O thu được dung dịch A.
a) Tính pH của dung dịch A.
b) Tính cho 100 ml dung dịch FeSO4 0,02M vào dung dịch A. Tính khối lượng kết tủa thu được
a, \(n_{H^+}=0,025.0,2=0,005\left(mol\right)\)
\(n_{OH^-}=0,01.2.0,3=0,006\left(mol\right)\)
\(\Rightarrow n_{OH^-dư}=0,001\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]_{dư}=\dfrac{0,001}{1}=10^{-3}\)
\(\Rightarrow\left[H^+\right]=10^{-11}\)
\(\Rightarrow pH=11\)
Đúng 0
Bình luận (0)
b, \(n_{Fe^{2+}}=n_{SO_4^{2-}}=0,02.0,1=0,002\left(mol\right)\)
\(n_{Ba^{2+}}=0,01.0,3=0,003\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{BaSO_4\downarrow}=n_{SO_4^{2-}}=0,002\left(mol\right)\\n_{Fe\left(OH\right)_2\downarrow}=n_{OH^-dư}=0,001\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{\downarrow}=0,002.233+0,001.90=0,556\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 30 ( 1 điểm): Cho 200 ml dung dịch NaOH 1,0M tác dụng với 100 ml dung dịch H3PO4 1,0M thu được dung dịch X. Xác định muối tạo thành.Câu 31( 0,5 điểm) : Tính pH của dung dịch thu được khi trộn lẫn 200ml dung dịch HCl 0,02M với 200ml dung dịch KOH 0,04M. mọi người giúp mình 2 câu này nhanh với ạ !! T-T
Đọc tiếp
Câu 30 ( 1 điểm): Cho 200 ml dung dịch NaOH 1,0M tác dụng với 100 ml dung dịch H3PO4 1,0M thu được dung dịch X. Xác định muối tạo thành.
Câu 31( 0,5 điểm) : Tính pH của dung dịch thu được khi trộn lẫn 200ml dung dịch HCl 0,02M với 200ml dung dịch KOH 0,04M.
mọi người giúp mình 2 câu này nhanh với ạ !! T-T
Tính thể tích dung dịch HCl có pH = 5 và thể tích dung dịch KOH có pH = 9 cần lấy để pha thành 10 lít dung dịch có pH = 8?
Gọi V1, V2 lần lượt là thể tích của HCl và KOH
nH+ = 10-5.V1
nOH- = 10-5.V2
Sau pha trộn: nOH- dư = 10-6(V1 + V2)
=> 11V1 = 9V2
Mặc khác : V1 + V2=10
=> V1=4,5 ; V2=5,5
Đúng 2
Bình luận (1)
1) Lấy 20mL dung dịch HCL có pH=3 pha loãng thành 200mL dung dịch. Tính pH của dung dịch thu được 2) Lấy 30mL dung dịch HCL có pH=4 pha loãng thành 300mL dung dịch. Tính pH của dung dịch thu được
2) \(n_{HCl}=10^{-4}.0,03=0,000003\left(mol\right)\)
\(\Rightarrow C_{MddHCl}=\dfrac{0,000003}{0,03}=0,0001\left(M\right)\)
\(\Rightarrow\left[H^+\right]=C_{MddHCl}=0,0001M\)
\(pH=-log\left(0,0001\right)=4\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
1) \(n_{HCl\left(bđ\right)}=10^{-3}.0,02=0,00002\left(mol\right)\)
\(\Rightarrow C_{MddHCl}=\dfrac{0,00002}{0,02}=0,001\left(M\right)\)
\(\Rightarrow\left[H^+\right]=C_{MddHCl}=0,001M\)
\(pH=-log\left(0,001\right)=3\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)