Cho 100ml dung dịch \(Al_2\left(SO_4\right)_3\)0,5M và HCl 1M vào 450ml dung dịch \(Ba\left(OH\right)_2\) 0,5(M) tạo ra m(g) kết tủa và dung dịch X. Tính m và \(C_M\) của các ion trong dung dịch X.
Mấy cao nhân giúp e với ạ huhiuu :(
Cho 300ml dung dịch NaOH 2M vào 200ml dung dịch chứa \(Fe_2\left(SO_4\right)_3\) 0,5M và \(H_2SO_4\) 0,5M đến khi phản ứng hoàn toàn, thu được m gam kết tủa và dung dịch X. Tính m và nồng độ mol các ion trong X
\(\left\{{}\begin{matrix}n_{NaOH}=0,3.2=0,6\left(mol\right)\\n_{Fe_2\left(SO_4\right)_3}=0,2.0,5=0,1\left(mol\right)\\n_{H_2SO_4}=0,2.0,5=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left\{{}\begin{matrix}n_{Na^+}=0,6\left(mol\right)\\n_{Fe^{3+}}=0,1.2=0,2\left(mol\right)\\n_{H^+}=0,1.2=0,2\left(mol\right)\end{matrix}\right.\\\left\{{}\begin{matrix}n_{SO_4^{2-}}=0,1.3+0,1=0,4\left(mol\right)\\n_{OH^-}=0,6\left(mol\right)\end{matrix}\right.\end{matrix}\right.\)
PT ion rút gọn:
\(H^++OH^-\rightarrow H_2O\)
0,2-->0,2
\(Fe^{3+}+3OH^-\rightarrow Fe\left(OH\right)_3\downarrow\)
\(\dfrac{2}{15}\)<----0,4--------->\(\dfrac{2}{15}\)
\(\Rightarrow m=\dfrac{2}{15}.107=\dfrac{214}{15}\left(g\right)\)
dd sau phản ứng có: \(\left\{{}\begin{matrix}n_{Na^+}=0,6\left(mol\right)\\n_{Fe^{3+}\left(d\text{ư}\right)}=0,2-\dfrac{2}{15}=\dfrac{1}{15}\left(mol\right)\\n_{SO_4^{2-}}=0,4\left(mol\right)\end{matrix}\right.\)
\(V_{\text{dd}}=0,3+0,2=0,5\left(l\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C_{Na^+}=\dfrac{0,6}{0,5}=1,2M\\C_{Fe^{3+}}=\dfrac{\dfrac{1}{15}}{0,5}=\dfrac{2}{15}M\\C_{SO_4^{2-}}=\dfrac{0,4}{0,5}=0,8M\end{matrix}\right.\)
cho 13,8 g Na vào 240ml dung dịch có khối lượng riêng la 1,25g/ml chứa \(Fe_2\left(SO_4\right)_3\) 0,125M và \(Al_2\left(SO_4\right)_3\) 0,25M. sau phản ứng hoàn toàn thu được dung dịch A và kết tủa B. . Đem nung B đến khối lượng không đổi thu được m(g) chất rắn C
a, tính m
b. tính C% của các muối trong A
Dung dịch X chưa 0,12mol \(Na^+\), x mol \(SO_4^{2-}\), 0,12 mol Cl- và 0,05 mol \(NH_4^+\). Cho 300ml dung dịch \(Ba\left(OH\right)_2\) 0,1M vào X đến khi các phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y, thu được m gam chất rắn khan. Giá trị của m là
Bảo toàn điện tích : $x = \dfrac{0,12 + 0,05 - 0,12}{2} = 0,025(mol)$
$n_{Ba^{2+}} = n_{Ba(OH)_2} = 0,3.0,1 = 0,03(mol)$
$n_{OH^-} = 2n_{Ba(OH)_2} = 0,06(mol)$
$Ba^{2+} + SO_4^{2-} \to BaSO_4$
$NH_4^+ + OH^- \to NH_3 + H_2O$
Suy ra, dung dịch gồm :
$Na^+ : 0,12(mol)$
$Cl^- : 0,12(mol)$
$OH^- : 0,06 - 0,05 = 0,01(mol)$
$Ba^{2+} : 0,03 - 0,025 = 0,005(mol)$
Suy ra: $m = 0,12.23 + 0,12.35,5 + 0,01.17 + 0,005.137 = 7,875(gam)$
Cho từ từ 100 ml dung dịch chứa hỗn hợp NaHCO3 2M, Na2CO3 1M vào 100 ml dung dịch chứa HCl 1M và H2SO4 0,5M thu được V lít khí (đktc) và dung dịch X. Cho 100ml dung dịch Ba(OH)2 2M và NaOH 0,75M vào dung dịch X thu được m (g) kết tủa. Giá trị của m, V là:
A. 45 gam và 2,24 lít
B. 43 gam và 2,24 lít
C. 41,2 gam và 3,36 lít
D. 43 gam và 3,36 lít
Đáp án C
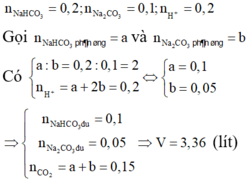
n Ba ( OH ) 2 = 0 , 2 ; n NaOH = 0 , 075
![]()
Cho 600 ml dung dịch \(NH_3\) 5M vào 200 ml dung dịch A gồm \(H_2SO_4\)1M, \(MgSO_4\)0,5M và \(Al_2\left(SO_4\right)_3\)0,5M, sau khi phản ứng hoàn toàn thu được m gam kết tủa và 800 ml dung dịch B. Tính giá trị m và nồng độ mol của chất tan trong dung dịch B.
Trộn 100ml dung dịch \(Fe_2\left(SO_4\right)_3\) 1,5M với 150ml dung dịch \(Ba\left(OH\right)_2\) 2M.
a, Tính khối lượng kết tủa thu được sau phản ứng.
b, Tính nồng độ mol của các chất có trong dung dịch sau phản ứng
PTHH: \(Fe_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow3BaSO_4\downarrow+2Fe\left(OH\right)_3\downarrow\)a. Số mol các chất tham gia: \(n_{Fe_2\left(SO_4\right)_3}=0,1.1,5=0,15\left(mol\right)\) \(n_{Ba\left(OH\right)_2}=0,15.2=0,3\left(mol\right)\) Lập tỉ lệ: \(\dfrac{0,15}{1}>\dfrac{0,3}{3}\) => \(Fe_2\left(SO_4\right)_3\) dư, tính toán theo \(Ba\left(OH\right)_2\). Theo PTHH, ta có: \(n_{BaSO_4}=n_{Ba\left(OH\right)_2}=0,3\left(mol\right)\) \(n_{Fe\left(OH\right)_3}=\dfrac{2}{3}n_{Ba\left(OH\right)_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\) Khối lượng kết tủa thu được sau pứ: \(m_{BaSO_4+Fe\left(OH\right)_3}=0,3.233+0,2.107=91,3\left(g\right)\)
b. Theo PTHH: \(n_{Fe_2\left(SO_4\right)_3\left(pứ\right)}=\dfrac{1}{3}n_{Ba\left(OH\right)_2}=\dfrac{1}{3}.0,3=0,1\left(mol\right)\)=> \(n_{Fe_2\left(SO_4\right)_3\left(dư\right)}=0,15-0,1=0,05\left(mol\right)\) Nồng độ mol các chất trong phản ứng: \(C_{M\left(BaSO_4\right)}=\dfrac{0,3}{0,25}=1,2M\) \(C_{M\left(Fe\left(OH\right)_3\right)}=\dfrac{0,2}{0,25}=0,8M\) \(C_{M\left(Fe_2\left(SO_4\right)_3\right)}=\dfrac{0,05}{0,25}=0,2M\)
Dung dịch X chứa 0,15 mol H2SO4 và 0,1 mol Al2(SO4)3. Cho V ml dung dịch NaOH 1M vào dung dịch X, thu được m gam kết tủa. Thêm tiếp 450ml dung dịch NaOH 1M vào, sau khi các phản ứng xảy ra hoàn toàn thu được 0,5m gam kết tủa. Tính giá trị của m .(không giải pt ion ạ giải bthuong giúp e ạ)
Dung dịch X chứa 0,15 mol H2SO4 và 0,1 mol Al2(SO4)3. Cho V ml dung dịch NaOH 1M vào dung dịch X, thu được m gam kết tủa. Thêm tiếp 450ml dung dịch NaOH 1M vào, sau khi các phản ứng xảy ra hoàn toàn thu được 0,5m gam kết tủa. Giá trị của m là:
A. 4,68 gam
B. 11,70 gam
C. 3,90 gam
D. 7,80 gam
Dung dịch X chứa 0,15 mol H2SO4 và 0,1 mol Al2(SO4)3. Cho V ml dung dịch NaOH 1M vào dung dịch X, thu được m gam kết tủa. Thêm tiếp 450ml dung dịch NaOH 1M vào, sau khi các phản ứng xảy ra hoàn toàn thu được 0,5m gam kết tủa. Giá trị của m là:
A. 4,68 gam
B. 11,70 gam
C. 3,90 gam
D. 7,80 gam