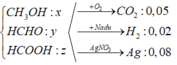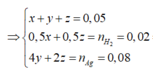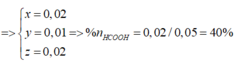Đốt cháy hoàn toàn 1 hợp chất hữu cơ X phải dùng 6,04 lít khí oxi (đktc) thu được 0,15 mol khí CO2 và 3,6g H2O.Xác định % khối lượng các nguyên tố trong phân tử chất X

Những câu hỏi liên quan
Đốt cháy hoàn toàn 2.25 gam một chất hữu cơ X thu được 3.36 lít khí co2(đo ở đktc) và 4.05 gam h2o
a)Chất X có những nguyên tố nào?
b)xác định công thức phân tử và viết công thức cấu tạo của X.Biết khối lượng mol của X nhỏ hơn 40gam/mol
a) Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{4,05}{18}=0,45\left(mol\right)\)
Xét mC + mH = 0,15.12 + 0,45 = 2,25 (g)
=> X gồm C và H
b, CTPT của X có dạng CxHy
=> x : y = 0,15 : 0,45 = 1 : 3
=> (CH3)n < 40
=> n = 2
CTPT: C2H6
Đúng 4
Bình luận (0)
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{4,05}{18}=0,45mol\)
\(n_O=\dfrac{2,25-\left(0,15.12+0,45.1\right)}{16}=0mol\)
=> X chỉ có C và H
\(CTHH:C_xH_y\)
\(\rightarrow x:y=0,15:0,45=1:3\)
\(\rightarrow CTPT:CH_3\)
\(CTĐG:\left(CH_3\right)n< 40\)
\(\rightarrow n=1;2\)
\(n=1\rightarrow CTPT:CH_3\left(loại\right)\)
\(n=2\rightarrow CTPT:C_2H_6\left(nhận\right)\)
\(CTCT:CH_3-CH_3\)
Đúng 4
Bình luận (0)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
=> X gồm có nguyên tố C , H.
\(nCO_2=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
=> nC = 0,15(mol)
mC = 0,15 .12 = 1,8(g)
\(nH_2O=\dfrac{4,05}{18}=0,225\left(mol\right)\)
=> nH = 0,225 . 2 = 0,45(mol)
mH = 0,45 . 1 = 0,45 (g)
Vì mH + mC = 1,8 + 0,45 = 2,25 (g) = mX
=> X không có nguyên tố O.
Gọi CTHH đơn giản của X là CxHy
ta có : x : y = 0,15 : 0,45 = 1 : 3
=> CTHH đơn giản của X là CH3
ta có:
(CH3)n < 40
=> n = 2
=> CTPT của X là C2H6
CTCT của X là CH3 - CH3
Đúng 3
Bình luận (0)
Hỗn hợp X gồm ba chất hữu cơ mạch hở , trong phân tử chỉ chứa các loại nhóm chức -OH, -CHO, -COOH. Chia 0,15 mol X thành ba phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được 1,12 lít khí CO2 (đktc). Phần hai tác dụng với Na dư, thu được 0,448 lít H2 (đktc). Đun nóng phần ba với lượng dung dịch AgNO3 trong NH3 , thu được 8,64g Ag. Phần trăm số mol của chất có phân tử khối lớn nhất trong X là : A. 50% B. 30% C. 20% D. 40%
Đọc tiếp
Hỗn hợp X gồm ba chất hữu cơ mạch hở , trong phân tử chỉ chứa các loại nhóm chức -OH, -CHO, -COOH. Chia 0,15 mol X thành ba phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được 1,12 lít khí CO2 (đktc). Phần hai tác dụng với Na dư, thu được 0,448 lít H2 (đktc). Đun nóng phần ba với lượng dung dịch AgNO3 trong NH3 , thu được 8,64g Ag. Phần trăm số mol của chất có phân tử khối lớn nhất trong X là :
A. 50%
B. 30%
C. 20%
D. 40%
Đáp án : D
+) P1 : nCO2 = nX => Các chất trong X có 1 C trong phân tử
=> Các chất đó là HCHO ; CH3OH ; HCOOH với số mol lần lượt là x;y;z
=> x + y + z = 0,05
+) P2 : 2nH2 = y + z = 0,04
+) P3 : nAg = 4x + 2z = 0,08
=> x = 0,01 ; y = 0,02 ; z = 0,02 mol
=> %nHCOOH = 40%
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 5,8g một hợp chất hữu cơ X bằng khí \(O_2\), thu được 6,72 lít khí \(CO_2\) (ở đktc), và 5,4g \(H_2O\). Xác định công thức phân tử và thành phần phần trăm khối lượng của các nguyên tố trong X?
Giúp mk vs ạ mình đang cần gấp thanks trước
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ n_{H_2O}=\dfrac{5,4}{18}=0,3(mol)\)
Bảo toàn C và H: \(n_C=0,3(mol);n_H=0,6(mol)\)
\(\Rightarrow m_C=0,3.12=3,6(g);m_H=0,6.1=0,6(g)\\ \Rightarrow m_X>m_C+m_H\)
Do đó X bao gồm \(O\)
\(\Rightarrow m_O=5,8-3,6-0,6=1,6(g)\\ \Rightarrow n_O=\dfrac{1,6}{16}=0,1(mol)\)
Gọi CT của X là \(C_xH_yO_z\)
\(\Rightarrow x:y:z=0,3:0,6:0,1=3:6:1\\ \Rightarrow CTPT_X:C_3H_6O\)
\(\%_C=\dfrac{36}{58}.100\%=62,07\%\\ \%_H=\dfrac{6}{58}.100\%=10,34\%\\ \%_O=100\%-62,07\%-10,34\%=27,59\%\)
Đúng 1
Bình luận (2)
Làm tiếp của Nguyễn Hoàng Minh
Gọi CTHH của X là: \(C_xH_yO_z\)
Ta có: \(m_{C_X}=m_{C_{CO_2}}=0,3.12=3,6\left(g\right)\)
\(m_{H_X}=m_{H_{H_2O}}=0,3.2=0,6\left(g\right)\)
\(m_{O_X}=m_{O_{CO_2}}+m_{O_{H_2O}}-m_{O_2}=9,6+4,8-12,8=1,6\left(g\right)\)
\(\Rightarrow\%_O=\dfrac{1,6}{5,8}.100\%=27,6\%\)
\(\%_H=\dfrac{0,6}{5,8}.100\%=10,3\%\)
\(\%_C=100\%-27,6\%-10,3\%=62,1\%\)
Đúng 1
Bình luận (1)
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của XCâu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của XCâu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC 40% ; %mH 6,67% còn lại là oxi.Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Đọc tiếp
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và
10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của X
Câu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.
Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của X
Câu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC = 40% ; %mH = 6,67% còn lại là oxi.
Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Câu 7:
\(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Bảo toàn C: nC = 0,6 (mol)
Bảo toàn H: nH = 1,2 (mol)
=> \(n_O=\dfrac{10,8-0,6.12-1,2}{16}=0,15\left(mol\right)\)
=> nC : nH : nO = 0,6 : 1,2 : 0,15 = 4:8:1
=> CTPT: (C4H8O)n
Mà M = 2,25.32 = 72(g/mol)
=> n = 1
=> CTPT: C4H8O
Câu 6
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn C: nC = 0,25 (mol)
Bảo toàn H: nH = 0,6 (mol)
=> \(n_O=\dfrac{4,4-0,25.12-0,6.1}{16}=0,05\left(mol\right)\)
nC : nH : nO = 0,25 : 0,6 : 0,05 = 5:12:1
=> CTPT: (C5H12O)n
Mà M = 44.2=88(g/mol)
=> n = 1
=> CTPT: C5H12O
Câu 8:
MX = 1,875.32 = 60 (g/mol)
Giả sử có 1 mol chất X => mX = 60.1 = 60 (g)
\(m_C=\dfrac{60.40}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{60.6,67}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
\(m_O=60-24-4=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> Trong 1 mol X chứa 2 mol C, 4 mol H, 2 mol O
=> CTPT: C2H4O2
Đúng 2
Bình luận (0)
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của XCâu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của XCâu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC 40% ; %mH 6,67% còn lại là oxi.Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Đọc tiếp
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và
10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của X
Câu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.
Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của X
Câu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC = 40% ; %mH = 6,67% còn lại là oxi.
Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Hỗn hợp X gồm ba chất hữu cơ mạch hở, trong phân tử chỉ chứa các loại nhóm chức – OH, - CHO, - COOH. Chia 0,15 mol X thành ba phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được 1,12 lít khí CO2 (đktc). Phần hai tác dụng với Na dư, thu được 0,448 lít H2 (đktc). Đun nóng phần ba với lượng dư dung dịch AgNO3 trong NH3, thu được 8,64 gam Ag. Phần trăm số mol của chất có phân tử khối lớn nhất trong X là: A. 30%. B. 50%. C. 40%. D. 20%.
Đọc tiếp
Hỗn hợp X gồm ba chất hữu cơ mạch hở, trong phân tử chỉ chứa các loại nhóm chức – OH, - CHO, - COOH. Chia 0,15 mol X thành ba phần bằng nhau. Đốt cháy hoàn toàn phần một, thu được 1,12 lít khí CO2 (đktc). Phần hai tác dụng với Na dư, thu được 0,448 lít H2 (đktc). Đun nóng phần ba với lượng dư dung dịch AgNO3 trong NH3, thu được 8,64 gam Ag. Phần trăm số mol của chất có phân tử khối lớn nhất trong X là:
A. 30%.
B. 50%.
C. 40%.
D. 20%.
đốt cháy hoàn toàn 0,3 gam hợp chất hữu cơ A, (phân tử chứa C, H, O) thu được 0,44 gam CO2, 0,18 gam H2O và 224ml khí N2 (đktc). tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất hữu cơ A
Đốt cháy hoàn toàn 8,2 gam hợp chất hữu cơ X, thu được 3,36 lít
CO
2
(đktc), 5,3 gam
Na
2
CO
3
và 2,7 gam
H
2
O
. Khối lượng nguyên tố oxi trong 8,2 gam X là A. 6,1 gam B. 3,8 gam C. 5,5 gam D. 3,2 gam
Đọc tiếp
Đốt cháy hoàn toàn 8,2 gam hợp chất hữu cơ X, thu được 3,36 lít CO 2 (đktc), 5,3 gam Na 2 CO 3 và 2,7 gam H 2 O . Khối lượng nguyên tố oxi trong 8,2 gam X là
A. 6,1 gam
B. 3,8 gam
C. 5,5 gam
D. 3,2 gam
Đáp án D
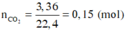
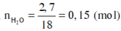
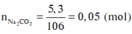
mX = mC + mH + mO + mNa = 12 ( n N a 2 C O 3 + n C O 2 ) + 2 n H 2 O + 23.2. n N a 2 C O 3 + m O
Þ 12.(0,15 + 0,05) + 2.0,15 + 46.0,05 + mO = 8,2
Þ mO = 3,2 gam
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn 9 gam chất hữu cơ X cần dùng 1 lượng oxi vừa đủ là 6,72 lít O2 (đktc), người ta thu được CO2 và H2O với tỉ lệ số mol tương ứng là 1:1
a. hỏi trong X có chứa những nguyên tố nào? Tính khối lượng của các nguyên tố có trong X
b. xác định công thức đơn giản của X
c. hãy tìm công thức phân tử của X, biết tỉ khối hơi của X so với He là d và 9<d<21
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ ĐLBTKL:m_{tg}=m_{sp}=m_X+m_{O_2}=m_{CO_2}+m_{H_2O}=9+0,3.32=18,6\left(g\right)\\ n_{CO_2}:n_{H_2O}=1:1\Rightarrow n_{CO_2}=n_{H_2O}\\ Đặt:n_{CO_2}=n_{H_2O}=t\left(mol\right)\left(t>0\right)\\ \Rightarrow44t+18t=18,6\\ \Leftrightarrow t=0,3\left(mol\right)\\ \Rightarrow n_C=n_{CO_2}=0,3\left(mol\right);n_H=2.0,3=0,6\left(mol\right)\\ Trong.X:m_C=0,3.12=3,6\left(g\right);m_H=0,6.1=0,6\left(g\right)\\ Vì:m_C+m_H=3,6+0,6=4,2< 9\\ \Rightarrow X.chắc.chắn.có.O\\ \Rightarrow X.có:C,H,O\\ m_O=9-4,2=4,8\left(g\right)\\ n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
\(b,Đặt.CTĐGN:C_iH_dO_q\left(i,d,q:nguyên,dương\right)\\ Ta.có:i:d:q=0,3:0,6:0,3=1:2:1\\ \Rightarrow CTĐGN:CH_2O\\ c,Ta.có:9< d_{\dfrac{X}{He}}< 21\\ \Leftrightarrow9< \dfrac{M_X}{4}< 21\\ \Leftrightarrow36< M_X< 84\\ Đặt.CTTQ:\left(CH_2O\right)_a\left(a:nguyên,dương\right)\\ \Leftrightarrow36< 30a< 84\\ \Leftrightarrow1,2< a< 2,8\\ \Rightarrow a=2\\ \Rightarrow CTPT:C_2H_4O_2\)
Chúc em học tốt!
Đúng 4
Bình luận (0)