Trong một bình kín chứa 2,24lít CH4 và 3,36 lít O2 đo ở cùng điều kiện về nhiệt độ và áp suất,bật tia lửa đốt cháy hỗn hợp.Tính thể tích các chất sau phản ứng.
Giải giúp mình với .Cảm mơn trước.
1 bình kín dung tích 2 lít ở 27,3 độ C chứa 0,03 mol C2H2;0,015 mol C2H4 và 0,04 mol H2 có bột Ni làm xúc tác.Nung nóng bình ở nhiệt độ cao để phản ứng xảy ra hoàn toàn,sau phản ứng đưa về nhiệt độ 27,3 độ C thì áp suất p1 trong bình là bao nhiêu?
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1 , 43 k g / m 3 + . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 o C bằng
A. 3,22 kg
B. 214,5 kg.
C. 7,5 kg
D. 2,25 kg
Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m / V 0
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 . V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 . V 0 = pV (2)
Từ (1) và (2) suy ra:
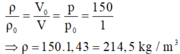
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1,43 kg/ m 3 + . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 o C bằng
A. 3,22 kg
B. 214,5 kg
C. 7,5 kg
D. 2,25 kg.
Chọn A.

Ở điều kiện tiêu chuẩn (1 atm, 0 o C ), khối lượng riêng của ôxi là: p 0 = m/ V 0 .
Ở điều kiện 150 atm, 0 o C , khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = p 0 V 0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p 0 V 0 = pV (2)
Từ (1) và (2) suy ra:
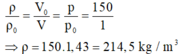
Và m = ρ . V = 214,5.15.10 − 3 ≈ 3,22 k g
Biết ở điều kiện tiêu chuẩn, khối lượng riêng của ôxi là 1 , 43 k g / m 3 . Khối lượng khí ôxi đựng trong một bình kín có thể tích 15 lít dưới áp suất 150 atm ở nhiệt độ 0 bằng
A. 3,23 kg.
B. 214,5 kg.
C. 7,5 kg.
D. 2,25 kg.
Chọn A.
Ở điều kiện tiêu chuẩn (1 atm, 0 oC), khối lượng riêng của ôxi là: ρ0 = m/V0.
Ở điều kiện 150 atm, 0 oC, khối lượng riêng của ôxi là: ρ = m/V.
Do đó: m = ρ0.V0 = ρ.V (1)
Do nhiệt độ không đổi, theo định luật Bôi-lơ – Ma-ri-ốt: p0V0 = pV (2)
Từ (1) và (2) suy ra:
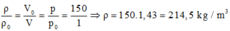
Và m = ρ.V = 214,5.15-3 ≈ 3,23 kg.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
A. 3 : 5.
B. 4 : 3.
C. 2 : 3
D. 3 : 2.
Chọn B.
Theo đề ta có: n O 2 = 1 , 225 ; n C O 2 = 1 , 05 v à n H 2 O = 1 , 05 => X no, đơn chức, mạch hở (vì n C O 2 = n H 2 O )
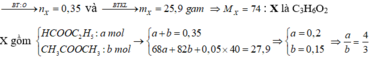
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai este đồng phân cần dùng 27,44 lít khí O2, thu được 23,52 lít khí CO2 và 18,9 gam H2O. Nếu cho m gam X tác dụng hết với 400ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thì thu được 27,9 gam chất rắn khan, trong đó có a mol muối Y và b mol muối Z (MY < MZ). Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Tỉ lệ a : b là
A. 3 : 5
B. 4 : 3
C. 2 : 3
D. 3 : 2
Đốt cháy hoàn toàn m gam chất béo X (chứa axit stearic, axit panmitic và các triglixerit của các axit này). Sau phản ứng thu được 20,16 lít CO2 (điều kiện tiêu chuẩn) và 15,66 gam nước. Xà phòng hóa m gam X (hiệu suất phản ứng bằng 90%) thì thu được khối lượng glixerol là
A. 2,484 gam
B. 1,242 gam
C. 1,380 gam
D. 2,760 gam
Hỗn hợp X gồm a mol Fe, b mol FeCO3 và c mol FeS2. Cho X vào bình dung tích không đổi chứa không khí (dư), nung bình đến khi các phản ứng xảy ra hoàn toàn sau đó đưa bình về nhiệt độ ban đầu, thấy áp suất trong bình bằng áp suất trước khi nung. Quan hệ của a, b, c là
A. a = b+c
B. 4a+4c=3b
C. b=c+a.
D. a+c=2b
Đáp án : C
2Fe + 1,5O2 -> Fe2O3
2FeCO3 + 0,5O2 -> Fe2O3 + 2CO2
2FeS2 + 5,5O2 -> Fe2O3 + 4SO2
Vì sau phản ứng thì áp suất trong bình không đổi
=> Số mol O2 phản ứng = số mol khí sinh ra
=> 0,75a + 0,25b + 2,75c = b + 2c
=> a +c = b
Đốt cháy 1,55g photpho trong bình kín chứa 1,12 lít khí oxi (đktc). a.Viết phương trình hóa học của phản ứng b.Sau phản ứng chất nào còn dư? Khối lượng (nếu P dư) hay thể tích (nếu O2 dư) là bao nhiêu?
a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{1,55}{31}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,05}{4}>\dfrac{0,05}{5}\), ta được P dư.
c, Theo PT: \(n_{P\left(pư\right)}=\dfrac{4}{5}n_{O_2}=0,04\left(mol\right)\Rightarrow n_{P\left(dư\right)}=0,05-0,04=0,01\left(mol\right)\)
\(\Rightarrow m_{P\left(dư\right)}=0,01.31=0,31\left(g\right)\)