Muối Sunfat có dạng RSO4 có khối luong phân tu là 160 đvC. Hỏi R là kim loại nào?
Help meeeeeeee

Những câu hỏi liên quan
Hỗn hợp X gồm 2 kim loại có tỉ lệ khối lượng 1: 1 và khối lượng mol nguyên tử cảu A nặng hơn B là 8g . Trong 53, 6 g có số mol A khác B là 0,0375 mol . Hỏi A,B là kim lạo nào ?
Các bạn giúp mk vs !!!!!
(A) và (B) có tỉ lệ khối lượng là 1:1
=>mA=mB=53.6/2=26.8(g)
MA-MB=8
=>MA=8+MB
nA khác B 0.0375mol
+TH1:nA>nB
=>nA-nB=0.0375
<=>26.8/8+MB-26.8/MB=0.0375
<=>0.0375MB^2+0.3MB+214.4=0
=>vô nghiệm
+TH2:nB>nA
=>nB-nA=0.0375
<=>26.8/MB-26.8/MB+8=0.0375
<=>0.0375MB^2+0.3MB-214.4=0
<=>MB=72(Gemani)
=>MA=72+8=80(Brom)
Vậy A là Brom,B là Gemani
Đúng 0
Bình luận (5)
câu 1 : nung 2,45g 1 muối vô cơ thấy thoát ra 0,96g khí oxi phần chất rắn còn lại chứa 52,35% kali và 47,65% clo. Tìm công thức phân tử của muối vô cơ đócâu 2 : có 1 muối nitrat trong đó nguyên tố kim loại chiếm 38,61% khối lượng . vậy trong oxit của kim loại đó thì nó chiếm bao nhiêu phần trăm và đó là kim loại nàobn nào biết thì giúp m nhé!!!!!
Đọc tiếp
câu 1 : nung 2,45g 1 muối vô cơ thấy thoát ra 0,96g khí oxi phần chất rắn còn lại chứa 52,35% kali và 47,65% clo. Tìm công thức phân tử của muối vô cơ đó
câu 2 : có 1 muối nitrat trong đó nguyên tố kim loại chiếm 38,61% khối lượng . vậy trong oxit của kim loại đó thì nó chiếm bao nhiêu phần trăm và đó là kim loại nào
bn nào biết thì giúp m nhé!!!!!![]()
câu 1 :một oxit kim loại ở mức hóa trị thấp chứa 77,78% kim loại còn lại là oxi , trong oxit của kim loại đó ở mức hóa trị cao thì chứa 70% khối lượng kim loại còn lại là oxi , hỏi đó là kim loại nào?câu 2:nếu hàm lượng phần trăm của 1 kim loại trong oxit là 60% thì trong muối xunfat của kim loại đó hàm lượng phần trăm của kim loại là bao nhiêu ?
Đọc tiếp
câu 1 :
một oxit kim loại ở mức hóa trị thấp chứa 77,78% kim loại còn lại là oxi , trong oxit của kim loại đó ở mức hóa trị cao thì chứa 70% khối lượng kim loại còn lại là oxi , hỏi đó là kim loại nào?
câu 2:
nếu hàm lượng phần trăm của 1 kim loại trong oxit là 60% thì trong muối xunfat của kim loại đó hàm lượng phần trăm của kim loại là bao nhiêu ?
bn nào hok giỏi hóa giúp mình với
Đúng 0
Bình luận (0)
Ngâm một lá kim loại có khối lượng 50g trong dung dịch HCl. Sau khi thu được 336ml khí H2 (đktc) thì khối lượng lá kim loại giảm 1,68%. Kim loại đó là kim loại nào?
A. Zn
B. Fe
C. Al
D. Ni
Đáp án B
Khối lượng kim loại phản ứng là:
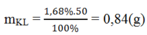
Số mol H2 là:
![]()
2M + 2nHCl → 2MCln + nH2
Số mol của M là:
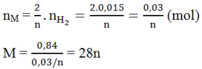
⇒ M = 28n ⇒ n = 2, M = 56 ⇒ M: Fe
Đúng 0
Bình luận (0)
Muối Sunfat có dạng RSO4 có khối lượng phân tử là 160 đvC. Hỏi R là kim loại nào?
Có: MRSO4 = 1.MR + 32.1 + 16.4 = 160
=> MR = 64(g/mol)
=> R là Cu
Đúng 0
Bình luận (0)
Ta có: R + 32 + 16 . 4 =160
<=> R = 64
Vậy R là kim loại đồng
Đúng 0
Bình luận (0)
Ta có:
\(NTK\left(R\right)+32+16.4=160\\ \Rightarrow NTK\left(R\right)+96=160\\ \Rightarrow NTK\left(R\right)=64\)
\(\Rightarrow R\) là đồng
Đúng 0
Bình luận (0)
Khi cho cùng một lượng kim loại M tác dụng với dung dịch HCl và H2SO4 đặc nóng thì khối lượng SO2 sinh ra gấp 48 lần H2 sinh ra. Mặt khác, khối lượng muối clorua bằng 31,75% khối lượng muối sunfat. Vậy M là:
A. Fe
B. Cu
C. Al
D. Mg
Đáp án A

Ta có: khối lượng SO2 =m/2.64 = 32m (g)
Khối lượng H2 = n/2.2 = n (g)
Theo đề ra: 32m = 48n
![]()
Vậy M có 2 hóa trị là 2 và 3.
Mặt khác:
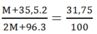
→ M = 56
Vậy M là Fe
Đúng 0
Bình luận (0)
Một khối kim loại hình hộp chữ nhật có chiều dài là o.26m;chiều rộng 0.25m và chiều cao là 0.24m.Mỗi khối kim loại hình lập phương cùng chất bằng trung bình cộng 3 kích thước của khối kim loại hình hộp chữ nhật trên.Biết rằng mỗi dề-xi-mét khối kim loại bằng 8kg.Tính:A,Tính thể tích mỗi khối kim loại đó.B,Hỏi khối đó cần dùng bao nhiêu ki-lô-gam? Ai giải nhanh nhất mình tick cho nha!
Đọc tiếp
Một khối kim loại hình hộp chữ nhật có chiều dài là o.26m;chiều rộng 0.25m và chiều cao là 0.24m.Mỗi khối kim loại hình lập phương cùng chất bằng trung bình cộng 3 kích thước của khối kim loại hình hộp chữ nhật trên.Biết rằng mỗi dề-xi-mét khối kim loại bằng 8kg.Tính:
A,Tính thể tích mỗi khối kim loại đó.
B,Hỏi khối đó cần dùng bao nhiêu ki-lô-gam?
Ai giải nhanh nhất mình tick cho nha!
Help mìnhB1: Biết 800g rượu có thể tích là 1la)Tính khối lượng riêng của rượub)Bao nhiêu lít nước sẽ có khối lượng bằng khối lượng của 800g rượu nói trênB2:1 mẩu hợp kim gồm chì và nhôm có khối lượnh là 500g. Khối lượng riêng là 6,8g/cm3.Hãy xác định khối lượng chì và nhôm mỗi loại. Biết khối lượng riêng của chì và nhôm lần lượt là : Dchì11,3g/cm3. Dnhôm2,7g/cm3 và xem rằng thể tích hợp kim90% tổng thể tích của các kim loại thành...
Đọc tiếp
Help mình
B1: Biết 800g rượu có thể tích là 1l
a)Tính khối lượng riêng của rượu
b)Bao nhiêu lít nước sẽ có khối lượng bằng khối lượng của 800g rượu nói trên
B2:1 mẩu hợp kim gồm chì và nhôm có khối lượnh là 500g. Khối lượng riêng là 6,8g/cm3.Hãy xác định khối lượng chì và nhôm mỗi loại. Biết khối lượng riêng của chì và nhôm lần lượt là : Dchì=11,3g/cm3. Dnhôm=2,7g/cm3 và xem rằng thể tích hợp kim=90% tổng thể tích của các kim loại thành phần
Các bạn giúp mình nhanh lên nhé.Sáng mai mình phải nộp rùi.Thanks
B1)
a) 800g = 0.8kg, 1l = 0.001 m3
Khối lượng riêng của rượu là :
D = m/v = 0.8 / 0.001 = 800
Vậy KLR của rượu 800 kg/m3
b) Vì KLR của nước là 1000kg/m3 có nghĩa là 1kg là trọng lượng của 1l nước.
800g là khối lượng của số lít nước là :
m = D.v <=> v = m/D = 0.8 / 1= 0.8 l
Đúng 0
Bình luận (0)
Cho 6,2 gam hỗn hợp gồm Na và một kim loại kiềm M có tỉ lệ số mol là 1:1 tác dụng với 104 gam nước, người ta thu được 110 gam dung dịch có khối lượng riêng là 1,1 g/ml. Vậy kim loại kiềm M là:
A. Li
B. K
C. Rb
D. Cs
Đáp án B
Phương trình phản ứng
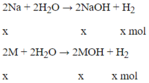
Theo đề bài ta có: 23x +Mx = 6,2 (1)
Áp dụng định luật bảo toàn khối lượng ta có:
mkim loại + mnước = mdd + mhiđro
Từ đó: mhiđro = mkim loại - mnước = mdd = 6,2 + 104 - 110 = 0,2 (g)
⇒x = 0,1 mol, thay vào (1) ta được M = 39 (K)
Đúng 0
Bình luận (0)
















