Cho 2,8g sắt tác dụng hết với axit HCl. Tính:
a. Thể tích khí hidro thu được ở đktc
b. Khối lượng axit HCl cần dùng
cho 2,8 gam sắt tác dụng với dung dịch axit clohiđric (HCL) thu được sắt (II) clorua và khí hiđro
a) tính thể tích khí hidro thu được ở đktc
b) tính khối lượng axit clohiđric cần dùng
c) dẫn khí hiđro sinh ra ở phản ứng đi qua bột CuO nung nóng, tính khối lượng đồng tạo thành sau phản ứng
a.b.
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05 0,1 0,05 ( mol )
\(V_{H_2}=0,05.22,4=1,12l\)
\(m_{HCl}=0,1.36,5=3,65g\)
c.
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,05 0,05 ( mol )
\(m_{Cu}=0,05.64=3,2g\)
Cho 28 gam sắt và 32,5 gam kẽm tác dụng với lượng dư axit clohidric (HCl).
a) Xác định thể tích khí hidro sinh ra ở đktc ?
b) Tính khối lượng axit đã dùng ?
a) \(n_{Fe}=\dfrac{28}{56}=0,5\left(mol\right);n_{Zn}=\dfrac{32,5}{65}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,5 1 0,5
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,5 1 0,5
\(V_{H_2}=\left(0,5+0,5\right).22,4=22,4\left(l\right)\)
b, \(m_{HCl}=\left(1+1\right).36,5=73\left(g\right)\)
sắt tác dụng với axit clohidric HCL theo sơ đồ phản ứng sau fe + HCL ---> FeCl2 +H2
nếu có 11,2 gam sắt tham gia phản ứng Hãy tính
a. khối lượng axit chohidric HCL cần dùng
b. thể tích khí hidro tạo thành ở đktc
( cho biết Fe = 56 ; Zn = 65 ; S=32; O = 16 ; K= 39; H=1 ; C=12; CL=35)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,2_____0,4__________0,2 (mol)
a, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Cho 2,4 gam magie tác dụng vừa đủ với dung dịch axit clohidric (HCl), thu được magie clorua (MgCl2) và khí hidro (H2)
a. Tính khối lượng HCl đã dùng.
b. Tính khối lượng MgCl2
c. Tính thể tích khí hidro thu được (đktc)
a) \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
_____0,1--->0,2------->0,1---->0,1
=> mHCl = 0,2.36,5 = 7,3(g)
b) mMgCl2 = 0,1.95 = 9,5 (g)
c) VH2 = 0,1.22,4 = 2,24(l)
8: Cho 28 gam sắt và 32,5 gam kẽm tác dụng với lượng dư axit clohidric (HCl).
a) Xác định thể tích khí hidro sinh ra ở đktc ?
b) Tính khối lượng axit đã dùng ?
nFe = 0.5 (mol)
nZn = 0.5 (mol)
Fe + 2HCl → FeCl2 + H2↑
0.5 1 0.5
Zn + 2HCl → ZnCl2 + H2↑
0.5 1 0.5
=> Tổng nH2 = 1 (mol) => VH2 = 22.4x1=22.4 (l)
b) Tổng nHCl = 2 (mol) => mHCl = 2x36.5=73 (g)
Cho 5,4 gam nhôm tác dụng với axit clohidic ( HCL) sau phản ứng thu được nhôm clorua (AlCl3) và khí hidro a.Tính khối lượng axit cần dùng b.Tính thể tích khí hidro thoát ra ở đktc
a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
______0,2-->0,6--------------->0,3
=> mHCl = 0,6.36,5 = 21,9 (g)
b) VH2 = 0,3.22,4 = 6,72 (l)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
______0,2-->0,6--------------->0,3
=> mHCl = 0,6.36,5 = 21,9 (g)
b) VH2 = 0,3.22,4 = 6,72 (l)
4. Cho kim loại sắt tác dụng với axit HCl thu được sắt (II) clorua và khí H2 a/ Tính khối lượng sắt và khối lượng axit biết thể tích hidro bằng 3,36 lít (đktc). b/ Tính khối lượng sắt clorua (FeCl2) tạo thành
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,3\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,3\cdot36,5=10,95\left(g\right)\\m_{Fe}=0,15\cdot56=8,4\left(g\right)\\m_{FeCl_2}=0,15\cdot127=19,05\left(g\right)\end{matrix}\right.\)
PTHH: Fe+2HCl→FeCl2+H2↑Fe+2HCl→FeCl2+H2↑
Ta có:
Cho 6 gam kim loại magie tác dụng hoàn toàn với dung dịch axit HCl.
a) Tính thể tích hiđro thu được ở đktc?
b) Tính khối lượng axit HCl phản ứng?
c) Lượng khí hiđro thu được ở trên cho tác dụng với 16 gam sắt (III) oxit. Tính khối lượng sắt thu được sau phản ứng
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,25.........0,5.........0,25.......0,25\left(mol\right)\\ a.V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b.m_{HCl}=0,5.36,5=18,25\left(g\right)\\ c.n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ Fe_2O_3+3H_2\underrightarrow{^{to}}2Fe+3H_2O\\ Vì:\dfrac{0,25}{3}< \dfrac{0,1}{1}\\ \Rightarrow Fe_2O_3dư\\ n_{Fe}=\dfrac{2}{3}.0,25=\dfrac{1}{6}\left(mol\right)\\ \Rightarrow m_{Fe}=\dfrac{1}{6}.56\approx9,333\left(g\right)\)
a,\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,25 0,5 0,25
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b,\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c,\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,25 \(\dfrac{1}{6}\)
Ta có: \(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)⇒ Fe2O3 dư, H2 hết
\(m_{Fe}=\dfrac{1}{6}.56=9,33\left(g\right)\)
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,25 0,5 0,25
a) \(n_{H2}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
\(V_{H2\left(dktc\right)}0,25.22,4=5,6\left(l\right)\)
b) \(n_{HCl}=\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
⇒ \(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c) \(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
Pt : \(3H_2+Fe_2O_3\rightarrow\left(t_o\right)2Fe+3H_2O|\)
3 1 2 3
0,25 0,1 \(\dfrac{1}{6}\)
Lập tỉ số so sánh : \(\dfrac{0,25}{3}< \dfrac{0,1}{1}\)
⇒ H2 phản ứng hết , Fe2O3 dư
⇒ Tính toán dựa vào số mol của H2
\(n_{Fe}=\dfrac{0,25.2}{3}=\dfrac{1}{6}\left(mol\right)\)
⇒ \(m_{Fe}=\dfrac{1}{6}.56=9,3\left(g\right)\)
Chúc bạn học tốt
Sắt tác dụng với axit clohiđric : Fe + 2HCl → FeCl2 + H2↑.
Nếu có 2,8g sắt tham gia phản ứng em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
a) PTPU

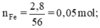
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)