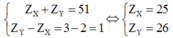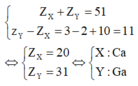Câu hỏi hay và khó :D
Bạn nào trả lời chính xác mình xin tặng 2 GP.
Đề bài như sau :
X thuộc chu kì 4, Y thuộc chu kì 2 của bảng tuần hoàn các nguyên tố hóa học. \(I_i\) là năng lượng ion hóa thứ i của một nguyên tử. Thực nghiệm cho biết tỉ số \(\dfrac{I_{k+1}}{I_k}\)của X và Y như sau :
| \(\dfrac{I_{k+1}}{I_k}\) | \(\dfrac{I_2}{I_1}\) | \(\dfrac{I_3}{I_2}\) | \(\dfrac{I_4}{I_3}\) | \(\dfrac{I_5}{I_4}\) | \(\dfrac{I_6}{I_5}\) |
| X | 1,94 | 4,31 | 1,31 | 1,26 | 1,30 |
| Y | 2,17 | 1,96 | 1,35 | 6,08 | 1,25 |
Hãy lập luận để xác định X và Y ?