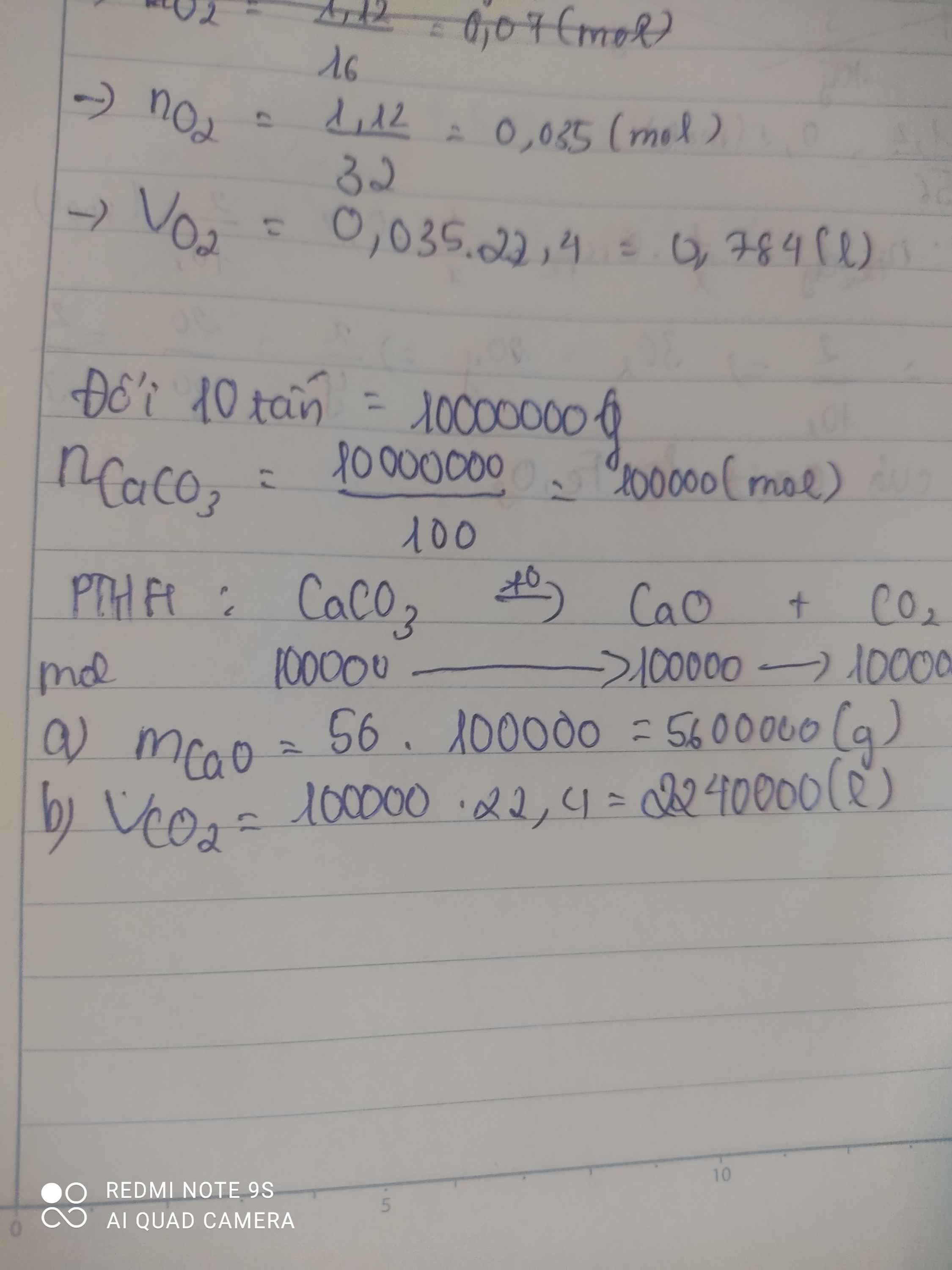một loại đá vôi có chứa 80% CaCo3. Nung 1 tấn đá vôi loại này có thể thu được bao nhiêu gam cao, biết h=90%

Những câu hỏi liên quan
Một loại đá vôi chứa 85% CaCO3 và 15% tạp chất không bị phân hủy ở nhiệt độ cao . Khi nung một lượng đá vôi đó thu được một chất rắn có khối lượng bằng 70% khối lượng đá trước khi nung
a, Tính hiệu suất quá trình phản ứng
b, Tính thành phần % khối lượng CaO trong chất rắn sau khi nung
tham khảo
a, Giả sử đem nung 100g đá vôi :
trong đó mCaCO3=100.85%=85(g )
m tạp chất=100-85=15(g )
khối lượng CO2 =100-70%.100=30(g )
PTHH: CaCO3----->CaO + CO2
100g------>56g---->44g
x-------> y-------->30g
m=Khối lượng CaCO3 bị nung là: mCaCO3= (30. 56 )/ 44= 68,2g
=>H%CaCO3 =68,2/ 85. 100%= 80,2%
b, Khối lượng CaO tạo thành là: mCaO= (30. 56)/ 44= 38.2(g)
Thành phần %CaO trong chất rắn sau khi nung là: m%CaO=38,2/70.100%=54.6%
Đúng 0
Bình luận (0)
Người ta nung 10 tấn đá vôi ( Canxi cacbonat ) Phản ứng tạo thành vôi sống CaO và khí Cacbonic.
a. Tính lượng vôi sống thu được
b. Tính thể tích Cacbonic sinh ra (đktc)?
PTHH : \(CaCO_3\left(t^o\right)->CaO+CO_2\uparrow\) (1)
10 tấn -> 10 000 000 g
\(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{10000000}{40+12+16.3}=\text{100000}\left(mol\right)\)
Từ (1) => \(n_{CaCO_3}=n_{CaO}=\text{100000}mol\)
=> \(m_{CaO}=n.M=100000.56=5600000\left(g\right)\)
b) Từ (1) => \(n_{CaCO_3}=n_{CO_2}=\text{100000}mol\)
=> \(V_{CO_2\left(đktc\right)}=n.22,4=100000.22,4=2240000\left(l\right)\)
Đúng 0
Bình luận (1)
Một loại đá có thành phần chính là CaCO3 và MgCO3, ngoài ra còn một số tạp chất trơ ( không tham gia vào các phản ứng hóa học trong quá trình thí nghiệm) . Để xác định thành phần phần trăm của CaCO3 và MgCO3 có trong loại đá trên , người ta lấy 10 gam bột đá đó cho phản ứng với dung dịch HCl loãng, dư, thu được 2,296 lít khí CO2 (ở đktc). Lọc bỏ tạp chất không tan. Cho toàn bộ phần nước lọc phản ứng với dung dịch NaOH loãng, dư, lọ...
Đọc tiếp
Một loại đá có thành phần chính là CaCO3 và MgCO3, ngoài ra còn một số tạp chất trơ ( không tham gia vào các phản ứng hóa học trong quá trình thí nghiệm) . Để xác định thành phần phần trăm của CaCO3 và MgCO3 có trong loại đá trên , người ta lấy 10 gam bột đá đó cho phản ứng với dung dịch HCl loãng, dư, thu được 2,296 lít khí CO2 (ở đktc). Lọc bỏ tạp chất không tan. Cho toàn bộ phần nước lọc phản ứng với dung dịch NaOH loãng, dư, lọc lấy kết tủa. Nung kết tủa đến khối lượng không đổi, thu được 2,4 gam chất rắn. Tính phần trăm khối lượng của CaCO3, MgCO3 trong loại đá nói trên.
CaCO3 + 2HCl -> CaCl2 + CO2 + H2O (1)
MgCO3 + 2HCl -> MgCl2 + CO2 + H2O (2)
MgCl2 + 2NaOH -> Mg(OH)2+ 2NaCl (3)
Mg(OH)2 -> MgO + H2O (4)
nMgO=0,06(mol)
nCO2=0,1025(mol)
=>nMgO=nMgCO3=0,06(mol)
mMgCO3=0,06.84=5,04(g)
Từ 2:
nCO2=nMgCO3=0,06(mol)
=>nCO2(1)=0,1025-0,06=0,0425(mol)
Từ 1:
nCaCO3=nCO2(1)=0,0425(mol)
mCaCO3=100.0,0425=4,25(g)
%mCaCO3=\(\dfrac{4,25}{10}.100\%=42,5\%\)
%mMgCO3=\(\dfrac{5,04}{10}.100\%=50,4\%\)
Đúng 0
Bình luận (5)
Quạng oxit sắt từ chứa 80% Fe3O4.Cần dùng bao nhiêu tấn kim loại quặng này để sản suất 100 tấn gang có 5% các nguyên tố không phải là sắt ?Biết rằng trong quá trình luyện gang lượng sắt bị hao hụt là 4%
Nung 5kg đá vôi có chứa 80% canxi cacbonat CaCO3 thu được canxi oxit CaO(vôi sống)và khí cacbon đioxit.Hãy tính khối lượng vôi sống thu được nếu hiệu suất phản ứng là 85%?
Nung 5kg đá vôi có chứa 80% canxi canbonat CaCo3 thu được canxi oxit CaO(vôi sống)và khí cacbon đioxit.Hãy tính khối lượng vôi sống thu được nếu hiệu suất phản ứng là 85%?
Một bể cá có chiều dài 2m, chiều rộng 1,2m và chiều cao 1m. Trong bể chứa nước có mực nước cao 0,6m. Người ta bỏ vào bể một hòn đá thì mực nước dâng cao lên 75% thể tích nước. Tính thể tích hòn đá.
Nhiệt phân đá vôi theo sơ đồ:
CaCO3 à CaO + CO2
Muốn điều chế 14 tạ vôi sống (CaO) thì cần bao nhiêu tạ đá vôi (CaCO3)?
14 tạ CaO=1,4 tấn CaO
nCaO=\(\dfrac{1,4}{56}=0,025kmol\)
PTHH: CaCO\(_3\)\(\rightarrow\)CaO+\(CO_2\)
0,025<--0,025-------
\(mCaCO_3=0,025.100=2,5\) tấn
Đúng 1
Bình luận (0)
Một loại đá vôi chứa 85% CaCO3 và 15% tạp chất không bị phân hủy ở nhiệt độ cao . Khi nung một lượng đá vôi đó thu được một chất rắn có khối lượng bằng 70% khối lượng đá trước khi nung
a, Tính hiệu suất phân hủy của CaCO3
b, Tính thành phần % khối lượng CaCO3 trong chất rắn sau khi nung
a)Đặt khối lượng đá vôi là 100g.
\(m_{CaCO_3}=\frac{100.85}{100}=85g\)
⇒m tạp chất=15g
\(n_{CaCO_3}=\frac{m}{M}=\frac{85}{100}=0,85mol\)
Gọi số mol \(CaCO_3\) phản ứng là x mol.
PTHH:
\(CaCO_3\)→\(t^o\)CaO +\(CO_2\)
bđ 0,85 0 0 (mol)
pứ x x x (mol)
spứ 0,85-x x x (mol)
\(m_{CR}\) spứ= \(m_{CaCO_3}\) dư + \(m_{CaO}\)+ m tạp chất
= 100(0,85-x) + 56x +15
=85 -100x +56x +15
=100-44x(g)
\(\frac{m_{CR}spu}{m_{CR}bd}=70\%\)
⇔\(\frac{100-44x}{100}=\frac{7}{10}\)
⇔700=1000-440x
⇔440x=300
⇔x=\(\frac{15}{22}\)mol
Vì là phản ứng phân hủy
⇒\(n_{CaCO_3}LT=n_{CaCO_3}bd=0,85mol\)
\(H=\frac{n_{CaCO_3}TT}{n_{CaCO_3}LT}.100=\frac{\frac{15}{22}}{0,85}.100=80,21\%\)
b)\(m_{CR}spu=\frac{100.70}{100}=70g\)
\(m_{CaCO_3}du=n.M=\left(0,85-\frac{15}{22}\right).100=16,82g\)
\(\%m_{CaCO_3}du=\frac{m_{CaCO_3}du}{m_{CR}spu}.100=\frac{16,82}{70}.100=24,03\%\)
Đúng 1
Bình luận (0)
\(n_{CaCO_3}=x\)
\(PTHH:CaCO_3\underrightarrow{t^o}CaO+CO_2\)
(mol)_____0,85x____0,85x___0,85x
Theo đề: \(n_{CaCO_3}=85\%x=0,85x\left(mol\right)\)
Ta có: \(\left\{{}\begin{matrix}\%CaCO_3+\%tc=85\%+15\%\\\%hhcr+\%tc=\frac{70\%}{100\%}\end{matrix}\right.\Leftrightarrow\%CaCO_3-\%hhcr=100-70=30\%\\ \rightarrow CaCO_3\cdot du\cdot30\%\)
\(pt:m_{cr}=m_{CaO}+m_{tapchat}+m_{CaCO_3du}\\ \Leftrightarrow47,6x+15\%x+0,255x=70\%\\ \Leftrightarrow x=0,015\left(mol\right)\)
\(H=\frac{0,015.\left(0,85-0,255\right)}{0,015}.100\%=59,5\%\)
\(\left\{{}\begin{matrix}\%m_{CaCO_3.pu}=85-30=55\left(\%\right)\\\%m_{CaCO_3.du}=30\left(\%\right)\end{matrix}\right.\)
( k chắc :''>)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời