Hợp chất hữu cơ A ở thể khí, đốt cháy hoàn toàn 5,6 lít khí A (ở đktc) thu đc 22g khí cacbonic và 9g H2O?
a) Xác định CTPT của A. Biết rằng 1lít khí A ở đktc có khối lượng= 1,25gb) Viết CTCT của A
đốt cháy hoàn toàn 5,6 lít khí A(đktc) thu được 22g CO2 và 9g H2O.Xác định công thức phân tử của A biết 1 lít khí A ở đktc có khối lượng 1,25g
\(n_C = n_{CO_2} = \dfrac{22}{44} = 0,5(mol)\\ n_H = 2n_{H_2O} = 2.\dfrac{9}{18} = 1(mol)\\ n_A = \dfrac{5,6}{22,4} = 0,25(mol)\\ M_A = \dfrac{1,25}{\dfrac{1}{22,4}}= 28\)
Số nguyên tử Cacbon = \(\dfrac{n_C}{n_A} = \dfrac{0,5}{0,25} = 2\)
Số nguyên tử Hidro = \(\dfrac{n_H}{n_A} = \dfrac{1}{0,25}=4\)
Số nguyên tử Oxi = \(\dfrac{28-12.2-4}{16} = 0\)
CTPT của A: \(C_2H_4\)
a/ 1 lit khí A thì có khối lượng 1,25g suy ra 5,6 lít khí A có khối lượng là: 5,6.1,25=7(g)5,6.1,25=7(g)
⇒MA=1,25122,4=28⇒MA=1,25122,4=28
Gọi công thức tổng quát của A là CxHyOz
nC=nCO2=2244=0,5nC=nCO2=2244=0,5
⇒mC=0,5.12=6⇒mC=0,5.12=6
nH=2.nH2O=2.918=1nH=2.nH2O=2.918=1
⇒mH=1.1=1⇒mH=1.1=1
⇒mO=7−6−1=0⇒mO=7−6−1=0
⇒z=0⇒z=0
Ta có: 612x=1y=728=0,25612x=1y=728=0,25
⇒{x=2y=4⇒{x=2y=4
Vậy A là C2H4
Hợp chất hữu cơ A ở thể khí, đốt cháy hoàn toàn 5,6 lít khí A (ở đktc) thu đc 22g khí cacbonic và 9g H2O?
a) Xác định CTPT của A. Biết rằng 1lít khí A ở đktc có khối lượng= 1,25ga/ 1 lit khí A thì có khối lượng 1,25g suy ra 5,6 lít khí A có khối lượng là: \(5,6.1,25=7\left(g\right)\)
\(\Rightarrow M_A=\frac{1,25}{\frac{1}{22,4}}=28\)
Gọi công thức tổng quát của A là CxHyOz
\(n_C=n_{CO_2}=\frac{22}{44}=0,5\)
\(\Rightarrow m_C=0,5.12=6\)
\(n_H=2.n_{H_2O}=2.\frac{9}{18}=1\)
\(\Rightarrow m_H=1.1=1\)
\(\Rightarrow m_O=7-6-1=0\)
\(\Rightarrow z=0\)
Ta có: \(\frac{6}{12x}=\frac{1}{y}=\frac{7}{28}=0,25\)
\(\Rightarrow\left\{\begin{matrix}x=2\\y=4\end{matrix}\right.\)
Vậy A là C2H4
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
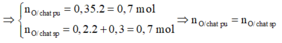
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
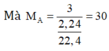
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
đốt cháy hoàn toàn 11,2 lít khí A đktc,thu được 11,2 lít CO2 và 9g H2O.Tìm CTPT A biết 1 lít khí A ở đktc có khối lượng 1,34g
\(n_C = n_{CO_2}= \dfrac{11,2}{22,4} = 0,5(mol)\\ n_H = 2n_{H_2O} = 2.\dfrac{9}{18} = 1(mol)\\ n_A = \dfrac{11,2}{22,4} = 0,5(mol)\\ M_A = \dfrac{1,34}{\dfrac{1}{22,4}}=30\)
Số nguyên tử Cacbon = \(\dfrac{n_C}{n_A} = \dfrac{0,5}{0,5} = 1\)
Số nguyên tử Hidro = \(\dfrac{n_H}{n_A} = \dfrac{1}{0,5} = 2\)
Số nguyên tử Oxi = \(\dfrac{30-12-2}{16}=1\)
Vậy CTPT của A :CH2O
Cho hợp chất hữu cơ a ở thể khí đốt cháy hoàn toàn 5,6 lít khí A ở điều kiện tiêu chuẩn thu được 22 gam CO2 và 9 gam nước. xác định công thức hóa học của phân tử là biết một lít khí A ở điều kiện tiêu chuẩn có khối lượng là 1,25 g
do hỗn hợp thu đc chỉ có CO2 và H2O => ct CxHy mà nCO2=O,5 mol , nH2O=0,5mol,=>đó là anken CnH2n
na=0,25 mol . áp dụng bảo toàn nguyên tố ooxxi t có nO2=(2nCO2+nH2O)/2=0.75mol
bảo toàn khối lượng => mhh=mCO2+mH2O-mO2=7g
=>Mhh=28 =>anken chính là C2H4
minh hoc lop 9. định luật nay chua hoc ạ
nếu hk tới laoij bài toán này rồi thì phải hk mấy định luật bảo toàn nguyên tố bỏa toàn khối lương rồi chứ nhỉ.
chị học bách khoa hà nội khoa hóa nhé
.Đốt cháy hoàn toàn 11,2 lít hợp chất A bởi Oxi thu được 11,2 lít khí cacbonic và 18 gam nước. Xác định công thức của A, biết rằng tỷ khối của khí A so với khí H2 bằng 8 (giả sử các khi đều đo ở đktc)help me
$n_{CO_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
$n_{H_2O} = \dfrac{18}{18} = 1(mol)$
Bảo toàn nguyên tố C,H :
$n_C = n_{CO_2} = 0,5(mol)$
$n_H = 2n_{H_2O} = 2(mol)$
$n_A = \dfrac{11,2}{22,4} = 0,5(mol)$
Số nguyên tử $C = \dfrac{0,5}{0,5} = 1$
Số nguyên tử $H = \dfrac{2}{0,5} = 4$
Mà : $M_A = 8.2 = 16$
$\Rightarrow A$ là $CH_4$
đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu đc 4,48l CO2(đktc) và 3,6g h2o a: tính CTPT của A biết MA= 60g/mol b: dẫn toàn bộ lượng CO2 qua dd Ca(OH)2 tính khối lượng khí thu đc
a.Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{3,6}{18}=0,4mol\)
\(n_O=\dfrac{6-\left(0,2.12+0,4.1\right)}{16}=0,2mol\)
=> A gồm C,H và O
\(CTPT:C_xH_yO_z\)
\(x:y:z=0,2:0,4:0,2=2:4:2\)
\(CTĐG:\left(C_2H_4O_2\right)n=60\)
\(\Leftrightarrow n=1\)
Vậy CTPT A: \(C_2H_4O_2\) hay \(CH_3COOH\)
b.\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 ( mol )
\(m_{CaCO_3}=0,2.100=20g\)
Hợp chất hữu cơ A ở thể khí đốt cháy hoàn toàn 5,6 lít khí A thu được 22 gam CO2 và 9 gam H2O .tìm công thức phân tử của a biết 1 lít khí ở điều kiện tiêu chuẩn có khối lượng là 1,25 g.. lớp 9 nhé
đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A thu được 8,8 gam khí CO2 và 3,6 gam H2O a) hợp chất chứa những nguyên tố hóa học nào ?
b)Xác định CTPT của A biết khối lượng mol của A là 60 gam
c) Viết CTCT chi tiết và thu gọn của A biết phân tử A có nhóm-COOH
d) Viết PTHH của A với dung dịch NaOH
GIÚP MÌNH VỚI Ạ MÌNH CẢM ƠN
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\) -> \(n_C=0,2\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\) -> \(n_H=0,4\)
\(m_C+m_H=0,2.12+0,4=2,8\left(g\right)\)
-> Trong A có \(m_O=6-2,8=3,2\left(g\right)\)
\(n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là \(C_xH_yO_z\)
\(x:y:z=n_C:n_H:n_O=0,2:0,4:0,2=1:2:1\)
\(\Leftrightarrow\left(CH_2O\right)_n=60.\Rightarrow n=2\)
a. CTPT của A là \(C_2H_4O_2\)
b. CTCT thu gọn:
\(CH_3COOH\)
mình không gõ được CTCT chi tiết (bạn lên mạng xem nhé)
c. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)