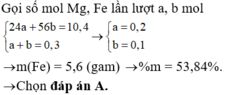Khi Clo hóa 9,2 gam hỗn hợp bột Mg và Fe cần 6,72 lít khí Cl2 (đktc) Thành phần phần trăm khối lượng của Mg trong hỗn hợp là:

Những câu hỏi liên quan
Khi clo hóa 20 gam một hỗn hợp bột gồm Mg và Cu cần phải dùng 1,12 lít khí clo đktc. Thành phần phần trăm của Mg trong hỗn hợp là
Sửa đề: "Clo hóa 2 gam hỗn hợp Mg và Cu"
Gọi a và b lần lượt là số mol của Mg và Cu
\(\Rightarrow24a+64b=2\) (1)
Ta có: \(n_{Cl_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Bảo toàn electron: \(2a+2b=0,1\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,02\end{matrix}\right.\)
\(\%m_{Mg}=\dfrac{0,03\cdot24}{2}\cdot100\%=36\%\)
Đúng 1
Bình luận (0)
Sửa đề: 1,12 \(\to\) 11,2
\(n_{Mg} = a\ mol ;n_{Cu} = b\ mol\\ \Rightarrow 24a + 64b = 20(1)\\ Mg + Cl_2 \xrightarrow{t^o} MgCl_2\\ Cu + Cl_2 \xrightarrow{t^o} CuCl_2\\ n_{Cl_2} = a + b = \dfrac{11,2}{22,4} = 0,5(2)\\ (1)(2) \Rightarrow a = 0,3 ; b = 0,2\\ \Rightarrow \%m_{Mg} = \dfrac{0,3.24}{20}.100\% =36\%\)
Đúng 0
Bình luận (1)
nMg=x,nCu=y
24x +64y=20
2x + 2y =0.05*2
=>x=-0.42 => đề sai
Đúng 1
Bình luận (0)
Đốt cháy hỗn hợp bột Al và Mg cần 16,8 lít khí oxi (đktc). Biết lượng Al trong hỗn hợp là 13,5 gam . Tính thành phần phần trăm theo khối lượng của Mg trong hỗn hợp đó?
PTHH: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (1)
\(2Mg+O_2\underrightarrow{t^o}2MgO\) (2)
Ta có: \(\left\{{}\begin{matrix}n_{O_2\left(1\right)}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}\cdot\dfrac{13,5}{27}=0,375\left(mol\right)\\n_{O_2\left(1\right)}+n_{O_2\left(2\right)}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(2\right)}=0,375\left(mol\right)\) \(\Rightarrow n_{Mg}=0,75\left(mol\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,75\cdot24}{0,75\cdot24+13,5}\cdot100\%\approx57,14\%\)
Đúng 1
Bình luận (0)
Cho 9,2 gam hỗn hợp Fe và Mg vào dung dịch HNO3 thu được 4,48 lít khí NO (đktc). Tính thành phần phần trăm theo khối lượng từng kim loại trong hỗn hợp.
\(n_{NO}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Gọi số mol Fe, Mg là a, b (mol)
=> 56a + 24b = 9,2 (1)
Fe0 - 3e --> Fe+3
a-->3a
Mg0 - 2e --> Mg+2
b-->2b
N+5 + 3e --> N+2
0,6<--0,2
Bảo toàn e: 3a + 2b = 0,6 (2)
(1)(2) => a = 0,1 (mol); b = 0,15 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{9,2}.100\%=60,87\%\\\%m_{Mg}=\dfrac{0,15.24}{9,2}.100\%=39,13\%\end{matrix}\right.\)
Đúng 4
Bình luận (1)
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là
A. 53,84%.
B. 80,76%.
C. 64,46%.
D. 46,15%.
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là: A. 53,84% B. 80,76 % C. 64,46 % D. 46,15 %
Đọc tiếp
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là:
A. 53,84%
B. 80,76 %
C. 64,46 %
D. 46,15 %
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là:
A. 53,84%
B. 80,76 %
C. 64,46 %
D. 46,15 %
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là:
A. 53,84%
B. 80,76 %
C. 64,46 %
D. 46,15 %
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là: A. 53,84% B. 80,76 % C. 64,46 % D. 46,15 %
Đọc tiếp
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là:
A. 53,84%
B. 80,76 %
C. 64,46 %
D. 46,15 %
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là
A. 53,84%
B. 80,76 %
C. 64,46 %
D. 46,15 %