Khi cho 0,6 g một kim loại nhóm IIA tác dụng với nước tạo ra 0,336 lít khí hiđro (ở đktc). Xác định kim loại đó.

Những câu hỏi liên quan
Khi cho 0,6g một kim lại nhóm IIA tác dụng với nước tạo ra 0,336 lít khí hiđro (ở điều kiện tiêu chuẩn). Xác định kim loại đó.
Gọi kí hiệu, nguyên tử khối của kim loại là M, kim loại M có 2 electron lớp ngoài cùng nên có hóa trị II.
M + 2H2O → M(OH)2 + H2.
nH2 = 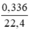 = 0,015 mol.
= 0,015 mol.
nM = 0,015.
→ 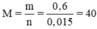 . Suy ra nguyên tử khối là 40u.
. Suy ra nguyên tử khối là 40u.
Vậy nguyên tố kim loại là Ca.
Đúng 0
Bình luận (0)
Khi cho 0,9 gam một kim loại nhóm IIA tác dụng với nước tạo ra 0,504 lít khí hiđro (ở đktc) . Xác định tên kim loại đó?
Gọi kim loại cần tìm là R.
\(n_{H_2}=\dfrac{0,504}{22,4}=0,0225mol\)
\(R+H_2O\rightarrow RO+H_2\)
0,0225 0,0225
Mà \(n_R=\dfrac{m_R}{M_R}=\dfrac{0,9}{M_R}=0,0225\Rightarrow M_R=40\left(đvC\right)\)
Vậy R là nguyên tố canxi.
KHHH: Ca
Đúng 0
Bình luận (0)
Khi cho 0,6g kim loại thuộc nhóm nhóm IIA tác dụng với 200 ml nước thì có 0,336 lít khí thoát ra (đktc). Xác định tên kim loại đó và nồng độ mol dung dịch thu được ( biết thể tích dung dịch thay đổi không đáng kể)
Câu 2 : Khi cho 3,25 gam một kim loại nhóm II tác dụng với dung dịch HCl tạo ra 1,12 lít khi hiđro (ở đktc). Xác định tên kim loại.
\(R+2HCl\rightarrow RCl_2+H_2\)
Theo PT : nH2=nR=0,05 (mol)
=> \(M_R=\dfrac{3,25}{0,05}=65\left(Zn\right)\)
Đúng 2
Bình luận (0)
nH2=0,05( mol)
Gọi KL hóa trị II là R.
PTHH: R + 2 HCl -> RCl2 + H2
nR=nH2=0,05(mol)
=>M(R)= 3,25/0,05=65(g/mol)
=>R(II) cần tìm là kẽm (Zn=65)
Đúng 1
Bình luận (0)
. Cho 8 gam một kim loại R thuộc nhóm IIA tác dụng hết với nước tạo ra 4,48 lít khí hiđro (đktc). Tìm tên kim loại R. (biết Mg=24, Be=9, Ca=40, Ba=137)
$R + 2HCl \to RCl_2 + H_2$
$n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
Theo PTHH : $n_R = n_{H_2} = 0,2(mol)$
$\Rightarrow M_R = \dfrac{8}{0,2} = 40$
Vậy R là Canxi
Đúng 1
Bình luận (0)
Bài 1: Cho 5.52g một kim loại kiềm tác dụng với nước tạo ra 2.688 lít khí H2 (đktc). Xác định tên kim loại đó.
Bài 2: Cho 1.84g một kim loại kiềm tác dụng với nước tạo ra 896ml khí H2 (đktc). Xác định tên kim loại đó.
Bài 1:
Gọi kim loại kiềm là R
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Giả sử R hóa trị I:
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\\ \Rightarrow n_R=0,12.2=0,24\left(mol\right)\\ \Rightarrow M_R=\dfrac{5,52}{0,24}=23\left(đvC\right)\)
Giả sử đúng, tên kim loại đó là sodium (Na)
Bài 2: Tự làm tương tự bài 1 nhé=0
Đúng 2
Bình luận (0)
Cho 8,8 gam một hỗn hợp gồm 2 kim loại ở 2 chu kì liên tiếp thuộc nhóm IIA tác dụng với dd HCl dư cho 6,72 lít khí hiđro ở đktc. Xác định tên 2 kim loại và % khối lượng mỗi kl trong hh ban đầu.
Đọc tiếp
Cho 8,8 gam một hỗn hợp gồm 2 kim loại ở 2 chu kì liên tiếp thuộc nhóm IIA tác dụng với dd HCl dư cho 6,72 lít khí hiđro ở đktc. Xác định tên 2 kim loại và % khối lượng mỗi kl trong hh ban đầu.
Gọi công thức chung của 2 kim loại là R
\(HCIII\text{R + 2HCl -> RCl2 + H2}I->RCI2+H2\)
Ta có : \(nH2=0,3mol->M\text{ R}=8,8\)/\(0,3=29,3\)
Ta có : \(\text{24 < 29,3 < 40 nên 2 kim loại là Mg và Ca}\)
Gọi số mol Mg và Ca lần lượt là x , y
\(\text{-> x+y=0,3; 24x+40y=8,8}\)
Giải được \(\text{x = 0,2 ; y = 0,1 }\)
\(\text{-> mMg=24.0,2=4,8 gam -> %Mg=54,5% -> %Ca=45,5%}\)
Đúng 1
Bình luận (0)
X là kim loại thuộc nhóm IIA. Cho 1,7 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 0,672 lít khí H2 (ở đktc). Mặt khác, khi cho 1,9 gam X tác dụng với lượng dư dung dịch
H
2
S
O
4
loãng, thì thể tích khí hiđro sinh ra chưa đến 1,12 lít (ở đktc). Kim loại X là A. Ba B. Ca C. Sr D. Mg
Đọc tiếp
X là kim loại thuộc nhóm IIA. Cho 1,7 gam hỗn hợp gồm kim loại X và Zn tác dụng với lượng dư dung dịch HCl, sinh ra 0,672 lít khí H2 (ở đktc). Mặt khác, khi cho 1,9 gam X tác dụng với lượng dư dung dịch H 2 S O 4 loãng, thì thể tích khí hiđro sinh ra chưa đến 1,12 lít (ở đktc). Kim loại X là
A. Ba
B. Ca
C. Sr
D. Mg
Cho 0,21 gam một kim loại kiềm tác dụng với nước (dư), thu được 0,336 lít khí hiđro (ở đktc). Kim loại kiềm là:
A. K.
B. Li.
C.Rb.
D. Na.
Chọn đáp án B
Gọi kim loại kiềm chưa biết là R.
Áp dụng định luật bảo toàn e ta có
![]()
⇒ Chọn B
Đúng 0
Bình luận (0)





















