cần phải dùng 150ml dd HCL a mol/lít để kết tủa hoàn toàn 200g dd AgNo3 8,5%. tính nồng độ dd HCL

Những câu hỏi liên quan
Tính nồng độ của hai dung dịch axit clohiđric trong các trường hợp sau:
a) Cần phải dùng 150ml dung dịch HCl để kết tủa hoàn toàn 200g dung dịch AgNO3 8,5%.
b) Khi cho 50g dung dịch HCl vào một cốc đựng NaHCO3 (dư) thì thu được 2,24 lít khí ở đktc.
a) 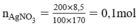
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
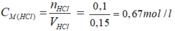
b) 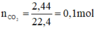
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
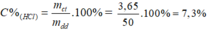
Đúng 0
Bình luận (0)
Tính nồng độ của hai dung dịch axit clohidric trong các trường hợp sau:
a)Cần phải dùng 150ml dung dịch HCl để kết tủa hoàn toàn 200g dung dịch AgNO3 8,5%.
b) Khi cho 50g dung dịch HCl vào một cốc đựng NaHCO3 thì thu được 2,24 lít khí ở đktc.
a)
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
b)
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g ( mình viết ko được rõ )
a.
mAgNO3 = (200.8,5%)/100 =17g
nAgNO3 = 17/170= 0,1 mol
để kết tủa hoàn toàn thì nAgNO3=nHCl = 0,1 mol
CHCl=0,1/0,15=2/3 (M)
b.
HCl + NaHCO3 =====> NaCl + CO2 + H2O
nCO2 = 0,1 mol=nHCl (theo pt)
mHCl =3,65 g
%CHCl = (3,65/50) .100% =7,3%
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
b)
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
cho 100ml dd CuCl2 2M tác dụng vừa đủ với V lít dung dịch NaOH 1M
a) tính khối lượng kết tủa thu được
b) tính nồng độ mol dd thu được sau phản ứng
c) hòa tan hoàn toàn lượng kết tủa trên bằng dd HCl 2M (d=1,1g/mol)
tính khối lượng dd HCl cần dùng
Hoà tan 1,35g KL R hoá trị III bằng 500ml dd HCl(d=1,2g/ml) lấy dư, thu đc dd X và 1,68 lít khí thoát ra ở đktc. a/ xác định tên KL b/ Lấy 1/2 dd X. Cho từ từ dd AgNO3 đến khi kết tủa hoàn toàn, thu đc 14,35g kết tủa. Tính nồng độ mol/lit của dd HCl đã dùng c/ Tính C% của X
Hoà tan 1,35g kim loại R hoá trị III bằng 500ml dd HCl (d=1,2g/ml) lấy dư, thu đc dd X và 1,85925 lít khí thoát ra ở đkc.
a/ Xác định tên kim loại.
b/ Lấy 1/2 dd X. Cho từ từ dd AgNO3 đến khi kết tủa hoàn toàn, thu đc 14,35g kết tủa. Tính nồng độ mol/L của dd HCl đã dùng.
c/ Tính C% của X.
\(n_{H_2}=\dfrac{1,85925}{24,79}=0,075\left(mol\right)\)
\(m_{dd.HCl}=500.1,2=600\left(g\right)\)
\(2R+6HCl\rightarrow2RCl_3+3H_2\)
0,05<-0,15<--0,05<----0,075
a. \(R=\dfrac{1,35}{0,05}=27\left(g/mol\right)\)
Vậy tên kim loại là nhôm (Al)
b.
\(n_{AgCl}=\dfrac{14,35}{143,5}=0,1\left(mol\right)\)
\(HCl+AgNO_3\rightarrow AgCl+HNO_3\)
0,025<-------------0,025
\(AlCl_3+3Ag\left(NO_3\right)\rightarrow3AgCl+Al\left(NO_3\right)_3\)
0,025------------------->0,075
\(CM_{HCl.đã.dùng}=\dfrac{0,025}{0,5}=0,05M\)
c.
\(m_{dd.X}=1,35+600-0,075.2=601,2\left(g\right)\)
\(n_{HCl.dư}=0,025.2=0,05\left(mol\right)\)
\(C\%_{AlCl_3}=\dfrac{0,05.133,5.100\%}{601,2}=1,11\%\)
\(C\%_{HCl.dư}=\dfrac{0,05.36,5.100\%}{601,2}=0,3\%\)
Đúng 3
Bình luận (0)
Cho 5,6 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dd Ca(OH)2
a, Tính nồng độ mol của dd Ca(OH)2 đã dùng ?
b, Tính khối lượng chất kết tủa thu được ?
c, Để trung hòa hết lượng dd Ca(OH)2 trên cần dùng bao nhiêu gam dd HCl nồng độ 20%
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}=n_{CO_2}=0,25\left(mol\right)\)
a, \(C_{M_{Ca\left(OH\right)_2}}=\dfrac{0,25}{0,1}=2,5\left(M\right)\)
b, \(m_{CaCO_3}=0,25.100=25\left(g\right)\)
c, \(Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\)
Theo PT: \(n_{HCl}=2n_{Ca\left(OH\right)_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,5.36,5}{20\%}=91,25\left(g\right)\)
Đúng 2
Bình luận (1)
Cho trộn 150ml dd H2SO4 0,1M với 250ml dd NaOH 0,1M.Sau phản ứng thu được dd X
1.Nhúng quỳ tím vào dd X.Quỳ tím có màu gì
2.tính nồng độ mol của mỗi chất trong X
3.Cần phải dùng dd KOH 1M hay dd HCl 0,1M để trung hoà dd X?Thể tích dd đã dùng
nNaOH=0,025mol
nH2SO4=0,015mol
2NaOH+H2SO4->Na2SO4+2H2O
Ta có 0,025/2 <0,015/1 =>H2SO4 dư
Khi nhúng quì tím vào dd thì quì tím chuyển sang màu đỏ
2NaOH+H2SO4->Na2SO4+2H2O
0,025 0,0125 0,0125
DD X: H2SO4:0,0025mol
Na2SO4: 0,0125mol
C(H2SO4)=0,00625M
C(NaOH)=0,03125M
Đúng 4
Bình luận (0)
3. Cần dùng KOH 1M để trung hòa dd X
H2SO4+2KOH->K2SO4+H2O
0,0025 0,005
V(KOH)=n/C=0,005lit=5ml
Đúng 4
Bình luận (0)
Cho trộn 150ml dd NaOH 0,1M với 250ml dd H2SO4 0,1M.Sau phản ứng thu được dd X
1.Nhúng quỳ tím vào dd X.Quỳ tím có màu gì
2.tính nồng độ mol của mỗi chất trong X
3.Cần phải dùng dd KOH 1M hay dd HCl 0,1M để trung hoà dd X?Thể tích dd đã dùng
1) $n_{NaOH} = 0,015(mol) ; n_{H_2SO_4} = 0,025(mol)$
$2NaOH + H_2SO_4 \to Na_2SO_4 + H_2O$
Ta thấy :
$n_{NaOH} : 2 < n_{H_2SO_4} : 1$ nên $H_2SO_4$ dư
Do đó quỳ tím hóa đỏ.
2)
$n_{Na_2SO_4} = \dfrac{1}{2}n_{NaOH} = 0,0075(mol)$
$n_{H_2SO_4\ dư} = 0,025 - 0,0075 = 0,0175(mol)$
$V_{dd\ X} = 0,15 + 0,25 = 0,4(lít)$
Suy ra :
$C_{M_{Na_2SO_4}} = \dfrac{0,0075}{0,4} = 0,01875M$
$C_{M_{H_2SO_4\ dư}} = \dfrac{0,0175}{0,4} = 0,04375M$
3)
$2KOH + H_2SO_4 \to K_2SO_4 + H_2O$
$n_{KOH} = 2n_{H_2SO_4\ dư} = 0,035(mol)$
$V_{dd\ KOH} =\dfrac{0,035}{1} = 0,035(lít)$
Đúng 3
Bình luận (0)
Cho 1 khối lượng mạt sắt dư vào 150ml dd HCl. Sau phản ứng thu được 10,08 lít khí (đktc)
a. Tính khối lượng mạt sắt tham gia phản ứng
b. Tính nống độ mol của dd HCl đã dùng
c. Cho toàn bộ muối trên tác dụng dd NaOH. Lọc kết tủa nung trong không khí đến khối lượng không đổi .Tính khối lượng chất rắn thu được sau khi nung
Ta có: \(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
a, \(n_{Fe}=n_{H_2}=0,45\left(mol\right)\Rightarrow m_{Fe}=0,45.56=25,2\left(g\right)\)
b, \(n_{HCl}=2n_{H_2}=0,9\left(mol\right)\) \(\Rightarrow C_{M_{HCl}}=\dfrac{0,9}{0,15}=6\left(M\right)\)
c, \(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_2}=\dfrac{1}{2}n_{FeCl_2}=\dfrac{1}{2}n_{H_2}=0,225\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,225.160=36\left(g\right)\)
Đúng 3
Bình luận (1)




















