Hoà tan hoàn toàn 11,68 g Cu và CuO trong 2 (l) dung dịch HNO3 0,25M thu được 1,792 (l) khí NO (đktc). Tính thành phần phần trăm về khối lượng của Cu và CuO trong hỗn hợp đầu.
Bài 9: Axit nitric à muối nitrat
3Cu+8HNO3->3Cu(NO3)2+2NO+4H2O
nNO=1,792/22,4=0,08(mol)
mCu=0,12x64=7,68(g)
=>mCuO=4(g)
%mCuO=4/11,68x100=34,25%
Đúng 0
Bình luận (0)
3Cu+8HNO3->3Cu(NO3)2+2NO+4H2O
nNO=1,792/22,4=0,08(mol)
mCu=0,12x64=7,68(g)
=>mCuO=4(g)
%mCuO=4/11,68x100=34,25%
=>%Cu=65,75%
Đúng 0
Bình luận (0)
Cho 1,35 g hỗn hợp Cu, Mg, Al tác dụng hết với HNO3 thu được 0,01 mol NO và 0,04 mol NO2. Tính khối lượng muối tạo thành.
nHNO3 pư = 4,5 (mol)
Giải thích các bước giải:
Đặt số mol của Cu, Mg, Al lần lượt là a,b,c (mol)
quá trình nhường e
Cu ---> Cu+2 +2e
a -----> 2a (mol)
Mg ---> Mg+2 +2e
b -----> 2b (mol)
Al -----> Al+3 +3e
c -----> 3c (mol)
quá trình nhận e
N+5 +3e ---> N+2 (NO)
0,03<-- 0,01 (mol)
N+5 + 1e ---> N+4 (NO2)
0,04<--- 0,04 (mol)
Bảo toàn e ta có:
ne KIm loại nhường = n e N+5 nhận
=> 2a + 2b + 3c = 0,01 + 0,04
=> 2a + 2b + 3c = 0,05 (mol)
Có: nNO3- (trong muối) = 2nCu(NO3)2 + 2nMg(NO3)2 + 3nAl(NO3)3
= 2a + 2b + 3c
= 0,05 (mol)
BTKL có: m muối = mKL + mNO3- (trong muối)
= 1,35 + 0,05.62
= 4,45 (g)
nHNO3 pư = nNO + nNO2 + nNO3- (trong muối)
= 0,01 + 0,04 + 4,45
= 4,5 (mol)
*tk
Đúng 0
Bình luận (0)
Cu, Mg, Al + \(HNO_3\) 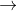 Muối nitrat + NO + \(NO_2\)
Muối nitrat + NO + \(NO_2\)
Bảo toàn điện tích: \(n_{NO_3}\)- (trong muối) = \(3n_{NO}\) + \(n_{NO_2}\) = 0,07 mol
=> Muối = \(m_{MK}\) + \(m_{NO_3}\)- = 1,35 + 0,07.62 = 5,69 g
Đúng 0
Bình luận (0)
phần sau dư rồi đâu cần tính số mol HNO3 đâu bạn
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 8,2 g hỗn hợp Al và Fe có tỉ lệ mol là 4:1 hoà tan hoàn toàn vào dung dịch HNO3 thu được 5,6 (l) khí X (đktc) là sản phẩm khử duy nhất. Xác định X
Đặt mol của Al và Fe lần lượt là 4x và x (mol)
Ta có: m hỗn hợp = 4x.27 + x.56 = 8,2 => x = 0,05 mol
=> nAl = 0,2 mol và nFe = 0,05 mol
Giả sử 1 mol khí trao đổi n mol electron.
Áp dụng định luật bảo toàn electron:
3nAl + 3nFe = n . n khí => 3.0,2 + 3.0,05 = n . 0,25 => n = 3
Vậy khí là NO
#tk
Đúng 0
Bình luận (1)
Hoà tan hoàn toàn m (g) Fe3O4 vào dung dịch HNO3 thu được hỗn hợp khí NO và N2O có tỉ khối hơi đối với H2 bằng 16,75. Tính thể tích của NO và N2O.
chac la de sai mat roi. thanks ban nhieu nha
Đúng 0
Bình luận (0)
Cho 11,8g hỗn hợp Al, Cu phản ứng với dung dịch HNO3, H2SO4 dư thu được 13,44 (l) hỗn hợp khí SO2, NO2 có tỉ khối so với H2 là 26. Tính khối lượng muối tạo ra trong dung dịch.
nk = 0,6 mol
\(\frac{d_k}{dH_2}=26=>d_k=52\)
Áp dụng sơ đồ đường chéo tính được: nSO2 = 0,2 mol ; nNO2 = 0,4 mol
Bảo toàn e:
S+6 + 2e ➝ S+4
mol: 0,4 ➝ 0,2
N+5 + 1e ➝ N+4
mol: 0,4 ➝ 0,4
mmuối = mkl + mSO42- + mNO3- = 55,8 g
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn hỗn hợp gồm 0,05 mol Ag và 0,03 mol Cu trong 200 ml dung dịch HNO3 3M vừa đủ thu được 1,12 (l) NO (đktc) và dung dịch A. Tính giá trị của M
M la khoi luong cua hon hop khi A nha ban . Minh thieu ti ![]()
Đúng 0
Bình luận (0)
Cho 19,8g kim loại M tan hoàn toàn trong HNO3 loãng dư, thu được 2,24 (l) khí (đktc) và dung dịch X. Cho KOH vào X thì có 2,24 (l) khí (đktc) làm xanh quỳ ẩm thoát ra . Xác định kim loại M.
de minh tai ve dc vay thoi chu mk cung ko biet nua
Ban thong cam cho mk nha ![]()
![]()
Đúng 0
Bình luận (0)
neu muoi nitrat tac dung voi bazo ma co the sinh ra dc khi NH3 la khi lam xanh quy am thi minh thay hoi vo li mot chut ![]()
Đúng 0
Bình luận (0)
Một hỗn hợp bột hai kim loại Mg và R được chia thành 2 phần bằng nhau:
- Phần 1: Cho tác dụng với HNO3 dư thu được 1,68 (l) khí duy nhất(đktc)
- Phần 2: Hoà tan trong 400 ml HNO3 loãng 0,7M thu được V(l) khí không màu, hoá nâu trong không khí (đktc) . Tính giá trị của V.
Phần 1: nN2O = 0,075
Phần 2 thoát khí NO, nếu kim loại tan hết thì bảo toàn electron:
3nNO = 8nN2O —> nNO = 0,2
—> nHNO3 phản ứng = 4nNO = 0,8
Trong khi đó nHNO3 = 0,28 < 0,8 —> Kim loại dư, HNO3 hết.
Vậy nNO = nHNO3/4 = 0,07
—> VNO = 1,568
#maymay#
Đúng 0
Bình luận (0)
Cho 15 g hỗn hợp Al và Mg tác dụng với dung dịch HNO3 dư. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và 4,48 (l) khí duy nhất NO ( đktc). Cô cạn dung dịch X thu được 109,8 g muối khan. Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu.
Gọi số mol Al, Mg lần lượt là a, b (mol)
Gọi số mol NH4NO3 là c (mol)
\(n_{NO}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Có: \(Al^0-3e\rightarrow Al^{+3}\)
____a----> 3a
\(Mg^0-2e\rightarrow Mg^{+2}\)
b-------> 2b
=> Số mol e nhường 3a + 2b
Có: \(NO_3^-+4H^++3e\rightarrow NO+2H_2O\)
__________________0,6 <--0,2
\(2NO_3^-+10H^++8e\rightarrow NH_4NO_3+3H_2O\)
________________ 8c <------- c
=> Số mol e nhận: 8c + 0,6
Áp dụng ĐLBT e => 3a + 2b = 8c + 0,6 (1)
Bảo toàn Al => \(n_{Al\left(NO_3\right)_3}=n_{Al}=a\left(mol\right)\)
Bảo toàn Mg => \(n_{Mg\left(NO_3\right)_2}=n_{Mg}=b\left(mol\right)\)
\(\left\{{}\begin{matrix}27a+24b=15\\213a+148b+80c=109,8\end{matrix}\right.\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,4\left(mol\right)\\c=0,1\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Mg}=0,4.24=9,6\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\frac{5,4}{15}.100\%=36\%\\\%m_{Mg}=\frac{9,6}{15}.100\%=64\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Cho m (g) hỗn hợp gồm Fe và FeO vào dung dịch H2SO4 dư thu được 2,24 (l) khí (đktc). Nếu hoà tan hỗn hợp trên vào HNO3 đặc nguội thì có 3,36 (l) khí (đktc) là sản phẩm khử duy nhất. Tính giá trị của m.










