Hãy viết công thức electron và công thức Lewis của các phân tử sau đây: NO2, N2O5, HNO3, CO2

Những câu hỏi liên quan
1. Cho các oxit có công thức hoá học sau: CO2, Mn2O7, SiO2 , P2O5, NO2, N2O5, CaO. Hãy phân loại và gọi tên các oxit trên.
2. Cho các oxit có công thức hoá học sau: SO2, Mn2O7, FeO, NO2, N2O5, BaO. Hãy phân loại và gọi tên các oxit trên.
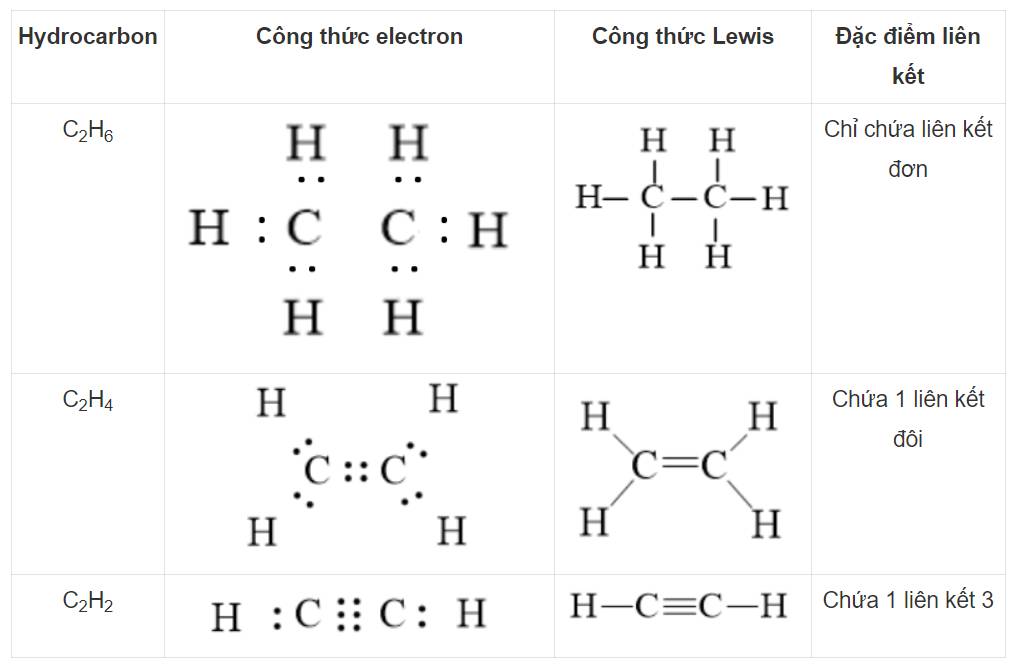
Em hãy viết công thức electron, công thức Lewis của các hydrocarbon sau: C2H6, C2H4, C2H2. Nhận xét sự khác nhau về đặc điểm liên kết trong phân tử của ba hydrocarbon trên.
Hãy biểu diễn sự hình thành các cặp electron chung cho phân tử NH3. Từ đó, viết công thức Lewis của phân tử này.
Bước 1: Viết cấu hình electron của N (Z = 7) và H (Z = 1)
N (Z = 7): 1s22s22p3
H (Z = 1): 1s1
Bước 2: Biểu diễn sự hình thành các cặp electron chung cho NH3
H có 1e ở lớp electron ngoài cùng, N có 5e ở lớp electron ngoài cùng.
⟹ Mỗi nguyên tử góp chung 1e để đạt cấu hình khí hiếm bền vững.
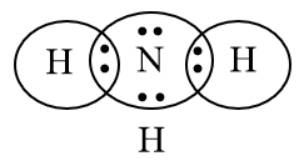
Bước 3: Công thức Lewis của NH3
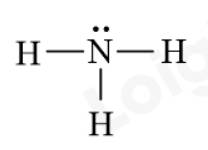
Đúng 0
Bình luận (0)
Viết công thức Lewis của CO2. Giữa nguyên tử carbon và mỗi nguyên tử oxygen có bao nhiêu cặp electron chung?
- Từ công thức electron của CO2:
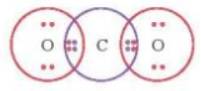
⟹ Mỗi nguyên tử O có 2 cặp electron dùng chung với nguyên tử C.
- Viết công thức Lewis của CO2: O = C = O
Đúng 0
Bình luận (0)
Viết công thức Lewis cho các phân tử H2O và CH4. Mỗi phân tử này có bao nhiêu cặp electron hóa trị riêng?
- Phân tử H2O:
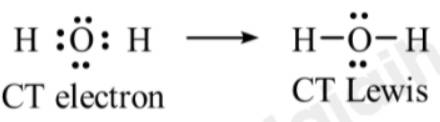
⟹ Phân tử H2O có 2 cặp electron hóa trị riêng.
- Phân tử CH4:
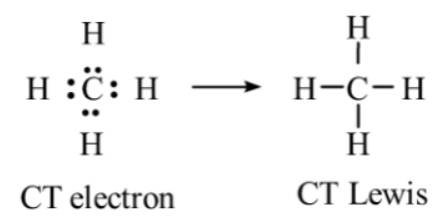
⟹ Phân tử CH4 không có cặp electron hóa trị riêng.
Đúng 0
Bình luận (0)
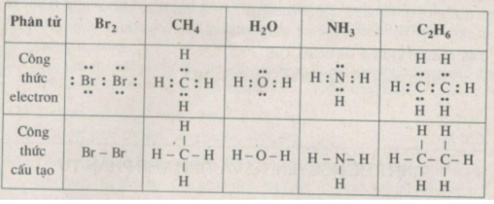
Hãy viết công thức electron và công thức cấu tạo của các phân tử sau:
Br
2
,
CH
4
,
H
2
O
,
NH
3
,
C
2
H
6
Đọc tiếp
Hãy viết công thức electron và công thức cấu tạo của các phân tử sau: Br 2 , CH 4 , H 2 O , NH 3 , C 2 H 6
hãy viết công thức electron và công thức cấu tạo của các phân tử sau: a) cl2 b) h20 c) nh3 d) ch4
Viết công thức electron công thức cấu tạo của các phân tử sau và xác định cộng hoá trị của các nguyên tố trong mỗi hợp . HCl, N2,NH3,CO2,CH4,C2H6,C2H4,C2H2
Để hình thành phân tử phosphorus trichloride (PCl3) thì mỗi nguyên tử chlorine và phosphorus đã góp chung bao nhiêu electron hóa trị? Viết công thức Lewis của phân tử.
- Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl
+ Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị
+ Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P.
=> Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon.
- Công thức Lewis của phân tử:

Đúng 0
Bình luận (0)
Miêu tả sự hình thành các liên kết ion trong các hợp chất sau : KCl và CaO . Viết công thức electron và công thức cấu tạo các hợp chất sau O2 , CO2 , HNO3
- KCl
K0-1e--> K+
Cl0+1e--> Cl-
Do 2 ion K+ và Cl- mạng điện tích trái dấu nên chúng hút nhau bởi lực hút tĩnh điện: K+ + Cl- --> KCl
- CaO
Ca0 -2e --> Ca2+
O0 +2e --> O2-
Do 2 ion Ca2+ và O2- mạng điện tích trái dấu nên chúng hút nhau bởi lực hút tĩnh điện: Ca2+ + O2- --> CaO

Đúng 0
Bình luận (1)