Cho m gam phenol vào 400 ml dung dịch NaOH 0.5M thì phản ứng vừa đủ. a/ Tính m b/Nếu cho lượng phenol trên tác dụng với dung dịch Br2 dư thì thu được x gam kết tủa. Tính x

Những câu hỏi liên quan
Hỗn hợp X gồm phenol, axit axetic và etyl axetat. Cho m gam X phản ứng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, nếu cho với kim loại K dư phản ứng với m gam X tác dụng thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là A. 4,36 gam B. 5,32 gam C. 4,98 gam D. 4,84 gam
Đọc tiếp
Hỗn hợp X gồm phenol, axit axetic và etyl axetat. Cho m gam X phản ứng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, nếu cho với kim loại K dư phản ứng với m gam X tác dụng thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là
A. 4,36 gam
B. 5,32 gam
C. 4,98 gam
D. 4,84 gam
Chọn đáp án A
nNaOH = 0,3 Þ nC6H5OH + nCH3COOH + nCH3COOC2H5 = 0,3
nH2 = 0,11 Þ nC6H5OH + nCH3COOH = 0,22 Þ nCH3COOC2H5 = 0,08 = nC2H5OH
BTKL Þ mX + 0,3x40 = mY + 0,22x18 + 0,08x46 Þ mY - mX = 4,36.
Đúng 0
Bình luận (0)
Cho Na tác dụng với dung dịch X gồm phenol và xiclohexanol trong dung môi hexan thu được 1792 ml khí H2 (đktc). Mặt khác, nếu cho nước brom lấy dư phản ứng với cùng một lượng dung dịch X như trên thì thu được 19,86 gam kết tủa trắng. Thành phần % khối lượng của xiclohexanol trong dung dịch X là A. 73,82%. B. 63,94%. C. 88,16%. D. 26,18%.
Đọc tiếp
Cho Na tác dụng với dung dịch X gồm phenol và xiclohexanol trong dung môi hexan thu được 1792 ml khí H2 (đktc). Mặt khác, nếu cho nước brom lấy dư phản ứng với cùng một lượng dung dịch X như trên thì thu được 19,86 gam kết tủa trắng. Thành phần % khối lượng của xiclohexanol trong dung dịch X là
A. 73,82%. B. 63,94%. C. 88,16%. D. 26,18%.
\(n_{C_6H_2Br_3OH}=\dfrac{19,86}{331}=0,06\left(mol\right)\)
=> \(n_{C_6H_5OH}=0,06\left(mol\right)\)
\(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
PTHH: 2C6H5OH + 2Na --> 2C6H5ONa + H2
0,06---------------------------->0,03
2C6H11OH + 2Na --> 2C6H11ONa + H2
0,1<----------------------------0,05
=> \(m_{C_6H_{11}OH}=0,1.100=10\left(g\right)\)
\(\%m_{C_6H_{11}OH}=\dfrac{10}{0,06.94+10}.100\%=63,94\%\)
=> B
Đúng 5
Bình luận (0)
Cho m gam hỗn hợp A gồm phenol (C6H5OH) và axit axetic tác dụng vừa đủ với p gam dung dịch nước brom C%, sau phản ứng thu được dung dịch B và 33,1 gam kết tủa trắng. Để trung hòa hoàn toàn B cần 144,144 ml dung dịch NaOH 10% (d 1,11 g/ml). Giá trị của m là ? A. 15,4 B. 33,4 C. 27,4 D. 24,8
Đọc tiếp
Cho m gam hỗn hợp A gồm phenol (C6H5OH) và axit axetic tác dụng vừa đủ với p gam dung dịch nước brom C%, sau phản ứng thu được dung dịch B và 33,1 gam kết tủa trắng. Để trung hòa hoàn toàn B cần 144,144 ml dung dịch NaOH 10% (d = 1,11 g/ml). Giá trị của m là ?
A. 15,4
B. 33,4
C. 27,4
D. 24,8
Đáp án : A
C6H5OH + 3Br2 -> C6H2OH(Br)3 + 3HBr
=> nkết tủa = nphenol = 0,1 mol
nNaOH = nHBr + nCH3COOH => nCH3COOH = 0,1 mol
=> m = 15,4g
Đúng 0
Bình luận (0)
Cho hỗn hợp X gồm 1 axit no, đơn chức, mạch hở và phenol. Lấy 27,4 gam X cho phản ứng 200ml dung dịch NaOH 2,5M . Để trung hoà bazơ dư cần vừa hết 0,1mol HCl . Nếu lấy 27,4 gam X cho phản ứng với dung dịch Br2 dư thì được 33,1 gam kết tủa trắng . Tìm axit : A. HCOOH B. CH3COOH C. C2H5COOH D. C2H3COOH
Đọc tiếp
Cho hỗn hợp X gồm 1 axit no, đơn chức, mạch hở và phenol. Lấy 27,4 gam X cho phản ứng 200ml dung dịch NaOH 2,5M . Để trung hoà bazơ dư cần vừa hết 0,1mol HCl . Nếu lấy 27,4 gam X cho phản ứng với dung dịch Br2 dư thì được 33,1 gam kết tủa trắng . Tìm axit :
A. HCOOH
B. CH3COOH
C. C2H5COOH
D. C2H3COOH
Đáp án B
nX = nNaOH – nHCl = 0,2.2,5 – 0,1 = 0,4 ( Vì X tác dụng với NaOH theo tỉ lệ 1:1)
Trong X chỉ có phenol + Br2 tạo kết tủa trắng
⇒ n phenol = n↓ = 33,1 : 331 = 0,1
⇒ nAxit = nX – n phenol = 0,3
Có mAxit = mX – m phenol ⇒ M Axit = (27,4 – 0,1.94) : 0,3 = 60
⇒ Axit đó là CH3COOH.
Đúng 0
Bình luận (0)
Cho m gam magie tác dụng vừa đủ với 200 ml dung dịch HCI 2M, sau phản ứng thu được dung dịch A và V lít khí ở điều kiện tiêu chuẩn. a. Tính m và V. b. Thêm 100 gam dung dịch NaOH 20% vào dung dịch A. Tính khối lượng kết tủa thu được khi phản ứng kết thúc.
Ta có: \(n_{HCl}=\dfrac{200}{1000}.2=0,4\left(mol\right)\)
\(PTHH:Mg+2HCl--->MgCl_2+H_2\uparrow\left(1\right)\)
a. Theo PT(1): \(n_{Mg}=n_{H_2}=n_{MgCl_2}=\dfrac{1}{2}.n_{HCl}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2.24=4,8\left(g\right)\\V_{H_2}=0,2.22,4=4,48\left(lít\right)\end{matrix}\right.\)
b. \(PTHH:2NaOH+MgCl_2--->Mg\left(OH\right)_2\downarrow+2NaCl\left(2\right)\)
Ta có: \(n_{NaOH}=\dfrac{\dfrac{20\%.100}{100\%}}{40}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,5}{2}>\dfrac{0,2}{1}\)
Vậy NaOH dư.
Theo PT(2): \(n_{Mg\left(OH\right)_2}=n_{MgCl_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Mg\left(OH\right)_2}=0,2.58=11,6\left(g\right)\)
Đúng 1
Bình luận (0)
a: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
200ml=0,2 lít
\(n_{HCl}=0.2\cdot22.4=4.48\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{H_2}=n_{H_2}\cdot M=2.24\cdot1=2.24\left(g\right)\)
\(n_{MgCl_2}=2.24\left(mol\right)\)
\(\Leftrightarrow n_{Mg}=2.24\left(mol\right)\)
\(\Leftrightarrow m_{Mg}=2.24\cdot24=53.76\left(g\right)\)
Đúng 0
Bình luận (1)
Có 500 ml dung dịch X chứa các ion K+; Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là A. 23,700 gam B. 14,175 gam C....
Đọc tiếp
Có 500 ml dung dịch X chứa các ion K+; Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
A. 23,700 gam
B. 14,175 gam
C. 11,850 gam
D. 10,062 gam
Đáp án C
Trong 100ml dd X có 0,1 mol Ba2+, 0,15 mol .
Trong 200ml dung dịch X có 0,2 mol Cl-.
Do đó trong 50 ml dung dịch X có 0,05 mol Ba2+, 0,075 mol , 0,05 mol Cl- và x mol K+
Theo định luật bảo toàn điện tích được x = 0,025
Khi cô cạn xảy ra quá trình:

Đúng 0
Bình luận (0)
Có 500 ml dung dịch X chứa các ion: K+, HCO3-, Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là A. 23,700 g. B. 14,17...
Đọc tiếp
Có 500 ml dung dịch X chứa các ion: K+, HCO3-, Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
A. 23,700 g.
B. 14,175 g.
C. 11,850 g.
D. 10,062 g.
Trong 100ml dung dịch X có 0,1 mol Ba2+, 0,15 mol HCO3-
Trong 200ml dung dịch X có 0,2 mol Cl-
Do đó trong 50ml dung dịch X có 0,05 mol Ba2+, 0,075 mol HCO3- , 0,05 mol Cl- và x mol K+.
Theo định luật bảo toàn điện tích được x = 0,025.
Khi cô cạn xảy ra quá trình: 2HCO3- ⟶ CO32- + CO2 + H2O
Do đó: n C O 3 2 - = 0 , 0375
Vậy khối lượng chất rắn khan thu được là: m K + + m B a 2 + + m C O 3 2 - + m C l - = 11 , 85 ( g a m )
Đáp án C
Đúng 0
Bình luận (0)
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là: A. 5,32 gam B. 4,36 gam. C. 4,98 gam. D. 4,84 gam
Đọc tiếp
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là:
A. 5,32 gam
B. 4,36 gam.
C. 4,98 gam.
D. 4,84 gam
Chọn B.
Ta có: n H 2 = 2 , 464 22 , 4 = 0 , 11 m o l
Chỉ có phenol và axit axetic mới phản ứng được với K nên:
C 6 H 5 O H C H 3 C O O H → + K 1 2 H 2
22 mol ← 0,11 mol
Khi cho X tác dụng với NaOH thì cả 3 chất đều tác dụng với NaOH theo tỉ lệ mol 1:1, nghĩa là:
n X = n N a O H = 0 , 3 m o l
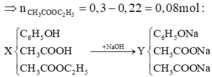
Theo sơ đồ trên ta thấy:
+ Đối với 2 chất đầu từ X đến Y chỉ thay 1 H bằng 1 Na nên khối lượng tăng: 22.0,22 gam.
+ Chất sau thay C2H5 bằng Na nên khối lượng giảm: (29 - 23).0,08 gam
=>mY - mX = 22.0,22 - (29 - 23).0,08 = 4,36 gam
Đúng 0
Bình luận (0)
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là: A. 5,32 gam. B. 4,36 gam. C. 4,98 gam. D. 4,84 gam.
Đọc tiếp
Hỗn hợp X gồm các chất: phenol, axit axetic, etyl axetat. Cho m gam X tác dụng vừa đủ với 300 ml dung dịch NaOH 1M, thu được dung dịch Y. Mặt khác, cho m gam X tác dụng với kim loại K dư thì thu được 2,464 lít khí H2 (đktc). Khối lượng muối trong Y lớn hơn khối lượng hỗn hợp X ban đầu là:
A. 5,32 gam.
B. 4,36 gam.
C. 4,98 gam.
D. 4,84 gam.
Dung dịch X gồm MgSO4 và Al2(SO4)3. Cho 400 ml dung dịch X tác dụng với dung dịch NH3 dư, thu được 65,36 gam kết tủa.Mặt khác, nếu cho 200 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, thu được 151,41 gam kết tủa. Nếu thêm m gam NaOH vào 500 ml dung dịch X, thu được 70 gam kết tủa. giá trị lớn nhất của m là A. 104. B. 128. C. 120. D. 136.
Đọc tiếp
Dung dịch X gồm MgSO4 và Al2(SO4)3. Cho 400 ml dung dịch X tác dụng với dung dịch NH3 dư, thu được 65,36 gam kết tủa.Mặt khác, nếu cho 200 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, thu được 151,41 gam kết tủa. Nếu thêm m gam NaOH vào 500 ml dung dịch X, thu được 70 gam kết tủa. giá trị lớn nhất của m là
A. 104.
B. 128.
C. 120.
D. 136.
Đáp án B
Gọi số mol MgSO4 và Al2(SO4)3 lần lượt là x và y (mol) có trong 200ml dung dịch.
+ 400 ml dd X + NH3 dư => kết tủa thu được là Mg(OH)2 : 2x ( mol) và Al(OH)3: 4y (mol)
=> ∑ mkết tủa = 58.2x + 78.4y = 65,36 (1)
+ 200 ml dd X + Ba(OH)2 dư => kết tủa thu được là Mg(OH)2 : x (mol) và BaSO4 : x + 3y (mol) ( Vì Al(OH)3 tan được trong dd Ba(OH)2 dư)
=> ∑ mkết tủa = 58x + (x + 3y).233 = 151,41 (2)
Từ (1) và (2) => x = 0,16 ; y = 0,15
+ 500 ml dd X ( có 0,4 mol Mg2+, 0,75 mol Al3+) + NaOH→ 70gam kết tủa => lượng NaOH lớn nhất ứng với trường hợp tạo Mg(OH)2↓ và Al(OH)3↓ sau đó kết tủa bị hòa tan 1 phần
=> nAl(OH)3 = (70 – 0,4.58)/78 = 0,6 (mol)
Mg2+ + 2OH → 2Mg(OH)2↓
0,4 → 0,8 (mol)
Al3+ + 3OH-→ Al(OH)3↓
0,75→2,25 → 0,75 (mol)
Al(OH)3+ OH- → AlO2- + 2H2O
(0,75-0,6) → 0,15 (mol)
∑ nOH-= 0,8 + 2,25 + 0,15 = 3,2 (mol) =nNaOH
=> mNaOH = 3,2.40 = 128 (g)
Đúng 0
Bình luận (0)












