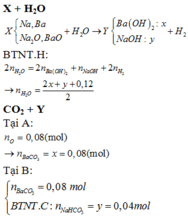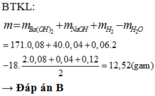Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) có được coi là nhiệt tạo thành chuẩn của Na2O(s) không? Giả sử Na tác dụng được với O3 thu được Na2O.

Những câu hỏi liên quan
2. Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) có được coi là nhiệt tạo thành chuẩn của Na2O(s) không? Giả sử Na tác dụng được với O3 thu được Na2O.
Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) không được coi là nhiệt tạo thành chuẩn của Na2O(s) vì oxygen dạng phân tử O3 (ozone) không là dạng bền nhất.
Đúng 1
Bình luận (0)
Trong ví dụ 1, ở cùng điều kiện phản ứng, nếu chỉ thu được 0,5 mol Na2O thì lượng nhiệt tỏa ra là bao nhiêu kJ?
2Na(s) + ½ O2(g) → Na2O(s) ${\Delta _f}H_{298}^0 = - 417,98$kJ.mol-1
Na(s) + ¼ O2(g) → ½ Na2O(s) ${\Delta _f}H_{298}^0 = \frac{{ - 417,98}}{2} = 208,99$kJ.mol-1
Đúng 0
Bình luận (0)
Cho 26, 8 g hỗn hợp bột X gồm Al và Fe2 O3 Tiến hành phản ứng nhiệt nhôm cho đến khi hoàn toàn hỗn hợp sau phản ứng cho tác dụng với dung dịch HCl được 12, 2 lít H2 ở điều kiện tiêu chuẩn Khối lượng của Al trong x là bao nhiêu
Giả sử Al dư sau phản ứng :
Gọi $n_{Al} = a(mol) ; n_{Fe_2O_3} = b(mol)$
$\Rightarrow 27a + 160b = 26,8(1)$
\(2Al+Fe_2O_3\xrightarrow[]{t^o}2Fe+Al_2O_3\)
2b b 2b (mol)
$n_{Al\ dư} = a - 2b(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{H_2} = (a - 2b).\dfrac{3}{2} + 2b = \dfrac{12,2}{22,4} (2)$
Từ (1)(2) suy ra a = 0,43 ; b = 0,096
$m_{Al} = 0,43.27 = 11,61(gam)$
Đúng 0
Bình luận (3)
Cho 26, 8 g hỗn hợp bột X gồm Al và Fe2 O3 Tiến hành phản ứng nhiệt nhôm cho đến khi hoàn toàn hỗn hợp sau phản ứng cho tác dụng với dung dịch HCl được 11, 2 lít H2 ở điều kiện tiêu chuẩn Khối lượng của Al trong x là bao nhiêu
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow n_{Al}=\dfrac{3}{2}n_{H_2}=\dfrac{3}{2}\cdot0,5=0,75mol\)
\(\Rightarrow m_{Al}=0,75\cdot27=20,25\left(g\right)\)
Đúng 0
Bình luận (1)
a) Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
4FeS2 (s) + 11O2 (g) → 2Fe2O3 (s) + 8SO2 (g)
Biết nhiệt tạo thành ΔrH0298 của các chất FeS2(s), Fe2O3(s) và SO2(g) lần lượt là -177,9 kJ/mol,
-825,5 kJ/mol và -296,8 kJ/mol.
\(\Delta_rH^o_{298}=2\left(-825,5\right)+8\left(-296,8\right)-4\left(-177,9\right)\\ \Delta_rH^o_{298}=-3313,8\left(kJ\right)\)
Đúng 2
Bình luận (0)
Hòa tan 21,9 gam hỗn hợp A gồm Na, Na2O, Ba, BaO vào nước dư, phản ứng hoàn toàn thu được dung dịch B chứa 20,52 gam Ba(OH)2 và có 1,12 lít khí thoát ra ở điều kiện tiêu chuẩn. Tính có khối lượng của dung dịch NaOH có trong dung dịch B.
\(n_{Ba\left(OH\right)_2}=\dfrac{20.52}{171}=0.12\left(mol\right)\)
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{NaOH}=a\left(mol\right)\)
\(n_H=0.12\cdot2+a+0.05\cdot2=0.34+a\left(mol\right)\)
\(\Rightarrow n_{H_2O}=0.17+0.5a\left(mol\right)\)
\(BTKL:\)
\(21.9+\left(0.17+0.5a\right)\cdot18=20.52+40a+0.05\cdot2\)
\(\Rightarrow a=0.14\)
\(m_{NaOH}=0.14\cdot40=5.6\left(g\right)\)
Đúng 2
Bình luận (0)
Quy đôi A gồm : Na,Ba và O
n Ba = n Ba(OH)2 = 20,52/171 = 0,12(mol)
Gọi n Na = a(mol) ; n O = b(mol)
=> 23a + 16b + 0,12.137 = 21,9(1)
n H2 = 1,12/22,4 = 0,05(mol)
Bảo toàn e :
$Na^0 \to Na^+ + 1e$
$Ba^0 \to Ba^{+2} + 2e$
$O^0 + 2e \to O^{-2}$
$2H^+ 2e \to H_2$
=> a + 0,12.2 = 2b + 0,05.2(2)
Từ (1)(2) suy ra a = b = 0,14
n NaOH = n Na = 0,14 mol
=> m NaOH = 0,14.40 = 5,6(gam)
Đúng 1
Bình luận (0)
Cho hỗn hợp gồm Na, K, Ba và
N
a
2
O
tác dụng hết với
H
2
O
, sau phản ứng thu được 0,19 mol
H
2
và dung dịch X. Hỗn hợp H gồm hai peptit mạch hở, được tạo bởi alanin và glyxin là
Z
C
x
H
y
N
z...
Đọc tiếp
Cho hỗn hợp gồm Na, K, Ba và N a 2 O tác dụng hết với H 2 O , sau phản ứng thu được 0,19 mol H 2 và dung dịch X. Hỗn hợp H gồm hai peptit mạch hở, được tạo bởi alanin và glyxin là Z C x H y N z O 8 v à T C n H m N t O 5 . Đốt cháy hết 31,33 gam hỗn hợp H cần vừa đủ 1,245 mol O 2 , sau phản ứng thu được tổng số mol H 2 O và N 2 là 1,175 mol. Mặt khác, 31,33 gam H tác dụng vừa đủ với dung dịch X. Tổng khối lượng của T và N a 2 O có giá trị là:
A. 21,52 gam
B. 23,14 gam
C. 20,22 gam
D. 17,25 gam
Cho 4,6 gam ancol X tác dụng với Na dư thu được 1,12 lít H2. Cho 9,0 gam axit hữu cơ Y tác dụng với Na dư thu được 1,68 lít H2. Đun nóng hỗn hợp gồm 4,6 gam ancol X và 9,0 gam axit hữu cơ Y (xúc tác H2SO4 đặc, t°) thu được 6,6 gam este E. Đốt cháy hoàn toàn E thu được CO2 và nước theo tỷ lệ mol là 1:1. Các thể tích khí đo ở điều kiện tiêu chuẩn, hiệu suất phản ứng tạo thành este là A. 50%. B. 60%. C. 75%. D. 80%.
Đọc tiếp
Cho 4,6 gam ancol X tác dụng với Na dư thu được 1,12 lít H2. Cho 9,0 gam axit hữu cơ Y tác dụng với Na dư thu được 1,68 lít H2. Đun nóng hỗn hợp gồm 4,6 gam ancol X và 9,0 gam axit hữu cơ Y (xúc tác H2SO4 đặc, t°) thu được 6,6 gam este E. Đốt cháy hoàn toàn E thu được CO2 và nước theo tỷ lệ mol là 1:1. Các thể tích khí đo ở điều kiện tiêu chuẩn, hiệu suất phản ứng tạo thành este là
A. 50%.
B. 60%.
C. 75%.
D. 80%.
Đáp án C
Đốt cháy hoàn toàn E thu được n H 2 O = n C O 2
=> este no, đơn chức, mạch hở
=> ancol và axit cũng no, đơn chức, mạch hở.
Xét ancol X ta có: n H 2 = 0 , 05 ( m o l )
⇒ n a n c o l = 2 n H 2 = 0 , 1 ( m o l ) ⇒ M a n c o l = 46 ⇒ a n c o l l à C 2 H 5 O H
Xét axit Y ta có: n H 2 = 0 , 075 ( m o l )
n a x i t = 2 n H 2 = 0 , 15 ( m o l ) ⇒ M Y = 60
=>axit là CH3COOH
=> este là CH3COOC2H5 => neste =0,075(mol)
Nếu H = 100% thì ancol hết => H tính theo ancol.
Vậy H = 0 , 075 0 , 1 = 75 %
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Na, Ba,
N
a
2
O
và BaO. Hoà tan hoàn toàn m gam X vào nước, thu được 1,344 lít khí
H
2
(đktc) và dung dịch Y. Khi sục từ từ khí
C
O
2
vào dung dịch Y thì mối liên hệ giữa số mol
C
O
2
phản ứng và số mol kết tủa
B
a
C
O...
Đọc tiếp
Hỗn hợp X gồm Na, Ba, N a 2 O và BaO. Hoà tan hoàn toàn m gam X vào nước, thu được 1,344 lít khí H 2 (đktc) và dung dịch Y. Khi sục từ từ khí C O 2 vào dung dịch Y thì mối liên hệ giữa số mol C O 2 phản ứng và số mol kết tủa B a C O 3 tạo thành được biểu diễn ở đồ thị dưới đây:

Giá trị của m là
A. 12,94
B. 12,52
C. 13,76
D. 13,64