Thực hiện Thí nghiệm 3 tạo iodoform. Từ phương trình hoá học, xác định vai trò của I2 và NaOH trong phản ứng tạo iodoform.


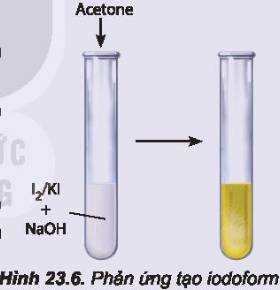
Phản ứng tạo iodoform từ acetone được tiến hành như sau:
- Cho khoảng 2 mL dung dịch I2 bão hoà trong KI vào ống nghiệm.
- Thêm khoảng 2 mL dung dịch NaOH 2 M.
- Thêm tiếp khoảng 0,5 mL acetone vào hỗn hợp trên và lắc đều ống nghiệm, quan sát thấy xuất hiện kết tủa màu vàng.
Viết phương trình hoá học của phản ứng xảy ra.
CH3 – CO – CH3 + 3 I2 + 4 NaOH → CH3COONa + 3 NaI + CHI3 + 3 H2O.
Cho các hợp chất sau: methanal, pentan – 3 – one, butanone. Hợp chất nào trong các chất ở trên tham gia được phản ứng tạo iodoform? Giải thích.
Chất tham gia được phản ứng tạo iodoform là butanone. Do butanone có nhóm methyl cạnh nhóm carbonyl.
Nêu hiện tượng, viết phương trình háo học khi tiến hành thí nghiệm rắc nhẹ bột nhôm lên ngọn lửa đèn cồn. Cho biết vai trò của nhôm trong phản ứng đó.
Hiện tượng: Bột nhôm cháy phát ra những tia sáng trắng.
Phương trình hóa học: 4 A l + 3 O 2 → 2 A l 2 O 3
Vai trò của nhôm: Al là chất khử
Cho phản ứng hoá học:
C l 2 + K O H → K C l + K C l O 3 + H 2 O
Tỉ lệ giữa số nguyên tử clo đóng vai trò chất oxi hoá và số nguyên tử clo đóng vai trò chất khử trong phương trình hoá học của phản ứng đã cho tương ứng là :
A. 1:5
B. 5:1
C. 1:3
D. 3:1
Trong phòng thí nghiệm, khí Cl2 được điều chế theo sơ đồ thí nghiệm sau:
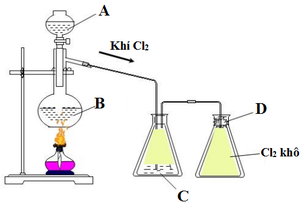
Từ sơ đồ thí nghiệm trên, hãy:
– Xác định các dung dịch A, C, D và chất rắn B.
– Cho biết vai trò của dung dịch C và bông tẩm dung dịch D.
Viết các phương trình hóa học xảy ra.
A: HCl
B: MnO2; KMnO4; KClO3
C: H2SO4 đặc
D: bông tẩm NaOH
Dung dịch C hấp thụ H2O làm khô khí Cl2.
Bông tẩm NaOH ngăn không cho khí Cl2 (độc hại) thoát ra ngoài môi trường.
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O
Nêu nhận xét về vai trò của thí nghiệm trong phương pháp thực nghiệm và xác định điểm cốt lõi của phương pháp lí thuyết.
Vai trò của phương pháp thực nghiệm: dựa vào phương pháp thực nghiệm mà có thể dự đoán được kết quả, hoàn thiện, bổ sung hay bác bỏ một giả thuyết nào đó
Điểm cốt lõi của phương pháp lí thuyết: lí thuyết được xây dựng dựa trên các quan sát ban đầu và trực giác của các nhà vật lí.
Lập phương trình hoá học và xác định tỉ lệ số phân tử của các chất trong sơ đồ phản ứng hoá học sau:
Na2CO3 + Ba(OH)2 −−→ BaCO3 + NaOH
\(Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+2NaOH\)
Tỉ lệ: Số phân tử Na2CO3 : Số phân tử Ba(OH)2 : Số phân tử BaCO3 : Số phân tử NaOH = 1:1:1:2
Áp dụng các bước lập phương trình hoá học, cân bằng phương trình.
PTHH: Na2CO3 + Ba(OH)2 → BaCO3 + 2NaOH
Tỉ lệ số phân tử chất trong phản ứng là:
Số phân tử Na2CO3 : số phân tử Ba(OH)2 : số phân tử BaCO3 : số phân tử NaOH = 1 : 1 : 1 : 2
Trộn một lượng nhỏ bột Al và I2 trong bát sứ, sau đó cho một ít nước vào.
a. Nêu hiện tượng xảy ra và giải thích
b. Viết phương trình hoá học cảu phản ứng và cho biết vai trò của các chất tham gia
c. Giải thích tại sao hợp chất COBr2 có tồn tại, còn hợp chất COI2 không tồn tại?
a, - Hiện tượng: Sau khi cho nước vào thấy có hơi màu tím thoát ra.
- Giải thích: Sau khi thêm nước, phản ứng giữa Al và I2 xảy ra, tỏa nhiệt mạnh là I2 thăng hoa.
b, PT: \(2Al+3I_2\underrightarrow{^{H_2O}}2AlI_3\)
Vai trò chất tham gia: Al là chất khử, I2 là chất oxy hóa, H2O là xúc tác.
c, - Do iot có độ âm điện nhỏ, bán kính nguyên tử lớn nên COI2 kém bền → không tồn tại.
4. Nêu nhận xét về vai trò của thí nghiệm trong phương pháp thực nghiệm và xác định điểm cốt lõi của phương pháp lí thuyết.
- Vai trò của phương pháp thực nghiệm: dựa vào phương pháp thực nghiệm mà có thể dự đoán được kết quả, hoàn thiện, bổ sung hay bác bỏ một giả thuyết nào đó
- Điểm cốt lõi của phương pháp lí thuyết: lí thuyết được xây dựng dựa trên các quan sát ban đầu và trực giác của các nhà vật lí.