Cho phương trình nhiệt hóa học sau:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l) Δr\(H^0_{298}\)= -57,3 kJ
Vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng.
Cho hai phương trình nhiệt hóa học sau:
C(s) + H2O(g) \(\underrightarrow{t^o}\) CO(g) + H2(g) Δr\(H^0_{298}\) = +131,25 kJ (1)
CuSO4(aq) + Zn(s) → ZnSO4(aq) + Cu(s) Δr\(H^0_{298}\) = -231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào thu nhiệt, phản ứng nào tỏa nhiệt?
c) Tính biến thiên enthanpy của phản ứng tạo thành ammonia (sử dụng năng lượng liên kết).
Cho biết phản ứng thu nhiệt hay toả nhiệt và vẽ sơ đồ biểu diễn biến thiên enthalpy của phản
ứng 3H2 (g) + N2 (g) → 2NH3 (g)
Liên kết Eb (kJ/ mol)
H – N 386
H – H 436
N ≡ N 945
\(\Delta_rH^{^{ }o}_{298}=3\cdot436+945-2\left(3\cdot386\right)=-63kJ\cdot mol^{-1}\)
Sơ đồ:
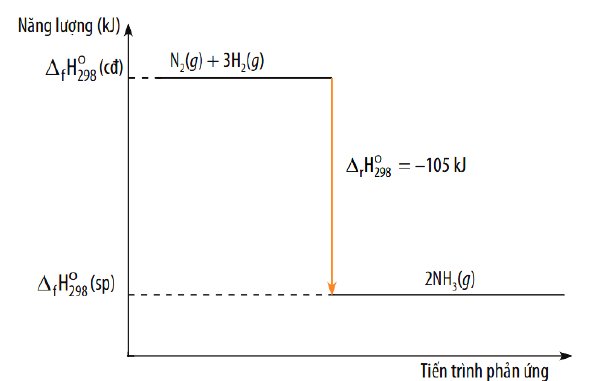
Quan sát Hình 13.5, mô tả sơ đồ biểu diễn biến thiên enthalpy của phản ứng. Nhận xét về giá trị của Δf\(H^0_{298}\)(sp) so với Δf\(H^0_{298}\) (cđ).
Trong công nghiệp, dung dịch sodium chlorine được đem điện phân để có phản ứng theo phương trình hóa học sau:
NaCl (aq) + H2O (l) → A (aq) + X (g) + Y (g) (*)
Từ phản ứng giữa Y với dung dịch A sẽ sản xuất được hỗn hợp tẩy rửa phổ biến.
Từ phản ứng kết hợp giữa X và Y sẽ sản xuất được hydrogen chlorine
a) Hãy cho biết công thức hóa học của A, X, Y
b) Hoàn thành phương trình hóa học (*)
- Chất tẩy rửa phổ biến là nước Javel gồm có NaCl và NaClO
=> Hai chất tác dụng với nhau để tạo thành nước Javel là: NaOH và Cl2
- Vì A ở dạng dung dịch, Y ở dạng khí
=> A là dung dịch NaOH, Y là khí Cl2
- Để sản xuất được hydrogen chloride cần: Cl2 và H2
- Mà Y là khí Cl2
=> X là khí H2
a) Công thức hóa học của A, X, Y lần lượt là: NaOH, H2, Cl2
b) Phương trình hóa học
2NaCl (aq) + 2H2O (l) → 2NaOH (aq) + H2 (g) + Cl2 (g) (*)
Hãy làm cho nhà em sạch bong với hỗn hợp baking soda (NaHCO3) và giấm (CH3COOH). Hỗn hợp này tạo ra một lượng lớn bọt. Phương trình nhiệt hóa học của phản ứng:
NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l) Δr\(H^0_{298}\)= 94,30 kJ
Phản ứng trên là tỏa nhiệt hay thu nhiệt? Vì sao? Tìm những ứng dụng khác của phản ứng trên

Cho biết phản ứng sau có ${\Delta _t},H_{298}^o$ > 0 và diễn ra ở ngay nhiệt độ phòng.
2NH4NO3(s) + Ba(OH)2.8H2O(s) → 2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
Khi trộn đều một lượng ammonium nitrate (NH4NO3) rắn với một lượng barium hydroxide ngậm nước (Ba(OH)2.8H2O) ở nhiệt độ phòng thì nhiệt độ của hỗn hợp sẽ tăng hay giảm? Giải thích.
Ta có: ${\Delta _t},H_{298}^o$ > 0 => Đây là phản ứng thu nhiệt
=> Phản ứng sẽ hấp thụ năng lượng dưới dạng nhiệt
=> Nhiệt độ của hỗn hợp giảm
viết phương trình hóa học của các phản ứng sau theo sơ đồ chuyển hóa : h2o →h2 → hcl → H2O → NaOH
\(2Na+2H_2O\rightarrow2NaOH+H_2\\ H_2+Cl_2\underrightarrow{^{tp}}2HCl\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ Na_2O+H_2O\rightarrow2NaOH\)

ĐỀ KIỂM TRA - HÓA HỌC 10
Câu 1: Bằng phương pháp hoá học hãy phân biệt các dung dịch không màu sau:
NaOH, HCl, NaCl, NaNO3, NaBr
Câu 2: Viết phương trình phản ứng thực hiện dãy biến hoá sau (ghi rõ điều kiện nếu có):
KMnO4 → Cl2 → NaCl → Cl2 → Br2 → I2
Câu 3: Cho 11,1 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch HCl 14,6% thu được 6,72 lít khí H2 (đktc).
a) Tính thành phần phần trăm khối lượng các kim loại trong hỗn hợp trên.
b) Tính nồng độ phần trăm các muối trong dung dịch sau phản ứng.
Câu 4: Cho a gam dung dịch HCl C% tác dụng hết với một lượng hỗn hợp 2 kim loại Na dư và K dư, thấy khối lượng H2 bay ra là 0,05a gam.Tìm C%.
Câu 3 :
\(a) n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b =1 1,1(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{6,72}{22,4} = 0,3(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,15\\ \%m_{Al} = \dfrac{0,1.27}{11,1}.100\% = 24,32\%\\ \%m_{Fe} = 100\% -24,32\% = 75,68\%\)
\(b) n_{HCl} = 2n_{H_2} = 0,3.2 = 0,6(mol)\\ \Rightarrow m_{dd\ HCl} = \dfrac{0,6.36,5}{14,6\%} = 150(gam)\\ m_{dd\ sau\ pư} = m_{hỗn\ hợp} + m_{dd\ HCl} - m_{H_2} = 11,1 + 150 - 0,3.2 = 160,5(gam)\\ n_{AlCl_3} = a = 0,1(mol)\ ;\ n_{FeCl_2} = b = 0,15(mol)\\ C\%_{AlCl_3} = \dfrac{0,1.133,5}{160,5}.100\% =8,32\%\\ C\%_{FeCl_2} = \dfrac{0,15.127}{160,5}.100\% = 11,87\%\)
Câu 2 :
\(2KMnO_4 + 16HCl \to 2MnCl_2 + 2KCl + 5Cl_2 + 8H_2O\\ Cl_2 + 2Na \xrightarrow{t^o} 2NaCl\\ 2NaCl \xrightarrow{đpnc} 2Na + Cl_2\\ Cl_2 + 2NaBr \to 2NaCl + Br_2\\ Br_2 + 2NaI \to 2NaBr + I_2\)
Câu 4 :
\(2Na + 2HCl \to 2NaCl + H_2\\ 2K + 2HCl \to 2KCl + H_2\\ 2Na + 2H_2O \to 2NaOH + H_2\\ 2K + 2H_2O \to 2KOH + H_2\\ n_{HCl} = \dfrac{a.C\%}{36,5} = \dfrac{a.C}{3650}(mol)\\ n_{H_2O} = \dfrac{a-a.C\%}{18} (mol)\)
Theo PTHH :
\(2n_{H_2} = n_{HCl} + n_{H_2O}\\ \Leftrightarrow 2.\dfrac{0,05a}{2} = \dfrac{a.C}{3650} + \dfrac{a-a.C\%}{18}\\ \Leftrightarrow 0,05 = \dfrac{C}{3650} + \dfrac{1-C\%}{18}\\ \Leftrightarrow C = 19,73\)
Vậy C% = 19,73%
Câu1:
- Trích mẫu thử
- Cho quỳ tìm vào các mẫu thử
+ mẫu thử nào làm quỳ tím hóa đỏ là HCl
+ mẫu thử nào làm quỳ tím hóa xanh là NaOH
+ các mẫu thử còn lại không hiện tượng là NaCl,NaNO3,NaBr
- Cho dd \(AgNO_3\) tới dư vào các mẫu thử còn lại :
+ mẫu thử nào tạo kết tủa trắng là NaCl
NaCl+\(AgNO_3\) →AgCl↓+ \(NaNO_3\)
+ mẫu thử nào tạo kết tủa màu vàng nhạt là NaBr
NaBr+ \(AgNO_3\) →AgBr↓+ \(NaNO_3\)
+ mẫu thử nào không có hiện tượng là \(NaNO_3\)
Câu 2:
1. \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
2. \(Cl_2+2Na\underrightarrow{t^o}2NaCl\)
3. \(2NaCl\underrightarrow{đpnc}2Na+Cl_2\)
4.\(2HBr+Cl_2\rightarrow2HCl+Br_2\)
\(2NaI_{\left(lạnh\right)}+Br_2\rightarrow2NaBr+I_2\)
Câu 1:Hoàn Thành các sơ đồ phản ứng sau
a. Fe3O4 + H --→ Fe + H2O
b. CH4 + O2 --→ CO2 + H2O
c. Na + H2O --→ NaOH + H2
d. Fe + HCL --→ FeCl2 + H2
Câu 2: Viết phương trình hóa học thực hiện dãy biến hóa sau:
SO3 → H2SO4 → H2 → H2O → NaOH
Câu 1
a) \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
b) \(CH_4+2O_2\rightarrow CO_2+2H_2O\)
c) \(2Na+2H_2O\rightarrow2NaOH+H_2\)
d) \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Câu 2
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(H_2SO_4+Fe\rightarrow FeSO_4+H_2\)
\(2H_2+O_2\rightarrow^{t^0}2H_2O\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
Câu 1:Hoàn Thành các sơ đồ phản ứng sau
a. Fe3O4 + 4H2 --→3 Fe + 4H2O
b. CH4 + 2O2 --→ CO2 + 2H2O
c.2 Na + 2H2O --→2 NaOH + H2
d. Fe + 2HCL --→ FeCl2 + H2