Đốt cháy hoàn toàn mẫu chất béo (C17H35COO)3C3H5 .Nêu hiện tượng và viết PTHH của phản ứng xảy ra .help meiii ![]()

Những câu hỏi liên quan
Cho a mol chất béo (C17H35COO)3C3H5 tác dụng với dung dịch NaOH dư. Sau khi phản ứng xảy ra hoàn toàn thu được 46 gam glixerol. Giá trị của a là:
A. 0,3 mol.
B. 0,6 mol.
C. 0,5 mol.
D. 0,4 mol.
dẫn 6,72 lít khí etilen và axetilen qua dd brom dư , phản ứng xảy ra hoàn toàn thì lượng brom phản ứng là 64 g a viết pthh sảy ra b tính % theo thể tích của mỗi chất trong hỗn hợp c đốt cháy 1/2 hỗn hợp khí trên rồi dẫn toàn bộ sản phẩm cháy qua nước vôi trong dư, sau phản ứng kết thúc thì khối lượng kết tủa thu được là
\(n_{hh}=6,72:22,4=0,3mol\\ C_2H_2+2Br_2->C_2H_2Br_4\\ C_2H_4+Br_2->C_2H_2Br_2\\ n_{Br_2}=0,4mol\\ n_{C_2H_2}=a;n_{C_2H_4}=b\\ a+b=0,3\\ 2a+b=0,4\\ a=0,2;b=0,1\\ \%V_{C_2H_2}=\dfrac{0,2}{0,3}.100\%=66,67\%\\ \%V_{C_2H_4}=33,33\%\)
1/2 hỗn hợp có 0,1 mol C2H2 và 0,05mol C2H4
\(BT.C:n_{CO_2}=2n_{C_2H_2}+2n_{C_2H_4}=0,3mol\\ n_{CaCO_3}=n_{CO_2}=0,3\\ m_{KT}=0,3.100=30g\)
Đúng 1
Bình luận (0)
Bài 1: Đốt cháy 3,68 gam CuFeS2 cần 1,68 lit khí O2(đktc)a. Viết PTHH biết sản phẩm CuO, Fe2O3 và SO2b. Nếu phản ứng xảy ra hoàn toàn, hãy tính: - Thành phần % theo thể tích các khí sau phản ứng(đktc)- Tính khối lượng chất rắn thu đcBài 2: Đốt cháy 22,8 gam hỗn hợp gồm CuS và FeS trong khí oxi dư thu đc m gam hỗn hợp CuO, Fe2O3 và 5,6 lít khí SO2(đktc)a. Viết PTHHb. Tính % theo khối lượng mỗi oxitGIÚP MÌNH 2 CÂU NÀY VỚI!!!
Đọc tiếp
Bài 1: Đốt cháy 3,68 gam CuFeS2 cần 1,68 lit khí O2(đktc)
a. Viết PTHH biết sản phẩm CuO, Fe2O3 và SO2
b. Nếu phản ứng xảy ra hoàn toàn, hãy tính:
- Thành phần % theo thể tích các khí sau phản ứng(đktc)
- Tính khối lượng chất rắn thu đc
Bài 2: Đốt cháy 22,8 gam hỗn hợp gồm CuS và FeS trong khí oxi dư thu đc m gam hỗn hợp CuO, Fe2O3 và 5,6 lít khí SO2(đktc)
a. Viết PTHH
b. Tính % theo khối lượng mỗi oxit
GIÚP MÌNH 2 CÂU NÀY VỚI!!!
Bài 1:
a) 2CuFeS2 + \(\dfrac{13}{2}\)O2 --to--> 2CuO + Fe2O3 + 4SO2
b) \(n_{CuFeS_2}=\dfrac{3,68}{184}=0,02\left(mol\right)\)
\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,02}{2}< \dfrac{0,075}{\dfrac{13}{2}}\) => CuFeS2 hết, O2 dư
PTHH: 2CuFeS2 + \(\dfrac{13}{2}\)O2 --to--> 2CuO + Fe2O3 + 4SO2
0,02----->0,065------->0,02---->0,01---->0,04
=> \(\left\{{}\begin{matrix}n_{O_2\left(dư\right)}=0,075-0,065=0,01\left(mol\right)\\n_{SO_2}=0,04\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{O_2}=\dfrac{0,01}{0,01+0,04}.100\%=20\%\\\%V_{SO_2}=\dfrac{0,04}{0,01+0,04}.100\%=80\%\end{matrix}\right.\)
- \(\left\{{}\begin{matrix}m_{CuO}=0,02.80=1,6\left(g\right)\\m_{Fe_2O_3}=0,01.160=1,6\left(g\right)\end{matrix}\right.\)
=> mrắn = 1,6 + 1,6 = 3,2 (g)
Bài 2:
a)
2CuS + 3O2 --to--> 2CuO + 2SO2
4FeS + 7O2 --to--> 2Fe2O3 + 4SO2
b) Gọi số mol CuS, FeS là a, b (mol)
=> 96a + 88b = 22,8 (1)
\(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
=> a + b = 0,25 (2)
(1)(2) => a = 0,1; b = 0,15
=> \(\left\{{}\begin{matrix}n_{CuO}=0,1\left(mol\right)\\n_{Fe_2O_3}=0,075\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,1.80}{0,1.80+0,075.160}.100\%=40\%\\\%m_{Fe_2O_3}=\dfrac{0,075.160}{0,1.80+0,075.160}.100\%=60\%\end{matrix}\right.\)
Đúng 4
Bình luận (5)
Xem thêm câu trả lời
Nêu hiện tượng và viết pthh: Muỗng sắt có chứa 2g lưu huỳnh đang cháy vào lọ chứa đầy khí oxi. Sau khi phản ứng xảy ra hoàn toàn, để nguội, cho vào 5ml nước cất, đậy nút lọ, lắc deu, cho tiếp vào lọ một mầu giấy quỳ tím.
Xem chi tiết
Lưu huỳnh cháy sáng, sinh ra khí mùi hắc :
\(S + O_2 \xrightarrow{t^o} SO_2\)
Cho nước cất vào : giấy quỳ tím chuyển dần sang màu đỏ :
\(SO_2 + H_2O \rightleftharpoons H_2SO_3\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 2,04g hợp chất A, thu được 1,08g H2O và 1,344 lít SO2 (đktc). Dẫn toàn lượng hợp chất A nói trên đi qua dung dịch axit sunfuric đặc thấy có kết tủa màu vàng xuất hiện. - Hãy giải thích tượng và viết phương trình phản ứng xảy ra. - Tính khối lượng chất kết tủa thu được
Đọc tiếp
Đốt cháy hoàn toàn 2,04g hợp chất A, thu được 1,08g H2O và 1,344 lít SO2 (đktc).
Dẫn toàn lượng hợp chất A nói trên đi qua dung dịch axit sunfuric đặc thấy có kết tủa màu vàng xuất hiện.
- Hãy giải thích tượng và viết phương trình phản ứng xảy ra.
- Tính khối lượng chất kết tủa thu được
Phương trình hóa học của phản ứng:
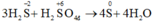
Do H2S có tính khử và H2SO4 có tính oxi hóa nên chúng có khả năng tác dụng với nhau sinh ra kết tủa vàng là S
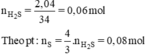
mS = 0,08 × 32 = 2,56g.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp A gồm CH4 và C2H2 tạo ra 1,344l (đktc). Mặt khác dẫn lượng A trên đi chậm qua 100ml dd brom 2M thì dung dịch mất màu hoàn toàn
a, Viết các PTHH xảy ra
b, Tính thể tích A biết các phản ứng không có chất dư
Xem chi tiết
Cho các phát biểu sau:(a) Chất béo được gọi chung là triglixerit hay triaxylglixerol. (b) Thủy phân chất béo thu được glixerol và các axit béo. (c) Phản ứng thủy phân chất béo trong môi trường axit là phản ứng thuận nghịch. (d) Tristearin, triolein có công thức lần lượt là: (C17H33COO)3C3H5, (C17H35COO)3C3H5. Số phát biểu sai là A. 3 B. 2 C. 4 D. 1
Đọc tiếp
Cho các phát biểu sau:
(a) Chất béo được gọi chung là triglixerit hay triaxylglixerol.
(b) Thủy phân chất béo thu được glixerol và các axit béo.
(c) Phản ứng thủy phân chất béo trong môi trường axit là phản ứng thuận nghịch.
(d) Tristearin, triolein có công thức lần lượt là: (C17H33COO)3C3H5, (C17H35COO)3C3H5.
Số phát biểu sai là
A. 3
B. 2
C. 4
D. 1
Phát biểu: (a); (b); (c) đúng.
(d): sai Tristearin, triolein có công thức lần lượt là: (C17H35COO)3C3H5, (C17H33COO)3C3H5.
Vậy có 1 phát biểu đúng.
Đáp án cần chọn là: D
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 2,4g magie trong bình chứa oxi a)viết pthh xảy ra b) tính thể tích khí oxi đã phản ứng ở đktc
a)2Mg+O2-----t0-->(ko có dấu gạch đứt nha bạn) 2MgO
1 1 (mol)
0,1 -> 0,05(mol)
b)nMg(Mg viết xuống dưới n dùm mình)=2,4/24=0,1 mol
=>Vo2=n.22,4=0,05.22,4=1,12 lít
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn 8,96 lít khí Axetilen (C2H2)(đktc) a) Tính thể tích khí Oxi (đktc) cần dùng ? b) Tính thể tích không khí cần dùng ? Biết rằng trong không khí, oxi chiếm 20% thể tích. c) Nêu hiện tượng và viết PTHH xảy ra khi cho Axetilen qua dung dịch Brom dư.
a, Ta có: \(n_{C_2H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PT: \(2C_2H_2+5O_2\underrightarrow{^{t^o}}4CO_2+2H_2O\)
\(n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=0,5\left(mol\right)\Rightarrow V_{O_2}=0,5.22,4=11,2\left(l\right)\)
b, \(V_{kk}=\dfrac{V_{O_2}}{20\%}=56\left(l\right)\)
c, - Hiện tượng: Br2 nhạt màu dần.
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Đúng 1
Bình luận (0)




















