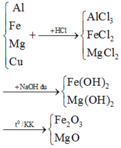
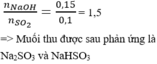BÀI 6/ Cho 56,5g hỗn hợp 3 kim loại Cu, Zn với Fe tác dụng với dung dịch axit clohidric (HCl) cho 15,68 dm3 khí H2. Và chất rắn không tan, Nung chất rắn trong không khí đến khối lượng không đổi ta thu được 16 gam(đktc)
a/ Viết phương trình hóa học của các phản ứng?
b/Tính thamh phần % theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
c/ Tính khối lượng Fe sinh ra khi cho khi cho toàn bộ khío H2 thu được ở trên t/d hoàn toàn với 46,4g Fe3O4.
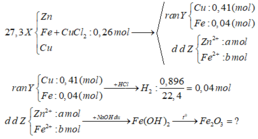
BÀI 7/ Đun khử hoàn toàn 4 gam hỗn hợp CuO và oxit sắt FexOy bằng khí CO ở nhiệt độ cao , sau phản ứng thu được 2,88 gam chất rắn ,hòa tan chất rắn này vào dung dịch HCl
( vừa đủ) thì có 0,896 lit khí thoát ra (ở đktc). Xác định công thức của oxit sắt .