Cho 1,4g một kim loại hóa trị II vào dd HCI thu được 0,56 lit H2(dktc). Kim loại đó là: A.Mg B.Zn C.Fe D.Ni

Những câu hỏi liên quan
Cho 0,5g một kim loại hóa trị II vào dung dịch HCl dư, sau phản ứng thu được 0,28 lit khí H2 (dktc). Kim loại đó là :
A. Mg
B. Sr
C. Ca
D. Ba
Giải thích: Đáp án C
Gọi kim loại hóa trị II là M
M + 2HCl -> MCl2 + H2
Mol 0,0125 <- 0,0125
=> MM = 40g => Ca
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 14,4 kim loại M hóa trị II vào dung dịch HNO3đặc dư thu được 26,88 lit NO2 (dktc) là sản phẩm khử duy nhất. Kim loại M là:
A. Zn
B. Cu
C. Fe
D. Mg
Đáp án D
(*) Phương pháp: Bảo toàn electron
-Lời giải: Bảo toàn e : 2 n M = 2 NO 2 = 1 , 2 mol ⇒ n M = 0 , 6 mol ⇒ M M = 24 g ⇒ Magie
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 14,4 kim loại M hóa trị II vào dung dịch
H
N
O
3
đặc dư thu được 26,88 lit
N
O
2
(dktc) là sản phẩm khử duy nhất. Kim loại M là A. Zn B. Cu C. Fe D. Mg
Đọc tiếp
Hòa tan hoàn toàn 14,4 kim loại M hóa trị II vào dung dịch H N O 3 đặc dư thu được 26,88 lit N O 2 (dktc) là sản phẩm khử duy nhất. Kim loại M là
A. Zn
B. Cu
C. Fe
D. Mg
Đáp án D
(*) Phương pháp: Bảo toàn electron
-Lời giải:
![]()
![]()
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 14,4g kim loại M hóa trị II vào dung dịch HNO3 đặc dư thu được 26,88 lit NO2 (dktc) là sản phẩm khử duy nhất. Kim loại M là : A. Zn B. Cu C. Fe D. Mg
Đọc tiếp
Hòa tan hoàn toàn 14,4g kim loại M hóa trị II vào dung dịch HNO3 đặc dư thu được 26,88 lit NO2 (dktc) là sản phẩm khử duy nhất. Kim loại M là :
A. Zn
B. Cu
C. Fe
D. Mg
Đáp án D
Bảo toản e : 2nM = nNO2 = 1,2 mol => nM = 0,6 mol
=> MM = 24g => Magie
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 6 gam một kim loại M hóa trị II vào dung dịch HCl, sau phản ứng thu được 3,36 lit khí H 2 (đktc). Kim loại M là:
A. Zn (65)
B. Mg (24)
C. Fe (56)
D. Ca (40)
Chọn D
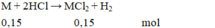
M M = 6 : 0 , 15 = 40 .
Vậy kim loại M là Ca.
Đúng 0
Bình luận (0)
hòa tan hết một gam hồn hợp gồm 2 kim loại A và B (chưa rõ hóa trị) vào dd HCI. Sau khi phản ứng kết thúc thu được m gam muối clorua và 8,96 lít H2 ( dktc )
a) Viết pthh
b) Tính a (biết a = 57,61 %m)
Câu 1: cho 20g kim loại hóa trị (II) tác dụng đủ dd HCl sau phản ứng thu được 11.2 lit khí đktc. Gọi tên kim loại
Câu 2: Cho 20.8g kim loại hóa trị (II) tác dụng đủ 800ml dd HCl 0.8M. Gọi tên kim loại
Câu 1:
Đặt kim loại hóa trị II cần tìm là A.
\(A+2HCl\rightarrow ACl_2+H_2\\ n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ n_A=n_{H_2}=\dfrac{20}{0,5}=40\left(\dfrac{g}{mol}\right)\\ \rightarrow A:Canxi\left(Ca=40\right)\)
Đúng 3
Bình luận (0)
Câu 2:
Đặt kim loại hóa trị II cần tìm là B.
\(n_{HCl}=0,8.0,8=0,64\left(mol\right)\\ B+2HCl\rightarrow BCl_2+H_2\\ n_B=\dfrac{n_{HCl}}{2}=\dfrac{0,64}{2}=0,32\left(mol\right)\\ M_B=\dfrac{20,8}{0,32}=65\left(\dfrac{g}{mol}\right)\\ \Rightarrow B\left(II\right)là:Kẽm\left(Zn=65\right)\)
Đúng 2
Bình luận (0)
2. \(A+2HCl\rightarrow ACl_2+H_2\)
\(n_{HCl}=0,8.0,8=0,64\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,32\left(mol\right)\)
=> \(M_A=\dfrac{20,8}{0,32}=65\left(Zn\right)\)
Đúng 1
Bình luận (0)
Cho 16 gam hỗn hợp kim loại Ba và kim loại kiểm R (( hóa trị I) tác dụng hết với nước được dung dịch A và 3,36 lit khi H2 ( dktc). a.Cần dùng bao nhiêu ml dung dịch HCI 0,5 M để trung hòa hết 1/10 lượng dung dịch A. b.Cô cạn 1/10 dung dịch A thu được bao nhiêu gam chất rắn khan. c.Lấy 1/ 10 dung dịch A rồi cho thêm 99 ml dung dịch Na2SO4 0,1 M thấy trong dung dịch vẫn còn hợp chất của Ba nhưng nếu thêm tiếp 2 ml dung dịch NaSO4 0,1 M vào thì thấy dư NaSO4,. Hoi R là kim loại gì.GIÚP MÌNH HỘ Ạ !!...
Đọc tiếp
Cho 16 gam hỗn hợp kim loại Ba và kim loại kiểm R (( hóa trị I) tác dụng hết với nước được dung dịch A và 3,36 lit khi H2 ( dktc). a.Cần dùng bao nhiêu ml dung dịch HCI 0,5 M để trung hòa hết 1/10 lượng dung dịch A. b.Cô cạn 1/10 dung dịch A thu được bao nhiêu gam chất rắn khan. c.Lấy 1/ 10 dung dịch A rồi cho thêm 99 ml dung dịch Na2SO4 0,1 M thấy trong dung dịch vẫn còn hợp chất của Ba nhưng nếu thêm tiếp 2 ml dung dịch NaSO4 0,1 M vào thì thấy dư NaSO4,. Hoi R là kim loại gì.
GIÚP MÌNH HỘ Ạ !!!!!!
Câu 1. Cho 2g hỗn hợp 2 kim loại Fe là kim loại hóa trị II vào dung dịch HCl dư thì thu được 1,12l khí H2(ĐKTC). Mặt khác nếu hòa tan 4,8g kim loại hóa trị II đó thì cần chưa tới 500ml dung dịch HCl 1M. Xác định kim loại hóa trị II.
Giúp MK với!!!












