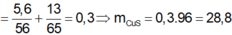Nung nóng 3,73g hỗn hợp bột kim loại kẽm và sắt trong bột lưu huỳnh dư. Chất rắng thu được sau phản ứng được hoà tan bằng dung dịch axit clohidric thấy có 1,33l khí (đktc) thoát ra. a. Viết phương trình hoá học xãy ra? b. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu? c. Túnh phần trăm khối lượng mỗi kim loại trong hỗn hợp?

Những câu hỏi liên quan
Nung nóng 3,72g hỗn hợp bột kim loại kẽm và sắt trong bột lưu huỳnh dư. Chất rắng thu được sau phản ứng được hoà tan bằng dung dịch axit clohidric thấy có 1,344l khí (đktc) thoát ra. a. Viết phương trình hoá học xãy ra? b. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu? c. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp?
a) PTHH: Fe + S --to--> FeS
Zn + S --to--> ZnS
FeS + 2HCl --> FeCl2 + H2S
ZnS + 2HCl --> ZnCl2 + H2S
Fe + 2HCl --> FeCl2 + H2
Zn + 2HCl --> ZnCl2 + H2
b)
Gọi số mol Zn, Fe là a, b (mol)
=> 65a + 56b = 3,72 (1)
Theo PTHH: \(a+b=n_{khí}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\) (2)
(1)(2) => a = 0,04 (mol); b = 0,02 (mol)
=> \(\left\{{}\begin{matrix}m_{Zn}=0,04.65=2,6\left(g\right)\\m_{Fe}=0,02.56=1,12\left(g\right)\end{matrix}\right.\)
c) \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{2,6}{3,72}.100\%=69,9\%\\\%m_{Fe}=\dfrac{1,12}{3,72}.100\%=30,1\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Gọi \(\left\{{}\begin{matrix}n_{Zn}=x\\n_{Fe}=y\end{matrix}\right.\)
\(Zn+S\rightarrow\left(t^o\right)ZnS\)
x x x ( mol )
\(Fe+S\rightarrow\left(t^o\right)FeS\)
y y y ( mol )
\(n_{H_2S}=\dfrac{1,344}{22,4}=0,06mol\)
\(ZnS+2HCl\rightarrow ZnCl_2+H_2S\)
x x ( mol )
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}97x+88y=3,72+32\left(x+y\right)\\x+y=0,06\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}97x+88y=5,64\\x+y=0,06\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,04\\y=0,02\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Zn}=0,04.65=2,6g\\m_{Fe}=0,02.56=1,12g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{2,6}{3,72}.100=69,89\%\\\%m_{Fe}=100\%-69,89\%=30,11\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra.
Viết các phương trình phản ứng xảy ra.
Theo đề bài cho, bột S dư nên Fe và Zn tác dụng hết với S.
Phương trình hóa học của phản ứng:
Zn + S → ZnS
Fe + S → FeS
ZnS + H2SO4 → ZnSO4 + H2S
FeS + H2SO4 → H2S + FeSO4
Đúng 0
Bình luận (0)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
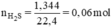
Ta có hệ phương trình: 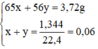
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Đúng 1
Bình luận (0)
Nung nóng 3,72 gam hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra.
a) Viết các phương trình hóa học của phản ứng xảy ra.
b) Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Theo đề bài ta có bột S dư nên Fe, Zn tác dụng hết với S.
a)Phương trình hóa học của phản ứng.
Zn + S -> ZnS Fe + S -> FeS
x mol x mol y mol y mol
ZnSO4 + H2SO4 -> ZnSO4 + H2S
x mol x mol
FeSO4 + H2SO4 -> FeSO4 + H2S
x mol y mol
Ta có hệ phương trình :
Giải hệ phương trình => x = 0,04 (mol), y = 0,02 (mol).
Vậy mZn = 0,04.65 = 2,6g
mFe = 0,02.56 = 1,12g.
Đúng 0
Bình luận (0)
Nung 5,6 gam bột sắt và 13 gam kẽm với một lượng dư bột lưu huỳnh, sau phản ứng thu được rắn X. Hòa tan hoàn toàn X trong dung dịch axit clohidric thu được khí Y. Dẫn khí Y vào V lit dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Gía trị của m là: A. 9,6 gam B. 19,2 gam C. 18,6 gam D. 28,8 gam
Đọc tiếp
Nung 5,6 gam bột sắt và 13 gam kẽm với một lượng dư bột lưu huỳnh, sau phản ứng thu được rắn X. Hòa tan hoàn toàn X trong dung dịch axit clohidric thu được khí Y. Dẫn khí Y vào V lit dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam kết tủa. Gía trị của m là:
A. 9,6 gam
B. 19,2 gam
C. 18,6 gam
D. 28,8 gam
Nung nóng m gam kim loại Zn trong bột S dư chất rắn thu được sau phản ứng được hòa tan bằng dung dịch H2SO4 loãng nhận thấy 2,24 lít khí (đktc) thoát ra
nH2S = 2.24/22.4 = 0.1 (mol)
ZnS + H2SO4 => ZnSO2 + H2S
0.1____________________0.1
Zn + S -to-> ZnS
0.1________0.1
mZn = 0.1*65 = 6.5 (g)
Đúng 2
Bình luận (0)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư, chất rắn thu được sau phản ứng hòa tan hoàn toàn bằng dung dịch H2SO4 loãng thấy có 1,344 lít khí (đktc) thoát ra.
a) Viết phương trình xảy ra
b) Xác định khối lượng mỗi kim loại
a) Zn + S ---> ZnS; Fe + S ---> FeS;
ZnS + H2SO4 ---> ZnSO4 + H2S; FeS + H2SO4 ---> FeSO4 + H2S
b) Gọi x, y là số mol Zn và Fe: 65x + 56y = 3,72 và x + y = 1,344/22,4 = 0,06
Giải hệ: x = 0,04; y = 0,02 ---> mZn = 65.0,04 = 2,6 g; mFe = 56.0,02 = 1,12 g.
Đúng 0
Bình luận (0)
a)Phương trình:
Zn+S→ZnS; Fe+S→FeS
ZnS+H2SO4→ZnSO4+H2S
FeS+H2SO4→FeSO4+H2S
b)Gọi m, m' là khối lượng Zn, Fe trong hỗn hợp ban đầu
m+m' = 3,72
nH2S=nZnS+nFeS=nZn+nFe=m/65+m'/56
=1,344/22,4=0,06
Bấm máy giải hệ phương trình:
m+m' = 3,72
(1/65).m+(1/56).m' = 0,06
ta được nghiệm: m = 2,6 ; m' = 1,12
Đúng 0
Bình luận (0)
\(Zn\left(x\right)+S\rightarrow ZnS\left(x\right)\)
\(Fe\left(y\right)+S\rightarrow FeS\left(y\right)\)
\(ZnS\left(x\right)+H_2SO_4\rightarrow H_2S\left(x\right)+ZnSO_4\)
\(FeS\left(y\right)+H_2SO_4\rightarrow H_2S\left(y\right)+FeSO_4\)
\(n_{H_2S}=\frac{1,344}{22,4}=0,06\)
Gọi số mol của Zn, Fe lần lược là x, y ta có hệ
\(\left\{\begin{matrix}65x+56y=3,72\\x+y=0,06\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=0,04\\y=0,02\end{matrix}\right.\)
\(\Rightarrow m_{Zn}=0,04.65=2,6\)
\(\Rightarrow m_{Fe}=0,02.56=1,12\)
Đúng 0
Bình luận (0)
Trộn m gam hỗn hợp hai kim loại Mg, Fe với 16 gam bột lưu huỳnh được hỗn hợp X. Nung X trong bình kín không có không khí một thời gian thu được hỗn hợp Y. Hòa tan hết Y trong dung dịch H2SO4 đặc nóng dư thấy có 44,8 lít khí SO2 (đktc) thoát ra. Dung dịch thu được cho tác dụng với dung dịch NaOH dư thấy xuất hiện kết tủa. Lọc lấy kết tủa, đem nung đến khối lượng không đổi thu được 24 gam chất rắn. Tính m và thành phần phần trăm về khối lượng từng kim loại trong hỗn hợp ban đầu.
Đọc tiếp
Trộn m gam hỗn hợp hai kim loại Mg, Fe với 16 gam bột lưu huỳnh được hỗn hợp X. Nung X trong bình kín không có không khí một thời gian thu được hỗn hợp Y. Hòa tan hết Y trong dung dịch H2SO4 đặc nóng dư thấy có 44,8 lít khí SO2 (đktc) thoát ra. Dung dịch thu được cho tác dụng với dung dịch NaOH dư thấy xuất hiện kết tủa. Lọc lấy kết tủa, đem nung đến khối lượng không đổi thu được 24 gam chất rắn. Tính m và thành phần phần trăm về khối lượng từng kim loại trong hỗn hợp ban đầu.
Gọi x,y lần lượt là số mol Mg, Fe
Mg + S ⟶ MgS
Fe + S ⟶ FeS
MgS + 4H2SO4 → MgSO4 + 4H2O + 4SO2
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
S + 2H2SO4 → 3SO2 + 2H2O
Ta có :
\(\left\{{}\begin{matrix}Mg:x\left(mol\right)\\Fe:y\left(mol\right)\end{matrix}\right.\underrightarrow{+S:0,5\left(mol\right)}\left\{{}\begin{matrix}MgS:x\left(mol\right)\\FeS:y\left(mol\right)\\S_{dư}:0,5-\left(x+y\right)\left(mol\right)\end{matrix}\right.\underrightarrow{+H_2SO_4}\left\{{}\begin{matrix}MgSO_4:x\left(mol\right)\\Fe_2\left(SO_4\right)_3:\dfrac{y}{2}\left(mol\right)\\SO_2\end{matrix}\right.\underrightarrow{+NaOH\left(dư\right)}\left(kt\right)\left\{{}\begin{matrix}Mg\left(OH\right)_2:x\left(mol\right)\\Fe\left(OH\right)_3:y\left(mol\right)\end{matrix}\right.\underrightarrow{to}\left\{{}\begin{matrix}MgO:x\left(mol\right)\\Fe_2O_3:\dfrac{y}{2}\left(mol\right)\end{matrix}\right.\)
Ta có :\(n_{SO_2}=4x+4,5y+\left[0,5-\left(x+y\right)\right].3=2\left(mol\right)\)
\(40x+160\dfrac{y}{2}=24\)
=> \(\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\)
=> \(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(m=4,8+11,2=16\left(g\right)\)
\(\%m_{Mg}=\dfrac{4,8}{16}.100=30\%\)
\(\%m_{Fe}=100-30=70\%\)
Đúng 1
Bình luận (0)
nung nóng 3,72 g hỗn hợp bột các kim loại Zn và Fe trong bột S dư , Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng , nhận thấy có 1,334 lít khi ( điều kiện tiêu chuẩn ) thoát ra : a) viết phương trình hóa học của các phản ứng đã xảy ra ; b) xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu .
a)Phương trình:
Zn+S→ZnS; Fe+S→FeS
ZnS+H2SO4→ZnSO4+H2S
FeS+H2SO4→FeSO4+H2S
b)Gọi m, m' là khối lượng Zn, Fe trong hỗn hợp ban đầu
m+m' = 3,72
nH2S=nZnS+nFeS=nZn+nFe=m/65+m'/56
=1,344/22,4=0,06
Bấm máy giải hệ phương trình:
m+m' = 3,72
(1/65).m+(1/56).m' = 0,06
ta được nghiệm: m = 2,6 ; m' = 1,12VV
Đúng 0
Bình luận (0)