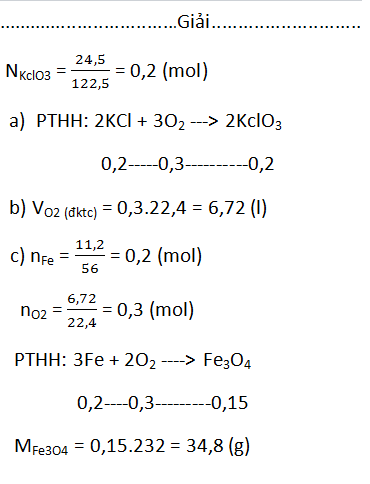thể tích khí oxi sinh ra (đktc) khi nung 0,4mol KMnO4 là

Những câu hỏi liên quan
Nung nóng 15,8g KMnO4 ở nhiệt độ cao.
a.Tính thể tích khí oxi ở đktc.
b tính khối lượng KMnO4 cần dùng để sinh ra một lượng oxi đủ để đốt cháy hết 1,68g sắt. Biết hiệu xuâtphản ứng điều chế khí oxi là 95‰
a) \(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
(mol)..........0,1................0,05..........0,05......0,05
\(V_{O_2}=0,05.22,4=1,12\left(l\right)\)
b) \(n_{Fe}=\dfrac{1.68}{56}=0,03\left(mol\right)\)
\(PTHH:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
(mol).......0,03....0,02.......0,1
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
(mol)..........0,04..............0,02............0,02....0,02
\(m_{KMnO_4}=0,04.158=6,32\left(g\right)\)
\(m_{KMnO_4\left(thựctế\right)}=6,32:95\%\approx6,65\left(g\right)\)
Đúng 1
Bình luận (0)
thể tích khí oxi sinh ra (đktc) khi nung 0,4 mol KMnO4
m.n nhanh giúp e vs ạ![]()
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(0.4..................................................0.2\)
\(V_{O_2}=0.2\cdot22.4=4.48\left(l\right)\)
Đúng 0
Bình luận (0)
\(2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,2(mol)\\ V_{O_2} = 0,2.22,4 = 4,48(lít)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Tính thể tích khí oxi ( ở đktc) đã sinh ra khi phân hủy : 24,5 g KMnO4 ( K=39;MN=55;CI=35,5;O=16)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=\dfrac{m}{M}=\dfrac{24,5}{158}=0,155mol\)
\(V_{O_2}=n.22,4=\left(\dfrac{0,155.1}{2}\right).22,4=1,73l\)
Đúng 5
Bình luận (0)
Phân hủy KClO3, KMnO4 đều là 0,2mol . tính thể tích khí oxi( ở đktc ) sinh ra trong mỗi trường hợp
Xem chi tiết
\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ \left(mol\right)..0,2\rightarrow.......0,2.......0,3\\ V_{O_2}=0,3.22,4=6,72\left(l\right)\)
\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ \left(mol\right)......0,2..\rightarrow.....0,1.........0,1........0,1\\ V_{O_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
PTHH:2KClO3to→2KCl+3O2
.0,2→.......0,2.......0,3 mol
VO2=0,3.22,4=6,72(l)
PTHH:2KMnO4→K2MnO4+MnO2+O2
......0,2..→.....0,1.........0,1........0,1 mol
VO2=0,1.22,4=2,24(l)
Đúng 1
Bình luận (0)
nung hoàn toàn 24,5g kaliclorat
a.viết PTHH
b.tính thể tích khi khí Oxi thu được (đktc)
c.đốt 11,2g sắt trong lượng khí Oxi thu được ở trên. Tính khối lượng sản phẩm sinh ra
\(n_{KClO_3}=\dfrac{24,5}{122,5}=0,2mol\)
a)\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
0,2 0,3
b)\(V_{O_2}=0,3\cdot22,4=6,72l\)
c)Bảo toàn khối lượng:
\(m_{Fe}+m_{O_2}=m_{sp}\)
\(\Rightarrow m_{sp}=11,2+0,3\cdot32=20,8g\)
Đúng 2
Bình luận (0)
Bài 10: Để điều chế khí oxi. Người ta tiến hành nhiệt phân 7,9 g kalipemanganat (thuốc tím) KMnO4 xảy ra phản ứng hóa học sau: KMnO4 ------ K2MnO4 + MnO2 + O2 .b. Tính thể tích khí oxi sinh ra ở (đktc)?c. Dùng toàn bộ lượng oxi sinh ra ở trên đem đốt cháy 2,4 g lưu huỳnh. Tính khối lượng lưu huỳnh đioxit tạo thành?
Đọc tiếp
Bài 10: Để điều chế khí oxi. Người ta tiến hành nhiệt phân 7,9 g kalipemanganat (thuốc tím) KMnO4 xảy ra phản ứng hóa học sau:
KMnO4 ------ > K2MnO4 + MnO2 + O2 ![]() .
.
b. Tính thể tích khí oxi sinh ra ở (đktc)?
c. Dùng toàn bộ lượng oxi sinh ra ở trên đem đốt cháy 2,4 g lưu huỳnh. Tính khối lượng lưu huỳnh đioxit tạo thành?
nKMnO4 = 7,9 : 158 = 0,05 (mol)
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 + O2
0,05 0,025
=> VO2 = 0,025 . 22,4 = 0,56 (L)
nS= 2,4 : 32 = 0,075 (mol)
pthh : S + O2 -t-> SO2
LTL : 0,075 > 0,025
=> S dư
theo pthh : nO2 = nSO2 = 0,025 (mol)
=> mSO2 = 0,025 . 64 = 1,6 (G)
Đúng 2
Bình luận (0)
\(n_{KMnO_4}=\dfrac{7,9}{158}=0,05\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,05 0,025
=> VO2 = 0,025.22,4 = 0,56 (l)
nS = \(\dfrac{2,4}{32}=0,075\left(mol\right)\)
PTHH: S + O2 --to--> SO2
LTL: \(0,075>0,025\rightarrow\) S dư
\(n_{SO_2}=n_{O_2}\rightarrow m_{SO_2}=0,025.64=1,6\left(g\right)\)
Đúng 3
Bình luận (0)
b,\(n_{KMnO_4}=\dfrac{7,9}{158}=0,05\left(mol\right)\)
PTHH:2KMnO4 ----to----> K2MnO4 + MnO2 + O2
Mol;: 0,05 0,025
\(V_{O_2}=0,025.22,4=0,56\left(l\right)\)
c,\(n_S=\dfrac{2,4}{32}=0,075\left(mol\right)\)
Ta có: \(\dfrac{0,075}{1}>\dfrac{0,025}{1}\) ⇒ S dư, O2 hết
PTHH: S + O2 ----to----> SO2
Mol: 0,025 0,025
\(m_{SO_2}=0,025.64=1,6\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 6 PT nhiệt phân theo sơ đồ sau: Sample picture a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 31,6 g KmnO4. b) Tính khối lượng CuO được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với Cu.
2KMnO4-to>K2MnO2+MnO2+O2
2--------------------------------------1 mol
n KMnO4= 31,6\158=2 mol
=>VO2=1.22,4=22,4l
2Cu+O2-to>2CuO
1----------2 mol
=>m CuO=2.80=160g
Đúng 0
Bình luận (0)
giúp em câu này với ạ,em đang cần gấp. Em cảm ơn.
Đốt cháy hoàn toàn 10,08 lít metan(đktc)
a/Tính thể tích khí oxi(đktc) và thể tích không khí cần dùng? Biết oxi chiếm 20% thể tích không khí
b/ tính khối lượng CO2 sinh ra?
c/ Tính khối lượng KMnO4 cần dùng để điều chế được oxi nói trên?
a. \(n_{CH_4}=\dfrac{10.08}{22,4}=0,45\left(mol\right)\)
PTHH : CH4 + 2O2 ----to---> CO2 + 2H2O
0,45 0,9 0,45
\(V_{O_2}=0,9.22,4=20,16\left(l\right)\)
\(V_{kk}=20,16.5=100,8\left(l\right)\)
b. \(m_{CO_2}=0,45.44=19,8\left(g\right)\)
c. PTHH : 2KMnO4 -> K2MnO4 + MnO2 + O2
1,8 0,9
\(m_{KMnO_4}=1,8.158=284,4\left(g\right)\)
Đúng 3
Bình luận (0)
Trog phòng thí nghiệm, để điều chế khi oxi, ngta nung nóng 73,5gam muối KClO3 ở nhiệt độ cao, thu đc muối Kali clorua (KCl) và khí Oxi
a) Viết PTPU
b) Tính k.lượng muối KCl
c) Tính thể tích khí Oxi sinh ra ở đktc
2KClO3 -- > 2KCl + O2
nKClO3 = 73,5 / 122,5 = 0,6 (mol)
mKCl = 0,6 . 74,5 = 44,7 (g)
VO2 = 0,3 . 22,4 = 6,72 (l)
Đúng 1
Bình luận (0)