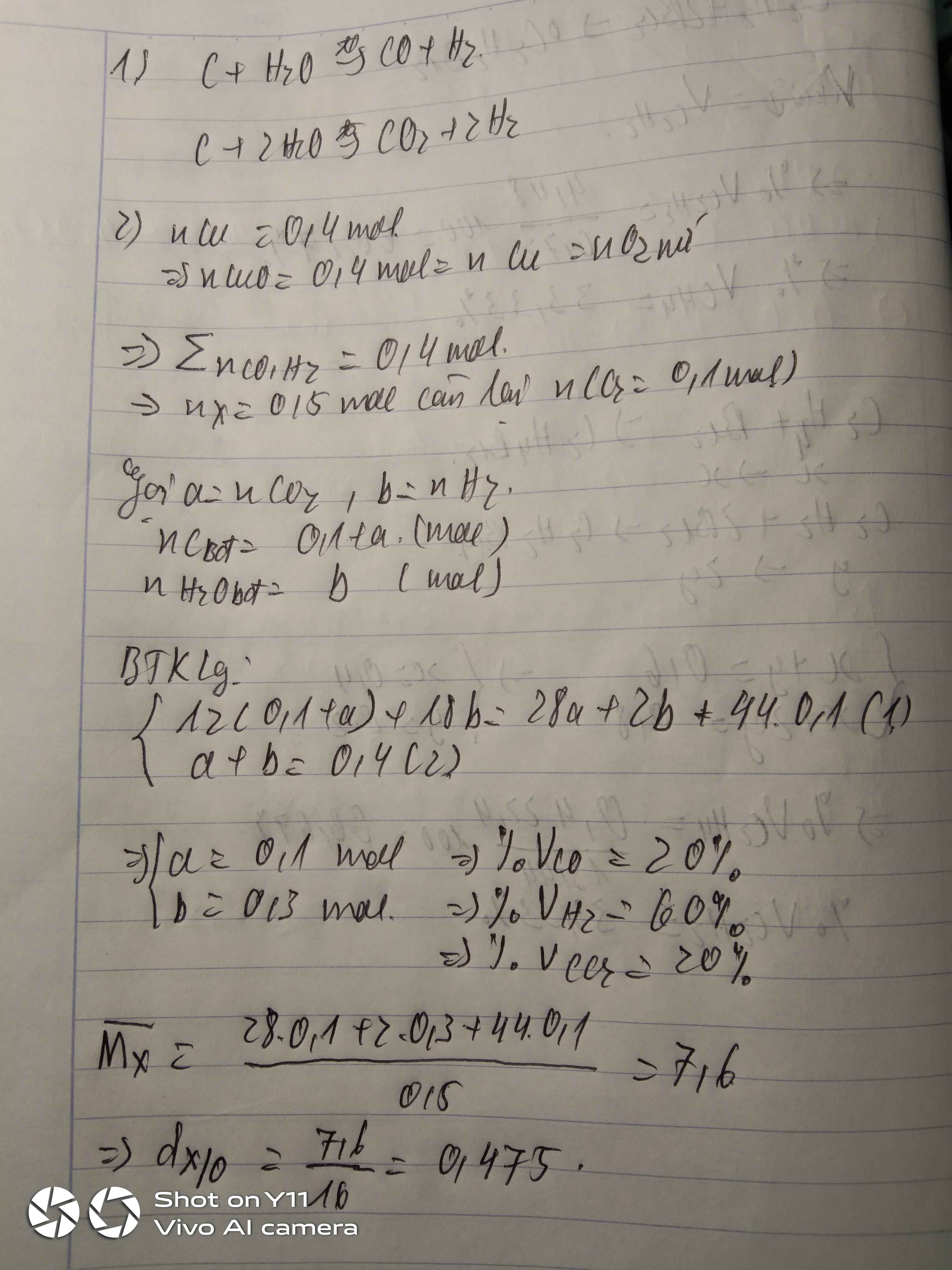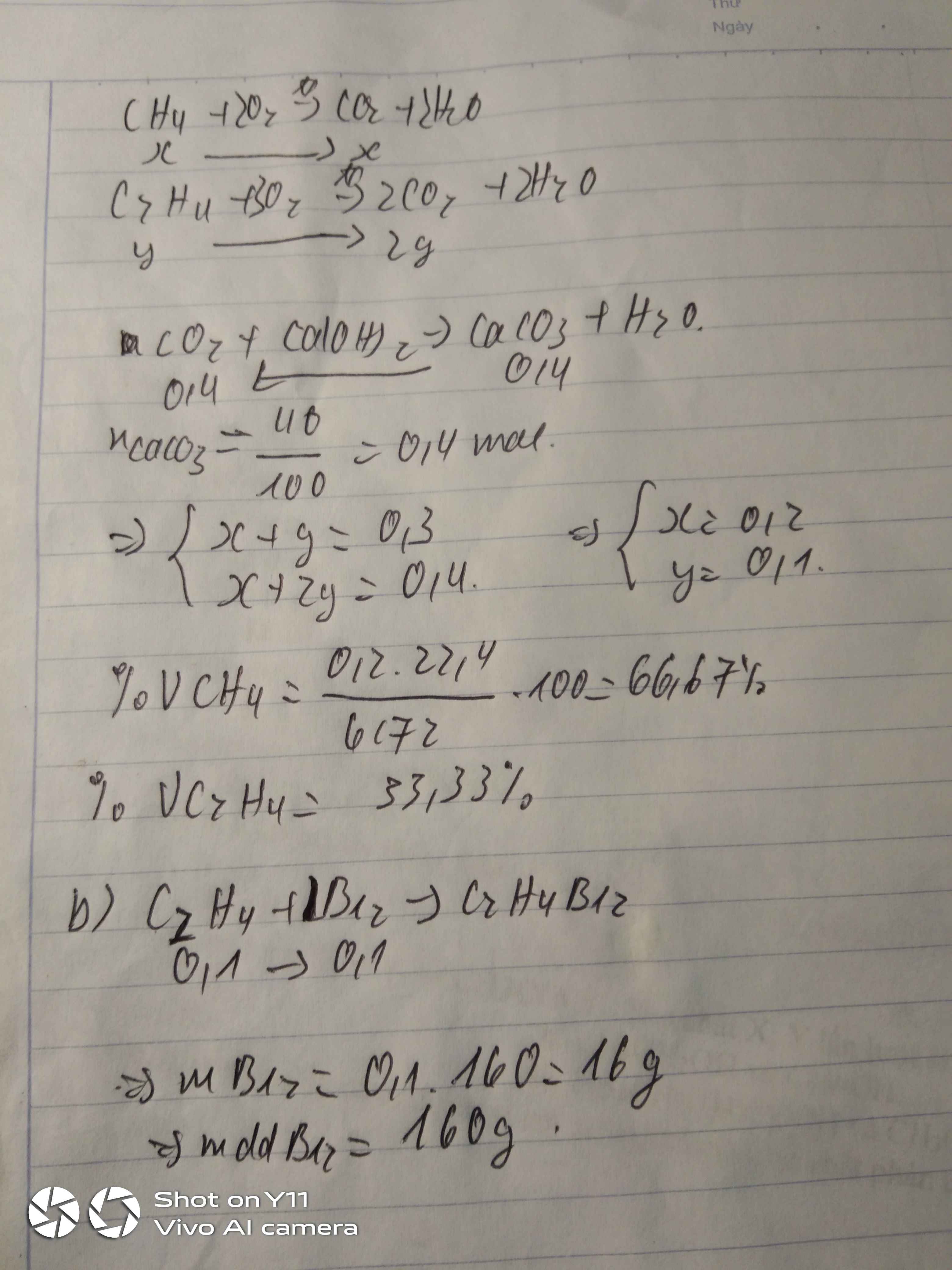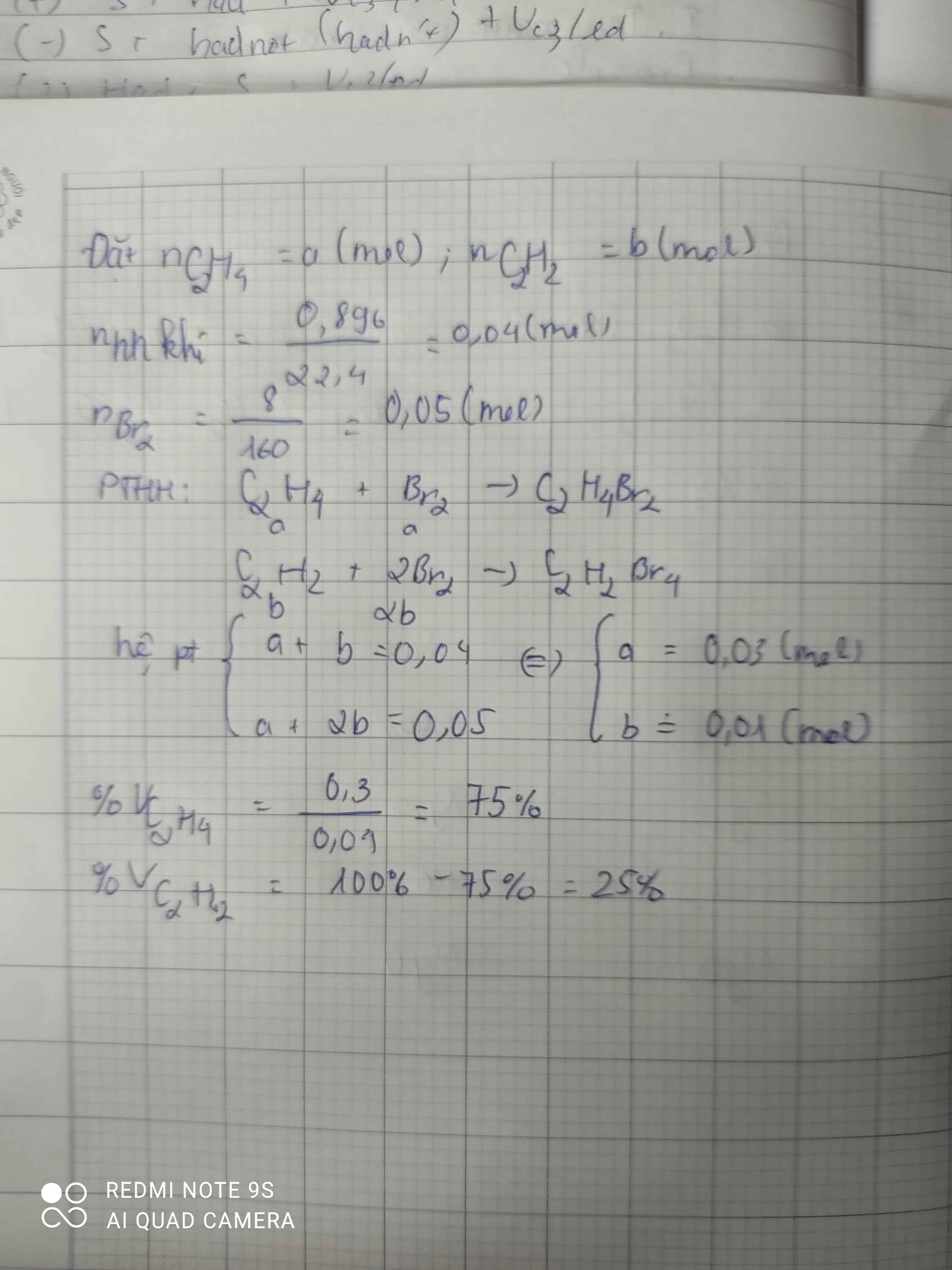Dẫn 13,44 lit khí C2H4 và C2H2 qua 800ml dd Br2 1M. Thấy Br2 mất màu hoàn toàn không có khí bay ra sau phản ứng. Tính %V mỗi khí

Những câu hỏi liên quan
4. Đốt cháy hoàn toàn 6,72 lit khí CH4 và C2H4 dẫn sản phẩm qua dd Ca(CH)2 dư sau phản ứng thu được 40g kết tủa
a. Tính %V mỗi khí
b. Dẫn 6,72 lit hỗn hợp khí trên qua Br2. Tính Kl dung dịch Br2 10% đã phản ứng?
a.\(n_{hh}=\dfrac{6,72}{22,4}=0,3mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{40}{100}=0,4mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,4 0,4 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,3\\x+2y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,3}.100=66,67\%\)
\(\%V_{C_2H_4}=100\%-66,67\%=33,33\%\)
b.\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1 0,1 ( mol )
\(m_{Br_2}=0,1.160:10\%=160g\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 3,36 lít hh ch4 và c2h4 trong không khí , cần dùng 8,96 lít oxi a. tính thể tích mỗi hh b.khối lượng mỗi khí trong hỗn hợp c. nếu dẫn toàn bộ hh khí qua dd br2 1M . Tính Thể Tích dd br2 phản ứng
a, Ta có \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,05\left(mol\right)\\n_{C_2H_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{CH_4}=0,05.22,4=1,12\left(l\right)\\V_{C_2H_4}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
b, \(m_{CH_4}=0,05.16=0,8\left(g\right)\)
c, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,1\left(mol\right)\Rightarrow V_{ddBr_2}=\dfrac{0,1}{1}=0,1\left(l\right)\)
\(m_{C_2H_4}=0,1.28=2,8\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 0,896lit hh gồm C2H4 và C2H2 phản ứng hoàn toàn với dd Br2, thấy có 8g Br2 tham gia. Tính: a/ %(V) mỗi khí trong hh các khí đo ở đkc b/ Khối lượng sản phẩm thu được
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít
Đúng 1
Bình luận (0)
a.\(n_{hh}=\dfrac{V_{hh}}{22,4}=\dfrac{0,896}{22,4}=0,04mol\)
\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{8}{160}=0,05mol\)
Gọi \(n_{C_2H_2}\) là x => \(V_{C_2H_2}=22,4x\)
\(n_{C_2H_4}\) là y => \(V_{C_2H_4}=22,4y\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
x 2x x ( mol )
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
y y y ( mol )
Ta có hpt:
\(\left\{{}\begin{matrix}22,4x+22,4y=0,896\\2x+y=0,05\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,01\\y=0,03\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{C_2H_2}=0,01.22,4=0,224\\V_{C_2H_4}=0,03.22,4=0,672\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,224}{0,896}.100=25\%\)
\(\%V_{C_2H_4}=100-25=75\%\)
b.\(m_{Sp}=0,01.186+0,03.346+0,03.188=16,02g\)
( Em cảm ơn anh Kudo Sinichi rất nhiều ạ!! )
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Dẫn 6,72 lít( đktc) hỗn hợp CH4 , C2H4, C2H2 vào dd AgNo3 trong NH3 dư sinh ra M (g) ktủa màu vàng và còn 4,48 lít (đktc) hỗn hợp khí X. Hấp thụ X vào br2 dư thấy dd bị nhạt màu và bay ra 0,56 lít ( đktc) khí Y a) viết ptpu xảy ra . Tính % thể tích mỗi khí trong hỗn hợp đầu b) tính khối lượng kết tủa màu vàng thu được
a, PT: \(C_2H_2+AgNO_3+NH_3\rightarrow Ag_2C_{2\downarrow}+NH_4NO_3\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(V_{CH_4}=V_Y=0,56\left(mol\right)\Rightarrow\%V_{CH_4}=\dfrac{0,56}{6,72}.100\%\approx8,33\%\)
\(V_{C_2H_4}=V_X-V_{CH_4}=3,92\left(l\right)\Rightarrow\%V_{C_2H_4}=\dfrac{3,92}{6,72}.100\%\approx58,34\left(\%\right)\)
\(\Rightarrow V_{C_2H_2}=6,72-4,48=2,24\left(l\right)\Rightarrow\%V_{C_2H_2}=\dfrac{2,24}{6,72}.100\%\approx33,33\%\)
c, \(n_{Ag_2C_2}=n_{C_2H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Ag_2C_2}=0,1.240=24\left(g\right)\)
Đúng 1
Bình luận (1)
Dẫn 2,24 lít (đktc) hỗn hợp A (gồm C2H4 và C2H6) vào bình đựng dung dịch Br2, thấy bình Br2 bị nhạt màu và có khí thoát ra. Sau phản ứng thấy khối lượng bình Br2 tăng 1,40 gam. Tính % thể tích từng khí trong hỗn hợp A?
nhh khí = 2,24/22,4 = 0,1 (mol)
nC2H4 = 1,4/28 = 0,05 (mol)
%VC2H4 = 0,05/0,1 = 50%
%VC2H6 = 100% - 50% = 50%
Đúng 2
Bình luận (0)
Dẫn 5,6 lít hỗn hợp khí CH4 và C2H2 (ở đktc) vào bình đựng dd brom dư. Sau phản ứng thấy có 48g Br2 đã tham gia phản ứng. Tính thể tích mỗi khí trong hỗn hợp khí ban đầu?
Ta có: \(n_{Br_2}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
____0,15___0,3 (mol)
\(\Rightarrow\left\{{}\begin{matrix}V_{C_2H_2}=0,15.22,4=3,36\left(l\right)\\V_{CH_4}=2,24\left(l\right)\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (3)
$C_2H_2+2Br_2\to Br_2CH-CHBr_2$
$n_{Br_2}=\dfrac{48}{160}=0,3(mol)$
$\Rightarrow n_{C_2H_2}=\dfrac{n_{Br_2}}{2}=0,15(mol)$
$\Rightarrow V_{C_2H_2}=0,15.22,4=3,36(l)$
$\Rightarrow V_{CH_4}=5,6-3,36=2,24(l)$
Đúng 0
Bình luận (0)
Dẫn 1,792 lít (đktc) hỗn hợp metan và axetilen đi qua bình đựng dd brom thì thấy mất màu hoàn toàn 400ml dung dịch Br2 0,2Ma/ Tính phần trăm về thể tích mỗi khí trong hỗn hợpb/ Nếu dẫn cùng lượng hỗn hợp metan và axetilen ở phản ứng trên đem đột cháy thì khối lượng khí oxi thu đc là bao nhiêu?Mọi người giúp mik với mai mik kiểm tra 1 tiết rồi !!
Đọc tiếp
Dẫn 1,792 lít (đktc) hỗn hợp metan và axetilen đi qua bình đựng dd brom thì thấy mất màu hoàn toàn 400ml dung dịch Br2 0,2M
a/ Tính phần trăm về thể tích mỗi khí trong hỗn hợp
b/ Nếu dẫn cùng lượng hỗn hợp metan và axetilen ở phản ứng trên đem đột cháy thì khối lượng khí oxi thu đc là bao nhiêu?
Mọi người giúp mik với mai mik kiểm tra 1 tiết rồi !!
Theo gt ta có: $n_{hh}=0,08(mol);n_{Br_2}=0,08(mol)$
$C_2H_2+2Br_2\rightarrow C_2H_2Br_4$
Suy ra $n_{C_2H_2}=0,04(mol)=n_{CH_4}$
a, $\Rightarrow \%V_{C_2H_2}=\%V_{C_2H_4}=50\%$
b, $CH_4+2O_2\rightarrow CO_2+2H_2O$
$2C_2H_2+5O_2\rightarrow 4CO_2+2H_2O$
Ta có: $n_{O_2}=0,04.2+0,04.5=0,28(mol)\Rightarrow m_{O_2}=8,96(g)$
Đúng 2
Bình luận (2)
\(a)C_2H_2 +2Br_2 \to C_2H_2Br_2\\ n_{C_2H_2} = \dfrac{1}{2}n_{Br_2} = \dfrac{0,4.0,2}{2} = 0,04(mol)\\ \Rightarrow V_{C_2H_2} = 0,04.22,4 = 0,896(lít)\\ \%V_{C_2H_2} =\dfrac{0,896}{1,792}.100\% = 50\%\\ \Rightarrow \%V_{CH_4} = 100\% -50\% = 50\%\\ b)\\V_{CH_4} = V_{C_2H_2} = 0,896(lít)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_2 + \dfrac{5}{2}O_2 \xrightarrow{t^o} 2CO_2 + H_2O\\ \)
\(V_{O_2} = 2V_{CH_4} + \dfrac{5}{2}V_{C_2H_2} = 4,032(lít)\\ \Rightarrow m_{O_2} = \dfrac{4,032}{22,4}.32 = 5,76(gam)\)
Đúng 2
Bình luận (1)
Hỗn hợp X gồm C2H4, C2H2, C3H8, C4H10 và H2. Lấy 6,32 gam X cho qua bình đựng dung dịch nước Br2 (dư) thấy có 0,12 mol Br2 tham gia phản ứng. Mặt khác, đốt cháy hết 2,24 lít X (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được 9,68 gam CO2. Biết các phản ứng hoàn toàn. Giá trị của V là A. 6,72 B. 8,96 C. 5,60 D. 7,84
Đọc tiếp
Hỗn hợp X gồm C2H4, C2H2, C3H8, C4H10 và H2. Lấy 6,32 gam X cho qua bình đựng dung dịch nước Br2 (dư) thấy có 0,12 mol Br2 tham gia phản ứng. Mặt khác, đốt cháy hết 2,24 lít X (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được 9,68 gam CO2. Biết các phản ứng hoàn toàn. Giá trị của V là
A. 6,72
B. 8,96
C. 5,60
D. 7,84
Hỗn hợp X gồm C2H4, C2H2, C3H8, C4H10 và H2. Lấy 6,32 gam X cho qua bình đựng dung dịch nước Br2 (dư) thấy có 0,12 mol Br2 tham gia phản ứng. Mặt khác, đốt cháy hết 2,24 lít X (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được 9,68 gam CO2. Biết các phản ứng hoàn toàn. Giá trị của V là A. 6,72. B. 8,96. C. 5,60. D. 7,84.
Đọc tiếp
Hỗn hợp X gồm C2H4, C2H2, C3H8, C4H10 và H2. Lấy 6,32 gam X cho qua bình đựng dung dịch nước Br2 (dư) thấy có 0,12 mol Br2 tham gia phản ứng. Mặt khác, đốt cháy hết 2,24 lít X (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được 9,68 gam CO2. Biết các phản ứng hoàn toàn. Giá trị của V là
A. 6,72.
B. 8,96.
C. 5,60.
D. 7,84.
Đáp án D
« Nhận xét “tinh tế”: 0,12 mol Br2 sẽ phản ứng với 0,12 mol pC=C trong X.
® Nếu thay 0,12 mol Br2 bằng 0,12 mol H2 thì sẽ thu được X gồm các hiđrocacbon no và H2.
® Thực hiện thì lúc này có 6,56 gam hỗn hợp X dạng CnH2n + 2 (trường hợp H2 ứng với n = 0).
Giả sử khối lượng 0,1 mol X gấp k lần 6,32 gam X. Thêm 0,12k mol H2 vào các nối đôi C=C trong 0,1 mol X không làm thay đổi số mol X, chỉ thay đổi số H và khối lượng X mà thôi.
« Giải đốt:
![]()
Biết luôn số mol H2O vì lúc này tương quan đốt:
![]()
Bảo toàn C, H ta có
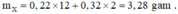
6 , 56 ÷ 3 , 28 = 2 ® tương ứng k = 0,5; nghĩa là lượng 0,12k mol H2 là 0,06 mol.
Theo đó:
![]()
Đúng 0
Bình luận (0)