neus lay cùng mọt lương KClO3 và KMnO4 đẻ điều chế khí oxi thì chất nào cho ra nhieuf khí oxi hơn, giải thích vì sao
(giúp mình với nha)Lấy cùng 1 lượng KClO3 và KMnO4 để điều chế khí oxi, chất nào cho nhiều khí oxi hơn? Viết phương trình hóa học và giải thích
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
\(\dfrac{m}{122,5}\) \(\dfrac{3m}{245}\) ( mol )
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
\(\dfrac{m}{158}\) \(\dfrac{m}{316}\) ( mol )
So sánh:
\(\dfrac{3m}{245}\) > \(\dfrac{m}{316}\)
=> \(KClO_3\) cho nhiều O2 hơn
Lấy cùng một lượng K C l O 3 và K M n O 4 để điều chế oxi. Chất nào tạo ra nhiều khí O 2 hơn. Nếu điều chế dùng một thể tích khí oxi thì dùng chất nào kinh tế hơn? Biết rằng giá K M n O 4 là 30.000 đ/kg và K C l O 3 là 96.000 đ/kg.
Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
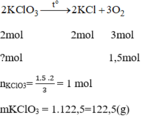
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
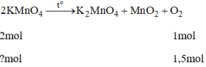
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.
Lấy cùng một lượng K C l O 3 và K M n O 4 để điều chế oxi. Chất nào tạo ra nhiều khí O 2 hơn. Viết phương trình phản ứng và giải thích.
Giả sử ta lấy cùng một khối lượng là a g
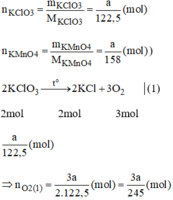
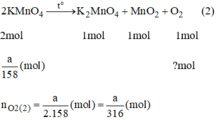
Vậy 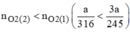 nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
Để điều chế khí oxi người ta phân hủy KMnO4 và KCLO3
a/Để thu được lượng khí oxi như nhau,chất nào cần số mol nhiều hơn?Cần dùng khối lượng nhiều hơn?
b/phân hủy cùng số mol,chất nào sinh ra khí nhiều hơn?
c/phân hủy cùng khối lượng chất nào sinh ra khí oxi nhiều hơn?
d/Biết giá thành 1kg KMnO4 là 200000đ,1kg KCLO3 là 300000đ,hãy cho biết để điều chế khí oxi như nhau,thì dùng chất nào có giá thành rẻ nhiều hơn?
a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.
trong phòng thí nghiệm ngta thường nung KClO3 hoặc KMnO4 để điều chế khí oxi sử dụng cho các thí nghiệm khác, nếu ta sử dụng cùng số mol hai chất này để điều chế khí oxi thì trường hợp nào sẽ thu được khối lượng khí oxi là nhiều nhất? giải thích.
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(\dfrac{a}{158}.............................\dfrac{a}{79}\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(\dfrac{a}{122.5}............\dfrac{3a}{245}\)
\(TC:\)
\(\dfrac{a}{79}>\dfrac{3a}{245}\)
=> Lượng Cl2 điều chế từ KMnO4 lớn nhất.
Nếu điều chế cùng một thể tích khí oxi thì dùng chất nào kinh tế hơn. Biết rằng giá KMnO4 là 30.000đ/kg và KClO3 là 96.000đ/kg.
Viết phương trình phản ứng và giải thích.

Mình không hiểu kinh tế hơn là gì ạ. Nhưng theo mình kinh tế hơn chắc là đắt hơn ![]()
Nên dùng KMnO4 "kinh tế" hơn.
Chúc bạn học tốt.
để điều chế cùng 1 thể tích khí oxi có thể nhiệt phân KMnO4 và KCLO3 . hãy cho biết khối lượng chất nào đã dùng là ít nhất . viết phương trình hóa học và giải thích ............. cần gấp
\(Coi\ n_{O_2} = 1(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 +O_2\\ n_{KMnO_4} = 2n_{O_2} = 2(mol)\\ m_{KMnO_4} = 2.158 = 316(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{KClO_3} = \dfrac{2}{3}(mol)\\ m_{KClO_3} = \dfrac{2}{3}.122,5= 81,6(gam)\\ m_{KClO_3} < m_{KMnO_4} (81,6 <316)\\ \)
trong phòng thí nghiệm người ta điều chế khí oxi bằng cách nhiệt phân kmno4 hoặc kclo3 xúc tác mno2 .nếu thu được cùng thể tích oxi thì chất nào cần khối lượng lớn hơn
\(Coi\ n_{O_2} = 1(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 2(mol) \\ m_{KMnO_4} = 2.158 =316(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{2}{3}(mol)\\ m_{KClO_3} = \dfrac{2}{3}.122,5 = 81,6(gam)\\ \Rightarrow m_{KMnO_4} > m_{KClO_3}(316<81,6)\)
KMnO4 cần khối lượng lớn hơn
Trong phòng thí nghiệm, người ta thường dùng KMnO4, KClO3 để điều chế oxi.
1. Nêu và giải thích phương pháp thu khí oxi vào lọ?
2. Khi nung nóng lần lượt a gam KMnO4 và b gam KClO3 sau phản ứng hoàn toàn thu được cùng một lượng khí oxi. Hãy tính tỉ lệ a/b?
-thu oxi có 2 loại
-Đẩy kk ; là ta lật ngửa bình để thu=>O2 nặng hơn kk
-Đẩy nước : ta có thể dời nước =>O2 ko tan trong nước , ko td vs nước
2
cùng 1 lượng oxi
2KMNO4-to>K2MnO4+MnO2+O2
2KClO3-to>2KClO3+3O2
=>\(\dfrac{a}{b}=\dfrac{2.158}{2\backslash3.122,5}=3.869\)
thu khí O2 bằng 2pp :
đẩy nước vì O2 ít tan trong nước
đẩy KK bằng cách đặt ngửa bình vì O2 nhẹ hơn KK
gọi nO2 là x
\(pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
2x x
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{3}x\) x
=> \(\left\{{}\begin{matrix}m_{KMnO_4}=2x.158=316x\\m_{KClO_3}=\dfrac{2}{3}x.122,5=81,6x\end{matrix}\right.\)
=> \(\dfrac{a}{b}=\dfrac{316x}{81,6x}=\dfrac{395}{102}\)