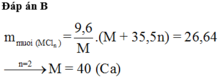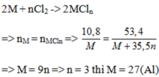Đốt cháy hết 4,8g kim loại M trong Cl2 dư được 19g muối Clorua. Kim loại M là

Những câu hỏi liên quan
Đốt cháy hoàn toàn 12,48 gam kim loại M trong khí Cl2 dư, thu được 38,04 gam muối. Kim loại M là
A. Fe
B. Mg
C. Al
D. Cr
Đốt cháy hoàn toàn m gam kim loại M trong bình chứa Cl2 dư sản phẩm sinh ra là muối clorua của kom loại M và lượng khí cl2 giảm đi 6.72 lít (đktc).cho toàn bộ muối sinh ra tác dụng với dung dịch NaOH dư thì thu đc 21.4 g kết tủa hiđro oxit của kim loại M ( là hợp chất của M và nhóm OH) tìm kim loại M
Giả sử M có hóa trị n.
PT: \(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
\(MCl_n+nNaOH\rightarrow M\left(OH\right)_{n\downarrow}+nNaCl\)
Ta có: \(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{MCl_n}=\dfrac{2}{n}n_{Cl_2}=\dfrac{0,6}{n}\left(mol\right)\)
\(n_{M\left(OH\right)_n}=\dfrac{21,4}{M_M+17n}\left(mol\right)\)
Theo PT: \(n_{MCl_n}=n_{M\left(OH\right)_n}\Rightarrow\dfrac{0,6}{n}=\dfrac{21,4}{M_M+17n}\)
\(\Rightarrow M_M=\dfrac{56}{3}n\left(g/mol\right)\)
Với n = 3 thì MM = 56 (g/mol) là tm.
Vậy: M là Fe.
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 9,6 gam kim loại M (có hóa trị không đổi) trong khí Cl2 dư, thu được 26,64 gam muối. Kim loại M là
A. K.
B. Ca.
C. Mg.
D. Al.
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị II không đổi trong hợp chất) trong khí
C
l
2
dư, thu được 28,5 gam muối. Kim loại M là A. Be B. Cu C. Ca D. Mg
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị II không đổi trong hợp chất) trong khí C l 2 dư, thu được 28,5 gam muối. Kim loại M là
A. Be
B. Cu
C. Ca
D. Mg
Chọn đáp án D
M + C l 2 → t 0 M C l 2
n M = n M C l 2 ⇒ 7 , 2 M = 28 , 5 M + 71
=> M = 24 (Mg)
Đúng 0
Bình luận (0)
Bài 9: Đốt chảy hoàn toàn m gam kim loại M trong bình chứa Cl2 dư sản phẩm sinh ra là muối clorua của kim loại M và lượng khí Cl2 giảm di 6,72 lit(dktc). Cho toàn bộ muối sinh ra tác dụng với dung dịch NaOH dư thì thu được 21,4 gam kết tủa hidroxit của kim loại M là hợp chất của M và nhóm OH) Tìm kim loại M
\(n_{Cl_2\left(pư\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2M + nCl2 --to--> 2MCln
0,3------>\(\dfrac{0,6}{n}\)
MCln + nNaOH + M(OH)n + nNaCl
\(\dfrac{0,6}{n}\)------------->\(\dfrac{0,6}{n}\)
=> \(\dfrac{0,6}{n}\left(M_M+17n\right)=21,4\)
=> \(M_M=\dfrac{56}{3}n\left(g/mol\right)\)
Xét n = 3 thỏa mãn => MM = 56 (g/mol)
=> M là Fe
Đúng 1
Bình luận (0)
Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl2 dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg
B. Al
C. Fe
D. Zn
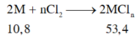
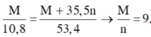
=> kim loại là Al (M=27; n=3)
Đáp án B
Đúng 0
Bình luận (0)
Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl2 dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg
B. Al
C. Fe
D. Zn
Đáp án B
Gọi n là hóa trị của M.
2M + nCl2 → 2MCln
Theo pt, nM = nmuối =>![]() => M = 9n
=> M = 9n
n = 1 => M = 9 (loại)
n = 2 => M = 18 (loại)
n = 3 => M = 27 (Al)
Đúng 0
Bình luận (0)
Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl2 dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg
B. Al
C. Fe
D. Zn
Cho 7,80 gam một kim loại M (hóa trị II không đổi) phản ứng hoàn toàn với Cl2 dư thu được 16,32 gam muối clorua. Kim loại M là A. Zn B. Ca C. Cu D. Mg
Đọc tiếp
Cho 7,80 gam một kim loại M (hóa trị II không đổi) phản ứng hoàn toàn với Cl2 dư thu được 16,32 gam muối clorua. Kim loại M là
A. Zn
B. Ca
C. Cu
D. Mg