Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách nhiệt phân kali pemanganat theo PTPƯ: KNO3 → KNO2 + O2.Tỉ lệ số phân tử của phản ứng sau cân bằng là: * 1 điểm
2,2,1
1,1,1
1,1,2
1,2,1
Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách nhiệt phân kali pemanganat theo PTPƯ: KClO3 → KCl + O2.Tỉ lệ số phân tử của phản ứng sau cân bằng là: *
2,2,3
1,1,1
1,1,2
1,2,1
2KClO3 --to--> 2KCl + 3O2
Tỉ lệ: 2:2:3
=> A
Có thể điều chế khí oxi trong phòng thí nghiệm bằng nhiều cách phân huỷ kali clorat hoặc kali pemanganat ở nhiệt độ cao giả sử lượng oxi thu được trong hai trừơng hợp là 3/1 viết pthh và tính tỷ lệ khối lượng kali clorat, kali pemangnat
Phương trình phản ứng khi phân huỷ kali clorat là:
2KClO3 → 2KCl + 3O2
Phương trình phản ứng khi phân huỷ kali pemanganat là:
2KMnO4 → K2MnO4 + MnO2 + 3O2
Theo đó, ta có thể tính tỷ lệ khối lượng giữa hai chất như sau:
Giả sử khối lượng kali clorat cần để thu được 3 mol oxi là x gram.
Theo phương trình phản ứng, 2 mol KClO3 tạo ra 3 mol O2, nên khối lượng KClO3 cần để thu được 3 mol O2 là (2/3)x gram.
Tỷ lệ khối lượng giữa KClO3 và O2 là:
(2/3)x : x = 2 : 3
Từ đó, ta có:
x = (3/2)(2/3)x
x = 1.5(2/3)x
x = 1.0x
Vậy, tỷ lệ khối lượng giữa KClO3 và O2 là 2 : 3.
Tương tự, giả sử khối lượng kali pemanganat cần để thu được 3 mol oxi là y gram.
Theo phương trình phản ứng, 2 mol KMnO4 tạo ra 3 mol O2, nên khối lượng KMnO4 cần để thu được 3 mol O2 là (2/3)y gram.
Tỷ lệ khối lượng giữa KMnO4 và O2 là:
(2/3)y : y = 2 : 3
Từ đó, ta có:
y = (3/2)(2/3)y
y = 1.5(2/3)y
y = 1.0y
Vậy, tỷ lệ khối lượng giữa KMnO4 và O2 cũng là 2 : 3.
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 theo sơ đồ phản ứng sau: Fe + O2 → Fe3O4
a) Tính số gam sắt và thể tích oxi cần dùng để có thể điều chế được 2,32 gam oxit sắt từ
b) Tính số gam Kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên( biết lượng oxi điều chế được hao hụt 10%)
a.\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1mol\)
\(3Fe+2O_2\rightarrow Fe_3O_4\)
0,3 0,2 0,1 ( mol )
\(m_{Fe}=0,3.56=16,8g\)
\(V_{O_2}=0,2.22,4=4,48l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,4 0,2 ( mol )
\(m_{KMnO_4}=\dfrac{0,4.158}{90\%}=70,22g\)
Em hãy chọn cặp từ thích hợp điền vào chỗ trống:
Em hãy tả một loài cây mà em thích nhất trong đó có sử dụng các biện pháp tu từ,so sánh đó).
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 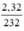 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
Trong phòng thí nghiệm, người ta điều chế oxi bằng cách đốt nóng kali clorat theo sơ đồ sau: KClO3 -> KCl + O2.
a)Tính thể tích khí oxi thu được ở điều kiện tiêu chuẩn khi nhiệt phân 0,4 mol kaliclorat ( KClO3)
b)Tính khối lượng cliclorua (KCl) thu được sau PƯ trên .
( biết K=39,Cl=35,5,O=16)
\(a.2KClO_3-^{t^o}\rightarrow2KCl+3O_2\\ n_{O_2}=\dfrac{3}{2}n_{KClO_3}=0,6\left(mol\right)\\ \Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\\ n_{KCl}=n_{KClO_3}=0,4\left(mol\right)\\ \Rightarrow m_{KCl}=0,4.74,5=29,8\left(g\right)\)
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)
Hãy chọn những từ và công thức hóa học thích hợp để điền vào chỗ trống trong câu sau:
Oxi có thể điều chế trong phòng thí nghiệm bằng phản ứng nhiệt phân ... Người ta thu khí này bằng cách đẩy ... trong ống nghiệm vì O 2 không tác dụng với ... Ống nghiệm phải đặt ở tư thế ...
K M n O 4 K C l O 3 , H 2 O , H 2 O và ít tan trong nước, úp ngược miệng ống nghiệm vào trong nước.
Trong phòng thí nghiệm, người ta thực hiện phản ứng nhiệt phân: KNO3 KNO2 + O2
a. Để thu được 6,4g O2 thì khối lượng KNO2 bị nhiệt phân là bao nhiêu? b. Đem nhiệt phân hoàn toàn 14,6 gam NO2 thì thu được bao nhiêu L khí oxygen (ở 25°C, 1 bar)? c. Cho biết hiệu suất của phản ứng trên là 85 %, thì thể tích khí oxygen (ở 25 °C, 1 bar) thực tế thu được là bao nhiêu khi nhiệt phân hoàn toàn 29,2g KNO2 trên.Trong phòng thí nghiệm ng ta điều chế oxi sắt từ Fe3O4 bằng cách dùng oxi oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và thể tích oxi cần dùng để có thể điều chế đc 2,32 (g) oxit sắt từ
b) Tính số gam kali pemanganat KMO4 cần dùng để có đc lượng oxi dùng cho phản ứng trên
a. \(n_{Fe_3O_4}=\dfrac{2.32}{232}=0,01\left(mol\right)\)
\(3Fe+2O_2\rightarrow Fe_3O_4\)
0,03 ..0,02 ...... 0,01 (mol)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe}=0,03.56=1,68\left(g\right)\\V_{O_2}=0,02.22,4=0,448\left(l\right)\end{matrix}\right.\)
\(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
0,04 ------------------------------------ 0,02 (mol)
\(\rightarrow m_{KMnO_4}=0,04.158=6,32\left(g\right)\)
a)PTHH: 3Fe+2O2__>Fe3O4
SỐ MOL OXIT SẮT TỪ:2.32/232=0.1MOL
THEO PT:
- ĐỂ TẠO RA 1 MOL Fe3O4 CẦN 2 MOL O2 VẬY ĐỂ TẠO RA 0.1 MOL Fe3O4 CẦN 0.2 MOL O2
- ĐỂ TẠO RA 1 MOL Fe3O4 CẦN 3 MOL Fe VẬY ĐỂ TẠO RA 0.1 MOL Fe3O4 CẦN 0.3 MOL Fe
=>SỐ GAM Fe CẦN: 0.3x56=16.8 g
-THỂ TÍCH KHÍ O2 CẦN: 0.2x22.4=4.48 l
b) PTHH: 2KMnO4 __>MnO2+O2+K2MnO4
Theo PT,để tạo 1 mol O2 cần 2 mol KMnO4
⇒để tạo ra 0.2 mol O2(cần dùng) thì cần 0.4 mol KMnO4
⇒ số g KMnO4 cần là:158*0.4=63.2
P/S: đúng thì nhớ tích vào đấy