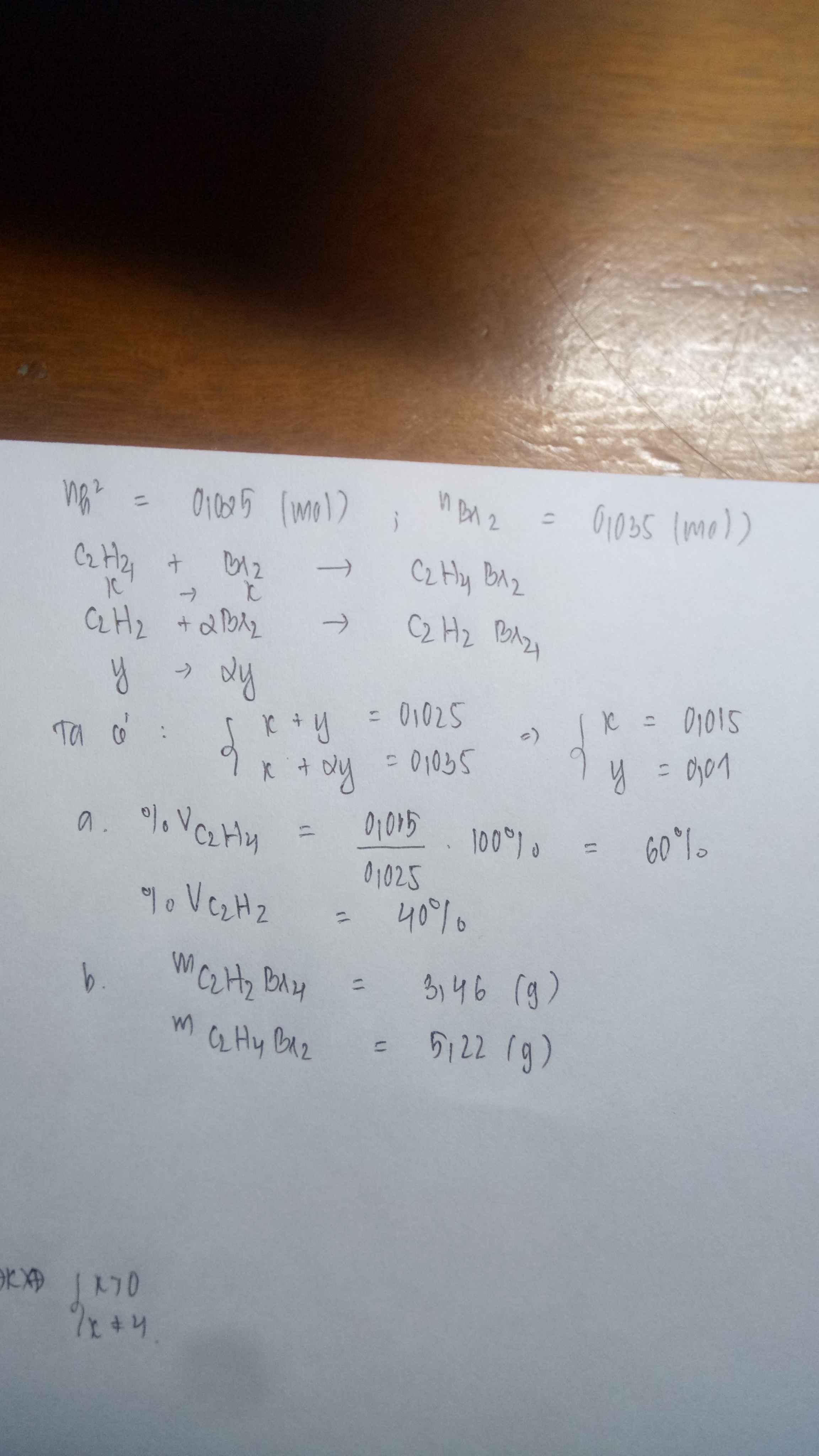Những câu hỏi liên quan
Cho hoàn toàn 0,56l hỗn hợp khí C2H2 và C2H4 đi qua dung dịch Brom biết khối lượng Brom tham gia la 5,6g.
a. Tính % thể tích mỗi khí trong hỗn hợp ban đầu.
b. Tính khối lượng khí Brom-Metan tạo thành.
\(n_{Br_2}=\dfrac{5,6}{160}=0,035mol\)
\(n_{hh}=\dfrac{0,56}{22,4}=0,025mol\)
Gọi \(\left\{{}\begin{matrix}n_{C_2H_2}=x\\n_{C_2H_4}=y\end{matrix}\right.\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
x 2x ( mol )
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,25\\2x+y=0,035\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,01\\y=0,015\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,01}{0,025}.100=40\%\)
\(\%V_{C_2H_4}=100\%-40\%=60\%\)
\(m_{C_2H_2Br_4}=0,01.346=3,46g\)
\(m_{C_2H_4Br_2}=0,015.188=2,82g\)
Đúng 4
Bình luận (0)
Số mol hỗn hợp khí và brom phản ứng lần lượt là 0,56/22,4=0,025 (mol) và 5,6/160=0,035 (mol).
a. Gọi a (mol) và b (mol) lần lượt là số mol của C2H2 và C2H4.
Ta có: a+b=0,025 (1).
BT\(\pi\): 2a+b=0,035 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,01 (mol) và b=0,015 (mol).
Phần trăm thể tích mỗi khí trong hỗn hợp ban đầu:
%V\(C_2H_2\)=0,01/0,025.100%=40%, suy ra %V\(C_2H_4\)=100%-40%=60%.
Bạn kiểm tra đề câu b giúp mình!
Có thể bạn tìm:
"Đề: Tính khối lượng tetrabrometan/1,2-đibrometan tạo thành.
Khối lượng tetrabrometan (C2H2Br4) là 0,01.346=3,46 (g).
Khối lượng 1,2-đibrometan (C2H4Br2) là 0,015.188=2,82 (g).".
Đúng 1
Bình luận (0)
Cho 0,56 lít ( đktc) hỗn hợp gồm 2 khí C2H4 và C2H2 tác dụng hết với dung dịch brom dư , khối lượng brom tham gia phản ứng là 5,6g. a. Viết PTHH? b. Tính khối lượng của C2H4 và C2H2 ? c. Tính khối lượng CaC2 cần dùng để điều chế được lượng C2H2 trên?
a, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
b, Ta có: \(n_{C_2H_4}+n_{C_2H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\) (1)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=\dfrac{5,6}{160}=0,035\left(mol\right)\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,015\left(mol\right)\\n_{C_2H_2}=0,01\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{C_2H_4}=0,015.28=0,42\left(g\right)\\m_{C_2H_2}=0,01.26=0,26\left(g\right)\end{matrix}\right.\)
c, \(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
Theo PT: \(n_{CaC_2}=n_{C_2H_2}=0,01\left(mol\right)\Rightarrow m_{CaC_2}=0,01.64=0,64\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 5,6 lít hỗn hợp gồm C2H4 và CH4 đó qua bình đựng nước brom dư thấy khối lượng bình brom nặng thêm 5,6g . Tính % thể tích mỗi khí trong hỗn hợp
Ta có: m bình Brom tăng = mC2H4 = 5,6 (g)
\(\Rightarrow n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\Rightarrow\%V_{C_2H_4}=\dfrac{0,2.22,4}{5,6}.100\%=80\%\)
\(\Rightarrow\%V_{CH_4}=100-80=20\%\)
Đúng 1
Bình luận (0)
Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là:
A. 15,66.1024
B. 15,66.1021
C. 15,66.1022
D. 15,66.1023
Đáp án D.
n Fe = 5 , 6 56 = 0 , 1 mol
0.1 mol sắt → 0.1.6,022.1023 = 6.022.1022 nguyên tử sắt
Số electron = 6.022.1022.26=1.56572.1024 e
Đúng 0
Bình luận (0)
Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là A.
15
,
66
.
10
24
B.
15
,
66
.
10
21
C.
15
,
66
.
10
22
D.
15
,...
Đọc tiếp
Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là
A. 15 , 66 . 10 24
B. 15 , 66 . 10 21
C. 15 , 66 . 10 22
D. 15 , 66 . 10 23
ĐÁP ÁN D
nFe = 0,1 mol → số nguyên tử Fe = 0,1.6,022.1023 = 6,022.1022
Số hạt p = 26. 6,022.1022 =15,66.1023.
Đúng 0
Bình luận (0)
Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là:
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(0,1\) mol sắt \(\rightarrow0,1.6,022.10^{23}=6,022.10^{22}\)nguyên tử sắt
Số electron \(=6,002.10^{22}.26=1,56572.10^{24}\) electron
Đúng 1
Bình luận (0)
tính thành phần phần trăm khối lượng C hợp chất CH4,C2H4,C2H2,C2H3OH và xác định nguyên tử C trong hợp chất nào lớn nhất
\(\%m_{C\left(CH_4\right)}=\frac{12}{12+4}.100\%=75\%\)
\(\%m_{C\left(C_2H_4\right)}=\frac{12.2}{12.2+4}.100\%\approx85,71\%\)
\(\%m_{C\left(C_2H_2\right)}=\frac{12.2}{12.2+2}.100\%\approx92,31\%\)
\(\%m_{C\left(C_2H_3OH\right)}=\frac{12.2}{12.2+4+16}.100\%\approx54,55\%\)
Vậy \(C_2H_2\) có %C lớn nhất.
11,2lit hh C2H4 và C2H6 (đkc) qua bình đựng dd Br2, phản ứng kết thúc thấy khối lượng bình Brom tăng thêm 5,6g. Tính: a/ %(V) và %(m) mỗi khí trong hh. b/ mdd Brom 8% cần phản ứng.
\(m_{Br_2}=m_{C_2H_4}=5,6g\)
\(\Rightarrow n_{C_2H_4}=\dfrac{5,6}{28}=0,2mol\)
\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
\(\Rightarrow n_{C_2H_6}=0,5-0,2=0,3mol\)
a)\(\%V_{C_2H_4}=\dfrac{0,2}{0,5}\cdot100\%=40\%\)
\(\%V_{C_2H_6}=100\%-40\%=60\%\)
b)\(m_{ddBr_2}=\dfrac{5,6}{8\%}\cdot100\%=70g\)
Đúng 3
Bình luận (0)
d/ Tính số phân tử H3PO4 và số nguyên tử của từng nguyên tố trong 0.5 mol H3PO4 e/Tính khối lượng của 7,437l SO2 ở đktc