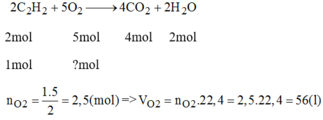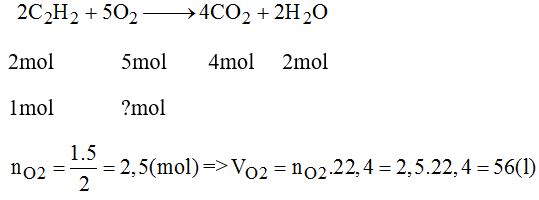Những câu hỏi liên quan
Khi đốt cháy khí axetilen 10gam C2H2 (là thành phần chính của khí đất đèn dùng để hàn cắt kim loại) với oxi ( có trong không khí) người ta thu được 13,8gam khí CO2 và 4,5 gam hơi nước H2 O.
a. Viết phương trình hóa học của phản ứng.
b. Cho biết tỉ lệ số phân tử giữa các chất trong phản ứng.
c. Tính khối lượng khí oxi tham gia phản ứng
giúp mình với ạ
\(a,PTHH:2C_2H_2+5O_2\rightarrow^{t^o}4CO_2+2H_2OO\\ b,\text{Tỉ lệ: }2:5:4:2\\ c,\text{Bảo toàn KL: }m_{C_2H_2}+m_{O_2}=m_{CO_2}+m_{H_2O}\\ \Rightarrow m_{O_2}=13,8+4,5-10=8,3\left(g\right)\)
Đúng 0
Bình luận (0)
Người ta dùng đèn xì oxi-axetilen để hàn và cắt kim loại. Phản ứng cháy axetilen C 2 H 2 trong oxi tạo thành khí cacbonic và hơi nước. Hãy tính thể tích khí oxi (đktc) cần thiết để đốt cháy 1 mol khí axetilen.
Người ta dùng đèn xì oxi - axetilen để hàn cắt kim loại. Phản ứng cháy của axentilen C2H2 trong oxi tại thành khí cacbonic và hơi nước. Hãy tính thể tích oxi (đktc) cần thiết để đốt cháy hoàn toàn 44,8 lít C2H2 (đktc)
\(n_{C_2H_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
PT: \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=5\left(mol\right)\)
\(\Rightarrow V_{O_2}=5.22,4=112\left(l\right)\)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn 1,00 gam khí C2H2 thu được CO2(k) và H2O(l) giải phóng 50,01 kJ. Tính biến thiên enthalpy của phản ứng đốt cháy 1 mol khí C2H2, từ đó cho biết vì sao C2H2 được sử dụng trong đèn xì hàn cắt kim loại mà không dùng mêtan.
\(\Delta_rH=-\dfrac{50,01kJ}{\dfrac{1}{26}mol}=-1300,26kJ\cdot mol^{-1}\)
Mặt khác, khi đốt 1 mol methane chỉ toả ra lượng nhiệt khoảng 890,2 kJ, thấp hơn nhiều so với acetylene nên acetylene được dùng trong đèn xì.
Đúng 1
Bình luận (0)
Dạng 1: Viết phương trình hóa họcBài 1: Viết PTPƯ cháy của các chất sau trong oxi: H2; Mg; Cu; S; Al; C và P. Bài 2: Khi đốt khí metan (CH4); khí axetilen (C2H2), rượu etylic (C2H6O) đều cho sản phẩm là khí cacbonic và hơi nước. Hãy viết PTHH phản ứng cháy của các phản ứng trên.
Đọc tiếp
Dạng 1: Viết phương trình hóa học
Bài 1: Viết PTPƯ cháy của các chất sau trong oxi: H2; Mg; Cu; S; Al; C và P.
Bài 2: Khi đốt khí metan (CH4); khí axetilen (C2H2), rượu etylic (C2H6O) đều cho sản phẩm là khí cacbonic và hơi nước. Hãy viết PTHH phản ứng cháy của các phản ứng trên.
Bài 1
H2+ 1/2O2 --> H2O
Mg + 1/2O2 --> MgO
Cu+ 1/2O2-->CuO
S+O2 -->SO2
4Al+ 3O2-->2Al2O3
C+ O2--> CO2
2P+5/2O2--> P2O5
Bài 2
CH4+2O2->CO2+2H2O
2C2H2+5O2->4CO2+2H2O
C2H6O+3O2->2CO2+3H2O
Đúng 2
Bình luận (0)
Axetilen là chất khí, khi cháy tỏa nhiều nhiệt nên được dùng trong đèn xì oxi - axetilen để hàn, cắt kim loại. Công thức phân tử của axetilen là A. C2H6. B. C2H2. C. C6H6. D. C2H4.
Đọc tiếp
Axetilen là chất khí, khi cháy tỏa nhiều nhiệt nên được dùng trong đèn xì oxi - axetilen để hàn, cắt kim loại. Công thức phân tử của axetilen là
A. C2H6.
B. C2H2.
C. C6H6.
D. C2H4.
Axetilen là một chất khí, khi cháy tỏa nhiều nhiệt nên được dùng trong đèn xì oxi - axetilen để hàn, cắt kim loại. Công thức phân tử của axetilen là A. C2H4 B. C6H6 C. C2H2 D. C2H6
Đọc tiếp
Axetilen là một chất khí, khi cháy tỏa nhiều nhiệt nên được dùng trong đèn xì oxi - axetilen để hàn, cắt kim loại. Công thức phân tử của axetilen là
A. C2H4
B. C6H6
C. C2H2
D. C2H6
giúp mik bài này nha
Câu 1: Đốt cháy 2,4 gam kim loại magnesium Mg trong không khí thu được 4g hợp chất magnesium oxide MgO. Biết rằng, magnesium cháy là xảy ra phản ứng với khí oxygen O2 trong không khí.
a. Lập PTHH của phản ứng trên.
b. Viết công thức về khối lượng và tính khối lượng của khí oxygen.
a) 2Mg + O2 --to--> 2MgO
b) Theo ĐLBTKL: mMg + mO2 = mMgO
=> mO2 = 4 - 2,4 = 1,6 (g)
Đúng 2
Bình luận (0)
a, PTHH: 2Mg + O2 \(\rightarrow\) 2MgO
b, Theo ĐLBTKL, ta có:
mMg + m\(O_2\) = mMgO
\(\Rightarrow m_{O_2}=4-2,4=1,6g\)
Đúng 1
Bình luận (0)
Đốt cháy hết 10,5 gam kim loại kẽm trong không khí thu được 20 gam hợp chất kẽm oxit(ZnO). biết rằng kẽm cháy là xảy ra phản ứng với khi oxy trong không khi
a)Viết pthh và công thức về khối lượng của phản ứng trên
b)tính khôi lượng khí oxi đã phản ứng
\(2Zn+O_2\underrightarrow{^{^{t^0}}}2ZnO\)
Bảo toàn khối lượng :
\(m_{Zn}+m_{O_2}=m_{ZnO}\)
\(\Rightarrow m_{O_2}=m_{ZnO}-m_{Zn}=20-10.5=9.5\left(g\right)\)
Đúng 1
Bình luận (0)