Đốt nóng hidro trong khí oxi người ta nhận thấy cứ 2 thể tích khí hidro kêt hợp với 1 thể tích oxi tạo thành nước. Hãy tìm công thức hóa học đơn giản của nước.

Những câu hỏi liên quan
Đốt nóng hidro trong khí oxi người ta nhận thấy cứ 2 thể tích khí hidro kêt hợp với 1 thể tích oxi tạo thành nước. Viết phương trình hóa học xảy ra khi đốt nóng hidro và oxi.
Đốt nóng hidro trong khí oxi người ta nhận thấy cứ 2 thể tích khí hidro kêt hợp với 1 thể tích oxi tạo thành nước. Sau phản ứng, người ta thu được 1,8g nước.Hãy tìm thể tích các khí hidro và oxi tham gia phản ứng ở đktc.
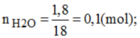
Theo phương trình hóa học: n H 2 = n H 2 O = 0,1(mol)
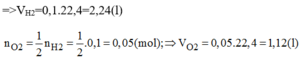
Đúng 0
Bình luận (0)
1/ Đốt khí hiđro trong khí oxi người ta nhận thấy cứ 2 thể tích hidro kết hợp với 1 thể tích oxi tạo thành nước
a/Hãy tìm công thức hóa học đơn giản ( Ai giải bằng cách x/y được mình tick cho )
Câu hỏi : Cho 5,6 lít nước hidro tác dụng với 3,2g khíc Oxi tạo ra nướca) Viết phương trình hóa học b) Khí Oxi và khí hidro ,chất nào dư sau phân tử tính thể tích khí dư.Biết thể tích các khí đo ở đktc c) Tính Khối lượng nước thu được bằng 2 cách?d) Tính thể tích ko khí (đktc) cần dùng để đốt cháy hết lượng khí hidro trên biết thể tích oxi bằng 1/5 thể tích ko khí?
Đọc tiếp
Câu hỏi : Cho 5,6 lít nước hidro tác dụng với 3,2g khíc Oxi tạo ra nước
a) Viết phương trình hóa học
b) Khí Oxi và khí hidro ,chất nào dư sau phân tử tính thể tích khí dư.Biết thể tích các khí đo ở đktc
c) Tính Khối lượng nước thu được bằng 2 cách?
d) Tính thể tích ko khí (đktc) cần dùng để đốt cháy hết lượng khí hidro trên biết thể tích oxi bằng 1/5 thể tích ko khí>?
- Bạn ơi, 5,6 lít của nước hay hiđro
Đúng 1
Bình luận (1)
a) 2H2 +O2 -->2H2O
b) nH2=5,6/22,4=0,25(mol)
nO2=3,2/16=0,2(mol)
lập tỉ lệ :
\(\dfrac{0,25}{2}< \dfrac{0,2}{1}\)
=> H2 hết , O2 dư =>bài toán tính theo H2
theo PTHH : nO2=1/2nH2=0,125(mol)
nO2(dư)=0,2 -0,125=0,075(mol)
=>VO2(dư)=0,075.22,4=1,68(l)
c)
C1 : theo PTHH :nH2O=nH2=0,25(mol)
=>mH2O=0,25.18=4,5(g)
C2: mH2=0,25.2=0,5(g)
mO2(phản ứng)=0,125.32=4(g)
áp dụng định luật bảo toàn khối lượng ta có :
mH2O=4 +0,5=4,5(g)
d) Vo2(đktc)=0,125.22,4=2,8(l)
=> Vkk=2,8 : 1/5=14(l)
Đúng 0
Bình luận (0)
mik sửa lại:
nO2=3,2/32=0,1(mol)
lập tỉ lệ :
\(\dfrac{0,1}{1}< \dfrac{0,25}{2}\)
=>O2 hết ,H2 dư =>bài toán tính theo O2
theo PTHH :
nH2=2nO2=0,2(mol)
=>nH2(dư)=0,25 -0,2=0,05(mol)
=>VH2(dư)=0,05.22,4=1,12(l)
c) C1:
theo PTHH : nH2O=2nO2=0,2(mol)
=>mH2O=0,2.18=3,6(g)
C2: mH2=0,2.2=0,4(g)
áp dụng định luật bảo toàn khối lượng ta có :
mH2O=0,4 +3,2=3,6(g)
d) VO2=0,1.22,4=2,24(l)
=>Vkk=2,24 :1/5=11,2(l)
Đúng 0
Bình luận (0)
đốt khí hidro trong khí oxi nhận thấy: cứ 2 thể tích H2 kết hợp với 1 thể tích O2 tạo thành nước . lập CTHH đơn giản của nước
Vì tỉ lệ thể tích bằng tỉ lệ số mol
=> nH2:nO2=VH2:VO2=2:1
=> PTHH: 2H2+O2-> 2H2O
=> CTHH H2O
Đúng 0
Bình luận (0)
1. Tính khối lượng của Nitơ có trong 49g NH4NO3
2. Đốt khí Hidro trong khí Oxi thấy: cứ 2 thể tích khí Hidro kết hợp với 1 thể tích khí Oxi tạo thành nước. Hãy lập công thức đơn giản của nước tạo thành
trong 1 mol NH4NO3 có: 2 mol N; 4 mol H; 3 mol O.
-> mN= nN.MN= 2 . 14 = 24g
Đúng 0
Bình luận (0)
hiện nay , để sản xuất amoniac , người ta điều chế nito và hidro bằng cách chuyển hóa có xúc tác một hỗn hợp gồm không khí , hơi nước và khí metan (thành phần chính của khí thiên nhiên) . Phản ứng giữa hơi nước và khí metan tạo ra hidro và cacbon dioxit . để loại khí oxi và thu khí nito , người ta đốt khí metan trong 1 thiết bị kín chứa không khí .hãy viết các phương trình hóa học của pah ứng điều chế hidro , loại khí oxi và tổng hợp khí amoniac .
Đọc tiếp
hiện nay , để sản xuất amoniac , người ta điều chế nito và hidro bằng cách chuyển hóa có xúc tác một hỗn hợp gồm không khí , hơi nước và khí metan (thành phần chính của khí thiên nhiên) . Phản ứng giữa hơi nước và khí metan tạo ra hidro và cacbon dioxit . để loại khí oxi và thu khí nito , người ta đốt khí metan trong 1 thiết bị kín chứa không khí .
hãy viết các phương trình hóa học của pah ứng điều chế hidro , loại khí oxi và tổng hợp khí amoniac .
CH4 + 2H2O 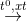 CO2 + 4H2
CO2 + 4H2
CH4 + 2O2 (kk) 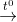 CO2 + 2H2O nên còn lại N2
CO2 + 2H2O nên còn lại N2
N2 + 3H2 ⇔ 2NH3
Đúng 0
Bình luận (0)
Thể tích của khí hidro cần dùng để hóa hợp với 2,24 lít khí oxi để tạo ra nước là.
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,2 \(\leftarrow\)0,1
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
Khí metan tan cháy trong oxi tạo thành khí cacbonic và hơi nước
a) viết phương trình phản ứng xảy ra , biết công thức hóa học của metan là CH4
b) tính thể tích oxi cần cần dùng để đốt cháy 11,2 l metan (đktc)
c) thể tích khí cacbonic tạo thành (đktc)
Xem chi tiết
a) PTHH: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
b+c)
Vì trong chất khí, tỉ lệ số mol cũng chính là tỉ lệ về thể tích
\(\Rightarrow\left\{{}\begin{matrix}V_{CO_2}=V_{CH_4}=11,2\left(l\right)\\V_{O_2}=2V_{CH_4}=22,4\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)




















