Hòa tan m gam Al bằng dung dịch NaOH dư. Sau khi phản ứng kết thúc thu được 3,36 lít khí H2 (đktc). Giá trị của m là
A. 8,1
B. 2,7
C. 2,025
D. 4,05
Hòa tan m gam Al bằng dung dịch NaOH dư. Sau khi phản ứng kết thúc thu được 3,36 lít khí H 2 (đktc). Giá trị của m là
A. 4,05
B. 2,025
C. 2,7
D. 8,1
Cho m gam hỗn hợp X gồm Al và Cu vào dung dịch HCl dư sau khi phản ứng kết thúc thu được 3,36 lít khí H2 (đktc). Nếu cho m gam hỗn hợp X trên tác dụng với H N O 3 đặc nguội dư, sau phản ứng thu được 6,72 lít khí N O 2 (đktc). Giá trị của m là
A. 15,6
B. 10,5
C. 11,5
D. 12,3
Hỗn hợp X gồm 8,1 gam Al và 10,8 gam FeO. Hòa tan hết X trong dung dịch axit sunfuric loãng dư, sau khi kết thúc phản ứng thu được V lít khí (đktc). Giá trị của V là:
A. 10,08.
B. 6,72.
C. 11,2.
D. 22,4.
$n_{Al} = \dfrac{8,1}{27} = 0,3(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
$n_{H_2} = \dfrac{3}{2}n_{Al} = 0,45(mol)$
$V = 0,45.22,4 = 10,08(lít)$
\(n_{Al}=\frac{8,1}{27}=0,3mol\\ 2Al+3H_2SO_4\rightarrow Al_2(SO_4)_3 +3H_2 n_{H_2}=0,45mol\\ V=10,08l\)
X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H 2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H 2 (đktc). Giá trị của m là
A. 19,1
B. 29,9
C. 24,5
D. 16,4
X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là
A. 19,1.
B. 29,9.
C. 24,5.
D. 16,4.
Hỗn hợp X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là
A. 16,4.
B. 29,9.
C. 24,5.
D. 19,1.
Hỗn hợp X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là
A. 16,4.
B. 29,9.
C. 24,5.
D. 19,1.
Hỗn hợp X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là
A. 29,9
B. 16,4
C. 19,1
D. 24,5
Hỗn hợp X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dung dịch NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là:
A. 24,5
B. 29,9
C. 19,1
D. 16,4
Đáp án A
Các phản ứng xảy ra:
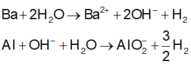
Vì thể tích H2 thu được ở hai trường hợp không bằng nhau nên khi hòa tan hỗn hợp vào nước dư thì còn một phần kim loại Al dư không tan.
Gọi n Ba = a n Al = b

Vậy m = mBa + mA1 = 24,5 (gam)