Số hiệu nguyên tử của X,Y lần lượt là 19 và 16. Hợp chất tạo thành từ X và Y là
![]()
![]()
![]()
![]()
Số hiệu nguyên tử của X, Y lần lượt là 19 và 16. Hợp chất tạo thành từ X và Y là ?
A. X2Y.
B. XY.
C. XY2.
D. X2Y3.
Đáp án A
X là Kali và Y là Lưu huỳnh
Công thức hợp chất tạo thành là K2S
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.
Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
A. 2 s 2 2 p 5 , 4 s 1 và liên kết cộng hóa trị.
B. 2 s 2 2 p 3 , 3 s 2 3 p 1 và liên kết cộng hóa trị.
C. 3 s 2 3 p 5 , 4 s 1 và liên kết ion.
D. 2 s 2 2 p 5 , 4 s 1 và liên kết ion.
Chọn D
Cấu hình electron nguyên tử X: [He]2s22p5.
Cấu hình electron nguyên tử Y: [Ar]4s1
X là phi kim điển hình (nhóm VIIA) và Y là kim loại điển hình (nhóm IA) nên liên kết trong hợp chất tạo thành từ X và Y là liên kết ion.
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
A. 2s22p5, 4s1 và liên kết cộng hóa trị.
B. 2s22p3, 3s23p1 và liên kết cộng hóa trị.
C. 3s23p1, 4s1 và liên kết ion.
D. 2s22p5, 4s1 và liên kết ion.
Cho các nguyên tố X và Y lần lượt có số hiệu nguyên tử là 19 và 8. Công thức hợp chất được tạo ra giữa X và Y có dạng như thế nào, trong hợp chất đó, liên kết giữa X và Y là
A. X2Y, liên kết ion.
B. Y2X, liên kết ion.
C. Y2X, liên kết cộng hóa trị.
D. X2Y, liên kết cộng hóa trị.
Đáp án A
X là Kali, Y là Oxi à K2O , liên hết ion
Cho các nguyên tố X và Y lần lượt có số hiệu nguyên tử là 19 và 8. Công thức hợp chất được tạo ra giữa X và Y có dạng như thế nào, trong hợp chất đó, liên kết giữa X và Y là
![]()
![]()
![]()
![]()
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 12, 17. Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
X: \(1s^22s^22p^63s^2\)
\(Y:1s^22s^22p^63s^23p^5\)
=> X cho 2e để đạt cấu hình bền vững, Y nhận 1e để đạt đến cấu hình bền vững
=> Hợp chất tạo bởi X,Y là XY2, liên kết ion
X, Y là những nguyên tố có đơn vị điện tích hạt nhân lần lượt là 6, 16. Công thức và liên kết hợp chất tạo thành từ X và Y là
A. XY và liên kết cộng hóa trị.
B. X 2 Y và liên kết ion.
C. XY và liên kết ion.
D. X Y 2 và liên kết cộng hóa trị.
Chọn D
Cấu hình electron nguyên tử X: [He]2s22p2
Cấu hình electron nguyên tử Y: [Ne] 3s23p4
Ta có:
: X : + 2 : Y . . : → : Y .. : : X : : Y : ..
→ Hợp chất cộng hóa trị tạo thành từ X và Y là XY2.
Cho các nguyên tử X, Y:
- Tổng số các loại hạt cơ bản trong nguyên tử X là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10.
- Kí hiệu của nguyên tử Y là Y 9 19 .
Công thức hóa học và liên kết trong hợp chất tạo thành từ X và Y là
A. XY và liên kết cộng hóa trị
B. X 2 Y và liên kết ion
C. XY và liên kết ion
D. X Y 2 và liên kết cộng hóa trị
Chọn C
- Xác định X:
Theo bài ra ta có hệ phương trình:
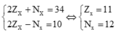
Cấu hình electron của X là: [Ne]3s1 → X là kim loại nhóm IA
X có xu hướng nhường 1e khi hình thành liên kết hóa học:
X → X+ + 1e
- Cấu hình electron của Y là: [He]2s22p5 → Y là phi kim nhóm VIIA hoặc từ kí hiệu nguyên tử xác định Y là Flo.
Y có xu hướng nhận 1e khi hình thành liên kết hóa học:
Y + 1e → Y-
Vậy hợp chất tạo thành là XY; liên kết trong hợp chất là liên kết ion.
X và Y đều là hợp chất ion cấu tạo thành từ các ion có chung cấu hình electron 1s22s22p6. Tổng số hạt proton, nơtron, electron trong phân tử X và Y lần lượt là 92 và 60. X và Y lần lượt là :
A.MgO; MgF2
B. MgF2 hoặc Na2O; MgO
C. Na2O; MgO hoặc MgF2
D. MgO; Na2O.
Đáp án B
Anion có cấu hình1s22s22p6 => Anion là F hoặc O
Cation có cấu hình1s22s22p6 => Cation là Na hoặc Mg
Nếu anion là O, tổng số hạt p,n,e trong X là 92, X là Na2O (2pNa + nNa) + (2pO + nO) = 92
Tổng số hạt trong Y là 60, vậy Y là MgO.
Nếu anion là F.
Tổng số hạt trong X là 92. X là MgF2