Trong phản ứng : Cl 2 + H 3 O → HCl + HClO phát biểu nào sau đây đúng ?
A. Clo chỉ đóng vai trò chất oxi hoá.
B. Clo chỉ đóng vai trò chất khử.
C. Clo vừa đóng vai trò chất oxi hoá, vừa đóng vai trò chất khử.
D. Nước đóng vai trò chất khử.
Trong phản ứng : Cl 2 + H 3 O → HCl + HClO phát biểu nào sau đây đúng ?
A. Clo chỉ đóng vai trò chất oxi hoá.
B. Clo chỉ đóng vai trò chất khử.
C. Clo vừa đóng vai trò chất oxi hoá, vừa đóng vai trò chất khử.
D. Nước đóng vai trò chất khử.
Cho phản ứng hoá học:
C l 2 + K O H → K C l + K C l O 3 + H 2 O
Tỉ lệ giữa số nguyên tử clo đóng vai trò chất oxi hoá và số nguyên tử clo đóng vai trò chất khử trong phương trình hoá học của phản ứng đã cho tương ứng là :
A. 1:5
B. 5:1
C. 1:3
D. 3:1
Hoàn thành PTHH của các phản ứng khi sục khí SO 2 vào dung dịch H 2 S à dung dịch nước clo. Trong các phản ứng đó, SO 2 đóng vai trò chất oxi hoá hay chất khử ?
1) SO 2 + H 2 S → S + H 2 O
2) SO 2 + Cl 2 + H 2 O → H 2 SO 4 + HCl
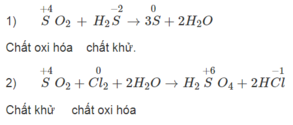
ở (1) SO 2 đóng vai trò là chất khử
ở (2) SO 2 đóng vai trò là chất oxi hóa.
Phản ứng dưới đây có thể được thực hiện để điều chế khí chlorine trong phòng thí nghiệm
4HCl + MnO2 → Cl2 + MnCl2 + 2H2O
a) Trong phản ứng trên, hãy xác định chất khử và chất oxi hóa
b) Hãy dự đoán, hydroiodic acid có phản ứng được với mangan(IV) oxide không. Giải thích.
\(4H\mathop {Cl}\limits^{ - 1} {\text{ }} + {\text{ }}\mathop {Mn}\limits^{ + 4} {O_2} \to {\mathop {Cl}\limits^0 _2} + {\text{ }}\mathop {Mn}\limits^{ + 2} C{l_2} + {\text{ }}2{H_2}O\)
a)
\(\mathop {Mn}\limits^{ + 4} + 2e \to \mathop {Mn}\limits^{ + 2} \) => MnO2 là chất oxi hóa
\(\mathop {2Cl}\limits^{ - 1} \to \mathop {C{l_2}}\limits^0 + 2e\) => HCl là chất khử
b) HI có tính khử mạnh hơn HCl
=> HI có thể phản ứng được với MnO2
4HI + MnO2 → I2 + MnI2 + 2H2O
Cho phản ứng điều chế nitơ trong phòng thí nghiệm:
N H 4 N O 2 → t ° N 2 + 2 H 2 O
Trong phản ứng này, nguyên tố nitơ đóng vai trò gì?
A. Chỉ đóng vai trò chất oxi hóa.
B. Chỉ đóng vai trò chất khử.
C. Vừa là chất oxi hóa, vừa là chất khử.
D. Không phải chất oxi hóa, cũng không phải là chất khử.
Cho các phản ứng hóa học sau:
Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hoá trong phản ứng nào sau đây?
A. 4S + 6NaOH → t ° 2Na2S + Na2S2O3 + 3H2O
B. S + 2Na → t ° Na2S
C. S + 6HNO3 đặc → t ° H2SO4 + 6NO2 + 4H2O
D. S + 3F2 → t ° SF6
Đáp án là A. 4S + 6NaOH → t ° 2Na2S + Na2S2O3 + 3H2O
Trong phản ứng hoá học, các chất : S, H 2 S , SO 2 , H 2 SO 3 có thể đóng vai trò chất oxi hoá hay chất khử ? Hãy viết PTHH của phản ứng để minh hoạ cho mỗi trường hợp.
Các chất có thể đóng vai trò chất oxi hoá là S, SO 2 , H 2 SO 3 . Thí dụ
a) S + 2Na → Na 2 S
b) SO 2 + 2 H 2 S → 3S + 2 H 2 O
c) H 2 SO 3 + 2 H 2 S → t ° 3S + 3 H 2 O
Các chất có thể đóng vai trò chất khử là S, H 2 S , SO 2 , H 2 SO 3 . Thí dụ
a) S + O 2 → t ° SO 2
b) H 2 S + Cl 2 → S + 2HCl
c) SO 2 + Br 2 + 2 H 2 O → H 2 SO 4 + 2HBr
d) 5 H 2 SO 3 + 2 KMnO 4 → 2 H 2 SO 4 + K 2 SO 4 + 2Mn SO 4 + 3 H 2 O
Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hoá trong phản ứng nào sau đây?
A. 4 S + 6 N a O H → 2 N a 2 S + N a 2 S 2 O 3 + 3 H 2 O
B. S + 2Na → Na2S
C. S + 6 H N O 3 đ ặ c → H 2 S O 4 + 6 N O 2 + 4 H 2 O
D. S + 3F2 → SF6
Cho sơ đồ hóa học của phản ứng: Cl2 + KOH → KCl + KClO3 + H2O. Tỉ lệ giữa số nguyên clo đóng vai trò chất oxi hóa và số nguyên tử clo đóng vai trò chất khử trong phương trình hóa học trên là:
A. 1 : 3.
B. 3 : 1.
C. 5 : 1.
D. 1 : 5.
Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3 số oxi hoá của nitơ biến đổi như thế nào? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hoá?
Phản ứng nhiệt phân:
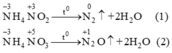
Trong hai phản ứng trên số oxi hoá của nitơ trong mỗi phản ứng đều thay đổi. Trong mỗi phân tử muối một nguyên tử nitơ có số oxi hoá tăng, một nguyên tử có số oxi hoá giảm, đây là phản ứng oxi hoá khử nội phân tử.Ở cả hai phản ứng nitơ nguyên tử trong ion NH+4 đều là chất khử (chất cho e) nitơ từ số oxi hoá -3 tăng lên 0 ở phản ứng (1) và lên +1 ở phản ứng (2).Nguyên tử nitơ trong ion NO2- và NO3- là chất oxi hoá (chất nhận e). Ở phản ứng (1) số oxi hoá của N từ +3 (trong NO2- ) xuống 0 và ở phản ứng (2) số oxi hoá của nitơ từ +5 (trong NO3-) xuống +1.