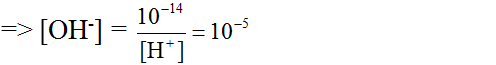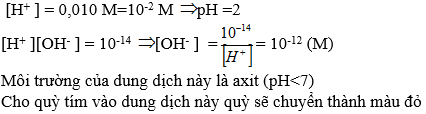Một dung dịch có pH = 9,0. Tính nồng độ mol của H+ và OH- trong dung dịch? Hãy cho biết màu của phenolphtalein trong dung dịch này?

Những câu hỏi liên quan
một dung dịch có pH=9,0 . Tính nồng độ mol của các ion H+ và OH- trong dung dịch . hãy cho biết màu của phenolphtalein trong dung dịch này .
[OH-] = 10^-14 : [H+] = 10^-12
pH = -log[H+] = 2 <7 => mt axit
pH = 9 => [H+] = 10^-9 => [OH-] = 10^-5 => mt bazo, phenolphtalein chuyển hồng
Đúng 0
Bình luận (0)
Một dung dịch có pH = 9,0. Tính nồng độ mol của các ion H+ và OH- trong dung dịch. Hãy cho biết màu của phenolphtalein trong dung dịch này.
pH=9 => CH+=10-9 và COH-=10-5
Đọo pH của dung dịch có môi trường kiêm nên Phenolphtalein có màu hồng (cái này trong sách giáo khoa 11 có)
Đúng 0
Bình luận (0)
Một dung dịch có pH = 9,0. Tính nồng độ mol của các ion H+ và OH- trong dung dịch. Hãy cho biết màu của phenolphtalein trong dung dịch này.
Một dung dịch có [H+] = 0,010 M. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm? Hãy cho biết màu của quỳ trong dung dịch này?
[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
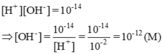
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ
Đúng 0
Bình luận (0)
Một dung dịch có [H+] = 0,020 M.
a. Tính [OH-] và pH của dung dịch.
b. Hãy cho biết màu của quỳ trong dung dịch này. Giải thích?
Một dung dịch có [H+] = 0,01 OM. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.
[H+] = 0,01M = 10-2M => pH = 2
[OH-] = 10-14 / 10-2M =10-12
Dung dịch có pH = 2 < 7 => môi trường axit, quỳ tím có màu đỏ.
Đúng 1
Bình luận (0)
Nhắc lại rằng, độ pH của một dung dịch được tính theo công thức pH - log left[ {{H^ + }} right], trong đó [H+] là nồng độ H+ của dung dịch đó tính bằng mol/L. Nồng độ H+ trong dung dịch cho biết độ acid của dung dịch đó.a) Dung dịch acid A có độ pH bằng 1,9; dung dịch acid B có độ pH bằng 25. Dung dịch nào có độ acid cao hơn và cao hơn bao nhiêu lần?b) Nước cất có nồng độ H+ là 10 mol/L. Nước chảy ra từ một vòi nước có độ pH từ 6,5 đến 6,7 thì có độ acid cao hay thập hơn nước cất?
Đọc tiếp
Nhắc lại rằng, độ pH của một dung dịch được tính theo công thức \(pH = - \log \left[ {{H^ + }} \right]\), trong đó [H+] là nồng độ H+ của dung dịch đó tính bằng mol/L. Nồng độ H+ trong dung dịch cho biết độ acid của dung dịch đó.
a) Dung dịch acid A có độ pH bằng 1,9; dung dịch acid B có độ pH bằng 25. Dung dịch nào có độ acid cao hơn và cao hơn bao nhiêu lần?
b) Nước cất có nồng độ H+ là 10 mol/L. Nước chảy ra từ một vòi nước có độ pH từ 6,5 đến 6,7 thì có độ acid cao hay thập hơn nước cất?
\(a,pH_A=1,9\Leftrightarrow-log\left[H^+\right]=1,9\Leftrightarrow H^+=10^{-1,9}\)
Vậy độ acid của dung dịch A là \(10^{-1,9}mol/L\)
\(pH_B=2,5\Leftrightarrow-log\left[H^+\right]=2,5\Leftrightarrow H^+=10^{-2,5}\)
Vậy độ acid của dung dịch B là \(10^{-2,5}mol/L\)
Ta có: \(\dfrac{H^+_A}{H_B^+}=\dfrac{10^{-1,9}}{10^{-2,5}}\approx398\)
Vậy độ acid của dung dịch A cao hơn độ acid của dung dịch B 3,98 lần.
Đúng 0
Bình luận (0)
b, Ta có:
\(6,5< pH< 6,7\\ \Leftrightarrow6,5< -log\left[H^+\right]< 6,7\\ \Leftrightarrow-6,7< log\left[H^+\right]< -6,5\\ \Leftrightarrow10^{-6,7}< H^+< 10^{-6,5}\)
Vậy nước chảy từ vòi nước có độ acid từ \(10^{-6,7}mol/L\) đến \(10^{-6,5}mol/L\)
Như vậy, nước đó có độ acid cao hơn nước cất.
Đúng 0
Bình luận (0)
một dung dịch có \(\left[H^+\right]=0,010M\) . Tính \(\left[OH^-\right]\) và pH của dung dịch . Môi trường của dung dịch là axit , trung tính hay kiềm ? hãy cho biết màu của quỳ tím trong dung dịch này .
[OH-]=1.10^-14/0.01=10^-12 (M) tính Ph=log[H+] từ kết quả của Ph xem nó lớn hơn 7 hay j xong suy ra môi trường ,môi trường axit thì quỳ đỏ môi trường kiềm quy xanh trung tính ko màu
Đúng 0
Bình luận (0)
Một dung dịch có [H+] = 0,01 OM. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm ? Hãy cho biết màu của quỳ tím trong dung dịch này.