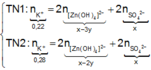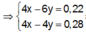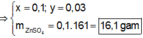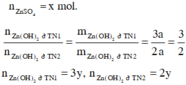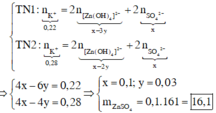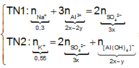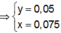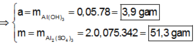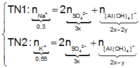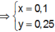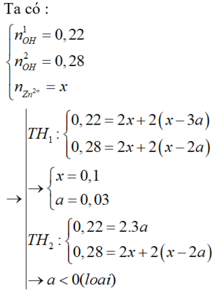Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:+ TN1: Cho dung dịch KOH dư vào V ml dung dịch Z, thu được
m
1
gam kết tủa.+ TN2: Cho dung dịch
K
2
C
O
3
dư vào V ml dung dịch Z, thu được
m
2
gam kết tủa.+ TN3: Cho dung dịch
A
g
N
O
3
dư v...
Đọc tiếp
Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
+ TN1: Cho dung dịch KOH dư vào V ml dung dịch Z, thu được
m
1
gam kết tủa.
+ TN2: Cho dung dịch
K
2
C
O
3
dư vào V ml dung dịch Z, thu được
m
2
gam kết tủa.
+ TN3: Cho dung dịch
A
g
N
O
3
dư vào V ml dung dịch Z, thu được
m
3
gam kết tủa. Biết các phản ứng xảy ra hoàn toàn và
m
1
<
m
3
<
m
2
. Hai chất X, Y lần lượt là
A.
C
a
H
C
O
3
2
v
à
F
e
C
l
2
.
B.
N
a
N
O
3
v
à
F
e
N
O
3
2
.
C.
N
a
C
l
v
à
F
e
C
l
2
.
D.
K
C
l
v
à
B
a
H
C
O
3
2
.







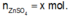
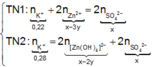
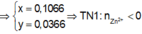 loại
loại