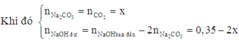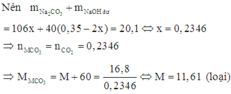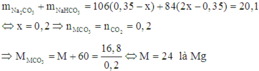1.Khí CO 2 có lẫn hơi nước, có thể làm khô khí CO 2 bằng:
A.H 2 SO 4 đậm đặc
B.Cả 3 trường hợp trên.
C.CaO khan
D.NaOH rắn
2.Nhiệt phân hoàn toàn 16,8g muối cacbonat của kim loại hóa trị II thu được 8g Oxit. Kim loại đó là:
A.Fe
B.Mg
C.Zn
D.Ca
3.Hàm lượng loại phân bón hóa học nào dưới đây chứa %N lớn nhất giúp cho cây trồng nhanh xanh tốt:
A.Supephotphat Ca(H 2 PO 4 ) 2
B.Urê CO(NH 2 ) 2
C.Kaliclorua KCl
D.Amônisunfat (NH 4 ) 2 SO 4
4Cặp chất nào sau đây phản ứng được với nhau:
A.K 2 CO 3 và NaOH
B.Cu(OH) 2 và CaCO 3
C.Na 2 CO 3 và HCl
D.KOH và MgCO 3
5.Cho 32,7 gam hỗn hợp gồm Cu(OH) 2 , Fe(OH) 2 phản ứng hoàn toàn với 300 ml dung dịch H 2 SO 4 thu được dung dịch A có chứa 54,4 gam muối. Phần % khối lượng mỗi chất có trong hỗn hợp đầu là.
A.80%; 20%
B.45%; 55%
C.40%; 60%
D.49,7; 50,3%