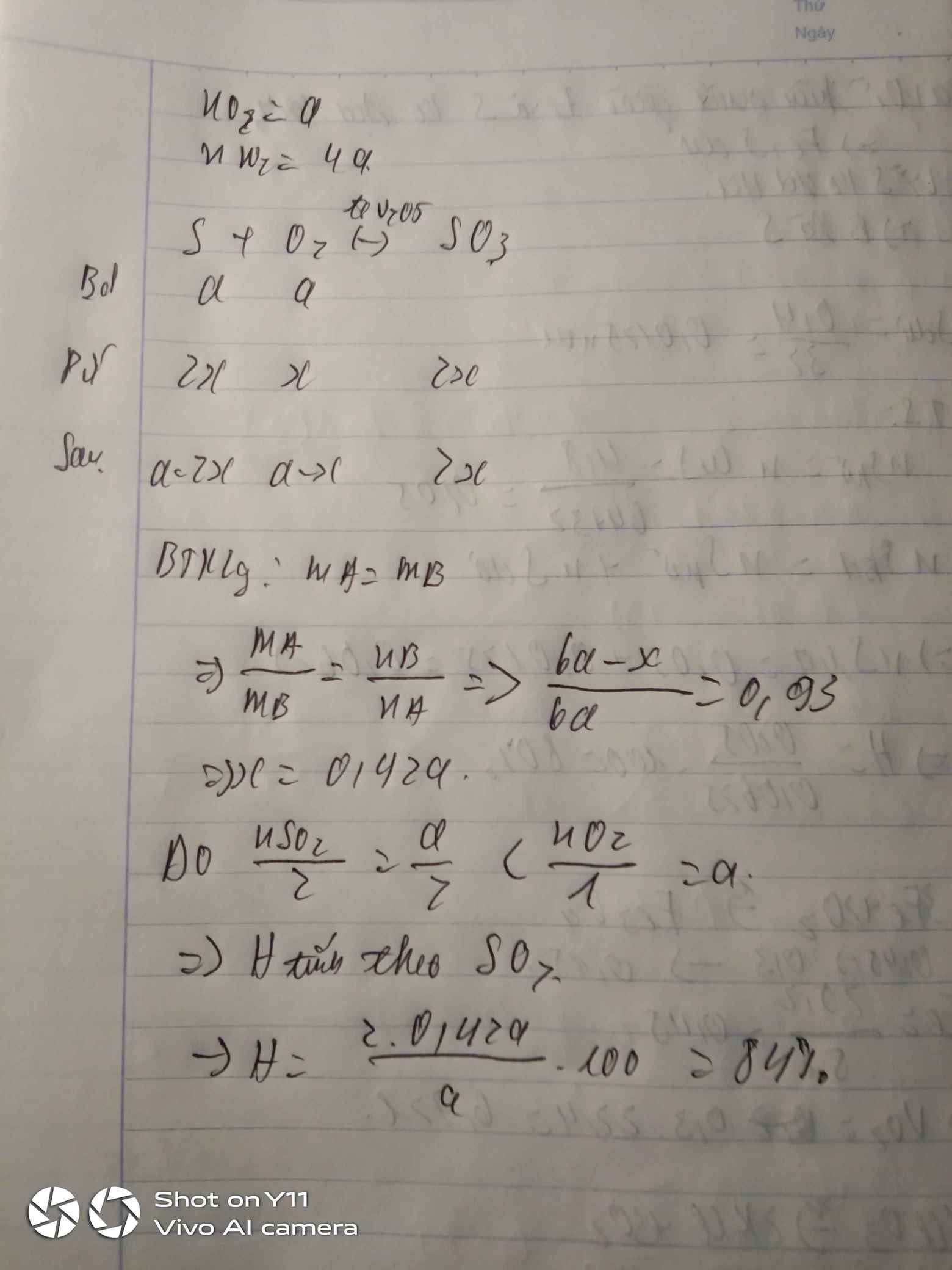hỗn hợp A gồm 63/100 mol N2 và x mol SO2.tính tỉ khối A so với khí H2 là........ tính x

Những câu hỏi liên quan
Bài 1. a) Tính tỉ khối hơi của khí SO2 so với khí O2 N2, SO3, CO, N2O, NO2.b) Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol 1:1 đối với khí O2.Bài 2. a) Tính tỉ khối hơi của hỗn hợp khí X gồm hai khí N2 và CO đối với khí metan CH4. Hỗn hợp X nặng hay nhẹ hơn không khí?b) Tính tỉ khối hơi của hỗn hợp Y đồng khối lượng gồm khí C2H4 (etilen), N2 và khí CO so với khí H2.c) Hỗn hợp khí X gồm: NO, NxO, CH4. Trong đó NO chiếm 30% về thể tích, NxO chiếm 30% còn lại là CH4. Trong hỗn hợp...
Đọc tiếp
Bài 1. a) Tính tỉ khối hơi của khí SO2 so với khí O2 N2, SO3, CO, N2O, NO2.
b) Tính tỉ khối hơi của hỗn hợp khí A gồm SO2 và O2 có tỉ lệ mol 1:1 đối với khí O2.
Bài 2. a) Tính tỉ khối hơi của hỗn hợp khí X gồm hai khí N2 và CO đối với khí metan CH4. Hỗn hợp X nặng hay nhẹ hơn không khí?
b) Tính tỉ khối hơi của hỗn hợp Y đồng khối lượng gồm khí C2H4 (etilen), N2 và khí CO so với khí H2.
c) Hỗn hợp khí X gồm: NO, NxO, CH4. Trong đó NO chiếm 30% về thể tích, NxO chiếm 30% còn lại là CH4. Trong hỗn hợp CH4 chiếm 22,377% về khối lượng. Xác định công thức hoá học của NxO. Tính tỷ khối của X so với không khí
Bài 2:
a) Vì khối lượng mol của N2 và CO đều bằng 28 và lớn hơn khối lượng mol của khí metan CH4 (28>16)
=> \(d_{\dfrac{hhX}{CH_4}}=\dfrac{28}{16}=1,75\)
Hỗn hợp X nhẹ hơn không khí (28<29)
b)
\(M_{C_2H_4}=M_{N_2}=M_{CO}=28\left(\dfrac{g}{mol}\right)\\ \rightarrow M_{hhY}=28\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{Y}{H_2}}=\dfrac{28}{2}=14\)
c) \(\%V_{NO}=100\%-\left(30\%+30\%\right)=40\%\\ \rightarrow\%n_{CH_4}=40\%\\ Vì:\%m_{CH_4}=22,377\%\\ Nên:\dfrac{30\%.16}{40\%.30+30\%.16+30\%.\left(x.14+16\right)}=22,377\%\\ \Leftrightarrow x=-0,03\)
Sao lại âm ta, để xíu anh xem lại như nào nhé.
Đúng 2
Bình luận (4)
Bài 1:
\(a.\\ d_{\dfrac{SO_2}{O_2}}=\dfrac{64}{32}=2\\ d_{\dfrac{SO_2}{N_2}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{SO_3}}=\dfrac{64}{80}=0,8\\ d_{\dfrac{SO_2}{CO}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{N_2O}}=\dfrac{64}{44}=\dfrac{16}{11}\\ d_{\dfrac{SO_2}{NO_2}}=\dfrac{64}{46}=\dfrac{32}{23}\\ b.M_{hhA}=\dfrac{1.64+1.32}{1+1}=48\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{hhA}{O_2}}=\dfrac{48}{32}=1,5\)
Đúng 4
Bình luận (2)
Hỗn hợp khí A gồm N2 và H2 có tỉ khối đối với hiđro là 5,875.
a/ Tính khối lượng mol trung bình của hỗn hợp.
b/ Tính % số mol mỗi khí trong hỗn hợp.
c/ Trộn thêm x mol NH3 vào 1 mol hỗn hợp A, ta được hỗn hợp mới (hỗn hợp B) có tỉ khối đối với hiđro là 6,4. Tìm x.
a) \(\overline{M}_A=5,875.2=11,75\left(g/mol\right)\)
b) Gọi số mol N2, H2 là a, b (mol)
\(\overline{M}_A=\dfrac{28a+2b}{a+b}=11,75\left(g/mol\right)\)
=> 16,25a = 9,75b
=> a = 0,6b
\(\left\{{}\begin{matrix}\%n_{N_2}=\dfrac{a}{a+b}.100\%=\dfrac{0,6b}{0,6b+b}.100\%=37,5\%\\\%n_{H_2}=\dfrac{b}{a+b}.100\%=\dfrac{b}{0,6b+b}.100\%=62,5\%\end{matrix}\right.\)
c)
1 mol hỗn hợp A chứa \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{1.37,5}{100}=0,375\left(mol\right)\\n_{H_2}=\dfrac{1.62,5}{100}=0,625\left(mol\right)\end{matrix}\right.\)
\(\overline{M}_B=\dfrac{0,375.28+0,625.2+17x}{1+x}=6,4.2=12,8\left(g/mol\right)\)
=> x = 0,25 (mol)
Đúng 1
Bình luận (0)
Hỗn hợp A gồm 0,1 mol CH4 và 0,4 mol N2. Tính tỉ khối của A so với khí H2.
mCH4 = 0,1 . 16 = 1,6 (g)
mN2 = 28 . 0,4 = 11,2 (g)
M(A) = (1,6 + 11,2)/(0,1 + 0,4) = 25,6 (g/mol)
d(A/H2) = 25,6/2 = 12,8
Đúng 3
Bình luận (0)
Câu 4. Tính khối lượng mol của các khí sau biết các khí này có tỉ khối đối với không khí lần lượt là: 2,207; 1,172; 1,517.
Câu 7. Một hỗn hợp khí A gồm 0,2 mol SO2; 0,5 mol CO2 và 0,75 mol N2.
a) Tính số mol và tính thể tích của hỗn hợp khí A( đktc).
b) Tính khối lượng của hỗn hợp khí A.
c) Tính khối lượng mol trung bình của hỗn hợp khí A
d) Tính thành phần % về khối lượng, %V của mỗi khí có trong hỗn hợp A.
Đọc tiếp
Câu 4. Tính khối lượng mol của các khí sau biết các khí này có tỉ khối đối với không khí lần lượt là: 2,207; 1,172; 1,517. Câu 7. Một hỗn hợp khí A gồm 0,2 mol SO2; 0,5 mol CO2 và 0,75 mol N2. a) Tính số mol và tính thể tích của hỗn hợp khí A( đktc). b) Tính khối lượng của hỗn hợp khí A. c) Tính khối lượng mol trung bình của hỗn hợp khí A d) Tính thành phần % về khối lượng, %V của mỗi khí có trong hỗn hợp A.
Bài 1:
a) tìm khối lượng mol của các khí có tỉ khối đối với không khí là : +1,172 .29=34
;+ 2,207 .29=64
+0,5862.29=17
b) tìm khối lượng mol của những chất khí có tỉ khối đối với hidro là: +8,5.2=17
+17 .2=34
+22.2=44
Bài 2 :
Tính thể tích ở ĐKTC của:
a) 2 mol khí C2H6
V C2H6=2.22,4=44,8(l)
b) 13 gam khí C2H2
n C2H2=13/26=0,5(mol)
V C2H2=0,5.22,4=11,2(l)
c) 8 gam khí SO2
n SO2=8/64=0,125(mol)
V SO2=0,125.22,4=2,8(l)
d) 0,2 mol khí cacbonic và 0,3 mol khí CO
V hỗn hợp = (0,2+0,3).22,4=11,2(l)
Đúng 3
Bình luận (0)
hỗn hợp X gồm 0,15 mol SO2 và 0,2 mol CO2
a) tính khối lượng mol trung bình của hỗn hợp X
b) tính tỉ khối của hỗn hợp X so với khí NO2
MONG MỌI NGƯỜI GIẢI CHI TIẾT RA GIÚP EM VỚI Ạ .|
\(a.\)
\(m_{hh}=m_{SO_2}+m_{CO_2}=0.15\cdot64+0.2\cdot44=18.4\left(g\right)\)
\(n_{hh}=0.15+0.2=0.35\left(mol\right)\)
\(\overline{M}_X=\dfrac{m_{hh}}{n_{hh}}=\dfrac{18.4}{0.35}=52.5\left(\dfrac{g}{mol}\right)\)
\(b.\)
\(d_{X\text{/}NO_2}=\dfrac{52.57}{46}=1.14\)
Đúng 2
Bình luận (1)
a)Tính khối lượng trung bình:
Mx=(n*Mso2+n*Mco2)/(nso2+nco2)
Mx=(0.15*64+0.2*44)/0.35
Mx=52.57(g/mol)
b)Ta có:dx/NO2=52.57/Mno2=52.57/46
=1.143
Đúng 0
Bình luận (0)
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:a, Khí hydrogen.b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Đọc tiếp
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:
a, Khí hydrogen.
b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Cho 12,395 lít hỗn hợp khí X gồm N2 và NO,tỉ khối của x so với khí hydrogen là 14,5 a) Tính số mol mỗi khí trong hỗn hợp khí x b) Tính % khối lượng mỗi khí trong x
Đọc tiếp
Cho 12,395 lít hỗn hợp khí X gồm N2 và NO,tỉ khối của x so với khí hydrogen là 14,5 a) Tính số mol mỗi khí trong hỗn hợp khí x b) Tính % khối lượng mỗi khí trong x
Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{NO}=y\left(mol\right)\end{matrix}\right.\)
\(n_{hh}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\) (chắc đkc nhỉ vì đktc số kì: )
=> x + y = 0,5 (1)
Tỉ khối của X so với khí `H_2` là 14,5 có:
\(M_X=14,5.2=29\left(g/mol\right)\\ \Leftrightarrow\dfrac{28x+30y}{x+y}=29\\ \Rightarrow x-y=0\left(2\right)\)
Từ (1), (2) có: \(\left\{{}\begin{matrix}x+y=0,5\\x-y=0\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,25\\y=0,25\end{matrix}\right.\) (bấm máy giải hệ)
a
Số mol mỗi khí trong hỗn hợp khí X: \(n_{N_2}=n_{NO}=0,25\left(mol\right)\)
b
\(\%_{m_{N_2}}=\dfrac{0,25.28.100\%}{0,25.28+0,25.30}=48,28\%\)
\(\%_{m_{NO}}=100\%-48,28\%=51,72\%\)
Đúng 2
Bình luận (0)
Bài 79 : Tính tỉ khối hơi trong các trường hợp sau : a) Hỗn hợp X chứa 0,2 mol O2 và 0,15 mol CO so với không khí b) Hỗn hợp Y chứa 0,5 mol CO2 và 2 mol H2 so với khí oxic) Hỗn hợp A chứa 17,75g Cl2 và 8,4g N2 so với khí CO2 d) Hỗn hợp B chứa 5,1g NH3 và 5,6g CO so với không khí e) Hỗn hợp R chứa 2,24 lít khí CO và 3,36 lít khí CO2 so với khí oxif) Hỗn Hợp Z chứa 5,6 lít khí NO2 và 8,96 lít CO2 so với khí SO2
Đọc tiếp
Bài 79 : Tính tỉ khối hơi trong các trường hợp sau :
a) Hỗn hợp X chứa 0,2 mol O2 và 0,15 mol CO so với không khí
b) Hỗn hợp Y chứa 0,5 mol CO2 và 2 mol H2 so với khí oxi
c) Hỗn hợp A chứa 17,75g Cl2 và 8,4g N2 so với khí CO2
d) Hỗn hợp B chứa 5,1g NH3 và 5,6g CO so với không khí
e) Hỗn hợp R chứa 2,24 lít khí CO và 3,36 lít khí CO2 so với khí oxi
f) Hỗn Hợp Z chứa 5,6 lít khí NO2 và 8,96 lít CO2 so với khí SO2
a, mX = 0,2.32 + 0,15.28 = 10,6 (g)
nX = 0,2 + 0,15 = 0,35 (mol)
=> MX = \(\dfrac{10,6}{0,35}=30,3\left(\dfrac{g}{mol}\right)\)
=> dX/kk = \(\dfrac{30,3}{29}=1,05\)
b, mY = 0,5.44 + 2.2 = 26 (g)
nY = 0,5 + 2 = 2,5 (mol)
=> MY = \(\dfrac{26}{2,5}=10,4\left(\dfrac{g}{mol}\right)\)
=> dY/O2 = \(\dfrac{10,4}{32}=0,325\)
c, mA = 17,75 + 8,4 = 26,15 (g)
nA = \(\dfrac{17,75}{71}+\dfrac{8,4}{28}=0,55\left(mol\right)\)
=> MA = \(\dfrac{26,15}{0,55}=47,6\left(\dfrac{g}{mol}\right)\)
=> dA/CO2 = \(\dfrac{47,6}{44}=1,1\)
Mình làm mẫu 3 ý đầu rồi mấy ý sau bạn tự làm nhé
Đúng 3
Bình luận (2)
Hỗn hợp khí A gồm a mol SO2 và 5a mol không khí. Nung nóng hỗn hợp A với V2O5 xúc tác thu được hỗn hợp khí B. Biết rằng tỉ khối hơi của A so với B bằng 0,93. Hãy tính hiệu suất phản ứng giữa SO2 và O2. Cho không khí có chưa 80% N2 và 20% O2 theo thể tích.
giúp em nhanh với e tick nhanh cho ạ , em cảm ơn ạ
Hỗn hợp A ban đầu có SO2 : a mol, N2: 4a mol và O2: a mol.
Phản ứng:
2SO2 + O2< --> 2SO3 (XT: V2O5, t0) (1)
Gọi số mol SO2 phản ứng là x.
Theo (1): Số mol giảm = số mol O2 phản ứng = 0,5x mol
=> nB = 6a – 0,5x mol
Theo định luật bảo toàn khối lượng: mA = mB = m
\(d_{A/B}=\dfrac{m}{6a}:\dfrac{m}{6a-0,5x}=\dfrac{6a-0,5x}{6a}=0,93\)
\(\Rightarrow\dfrac{x}{a}=0,84\)
\(VậyH\%=84\%\)
Đúng 2
Bình luận (2)
hỗn hợp khí A gồm N2 và CO2 có tỉ khối so với khí Hiđro là 18. Tính thành phần phần trăm khối lượng của mỗi khí trong hợp chất .Cần thêm bao nhiêu gam CO2 vào 0,2 mol hỗn hợp A để tỉ khối của hỗn hợp B thu được có tỉ khối so với H2 là 20
\(a.\)
\(GS:\)
\(n_{hh}=1\left(mol\right)\)
\(Đặt:n_{N_2}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(\Rightarrow a+b=1\left(1\right)\)
\(m_A=28a+44b=18\cdot2=36\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=b=0.5\)
\(\%m_{N_2}=\dfrac{0.5\cdot28}{0.5\cdot28+0.5\cdot44}\cdot100\%=38.89\%\)
\(\%m_{CO_2}=61.11\%\)
\(b.\)
\(\dfrac{n_{N_2}}{n_{CO_2}}=\dfrac{0.5}{0.5}=\dfrac{1}{1}\)
\(n_{N_2}=n_{CO_2}=\dfrac{1}{2}\cdot n_A=\dfrac{0.2}{2}=0.1\left(mol\right)\)
\(Đặt:n_{CO_2}=x\left(mol\right)\)
\(\overline{M}=\dfrac{0.1\cdot28+0.1\cdot44+44x}{0.2+x}=20\cdot2=40\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.2\)
\(m_{CO_2\left(cầnthêm\right)}=0.2\cdot44=8.8\left(g\right)\)
Đúng 1
Bình luận (6)