Tn1: CuO tác dụng vs dung dịch HCl
Tn2: dung dịch H2SO4 tác dụng dung dịch NaOH (Phản ứng trung hoà)
Tn3: Phân biệt 3 lọ: HCl, H2SO4, NaCl bị mất nhãn
Nếu hiện tượng, cách làm thí nghiệm, giải thích và viết PTHH ! HELP ME PLS
Cho các phát biểu sau:
(1) Cr không tác dụng với dung dịch HNO3 đặc nguội và H2SO4 đặc nguội.
(2) CrO3 là oxit lưỡng tính.
(3) Dung dịch hỗn hợp K2Cr2O7 và H2SO4 có tính oxi hóa mạnh.
(4) Ở nhiệt độ cao, Cr tác dụng với dung dịch HCl và Cr tác dụng với Cl2 đều tạo thành CrCl2.
(5) Cr(OH)3 vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH.
(6) Crom là kim loại có tính khử yếu hơn sắt.
Số phát biểu sai là:
A. 2
B. 3
C. 4
D. 5
Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe
Cho các phát biểu sau:
(1) Cr không tác dụng với dung dịch HNO3 đặc nguội và H2SO4 đặc nguội.
(2) CrO3 là oxit lưỡng tính.
(3) Dung dịch hỗn hợp K2Cr2O7 và H2SO4 có tính oxi hóa mạnh.
(4) Ở nhiệt độ cao, Cr tác dụng với dung dịch HCl và Cr tác dụng với Cl2 đều tạo thành CrCl2.
(5) Cr(OH)3 vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH.
(6) Crom là kim loại có tính khử yếu hơn sắt.
Số phát biểu sai là:
A. 2
B. 3
C. 4
D. 5
Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.
Trình bày phương pháp nhận biết cấc chất để trong những lọ riêng biệt bị mất nhãn sau: a, Các chất rắn: P2O5; NaOH; Al(OH)3; NaCl b, nước, dung dịch HCl, dung dịch KCl, dung dịch KOH. c. Các chất khí: O2, CO2, H2, N2, HCl
a) - Cho các chất rắn vào nước:
+ Chất rắn không tan, tạo kt keo trắng -> Al(OH)3
+ Còn lại 3 chất rắn tan, tạo thành dung dịch
PTHH: P2O5 + 3 H2O -> 2 H3PO4
- Cho quỳ tím vào các dung dịch:
+ Hóa xanh -> dd NaOH -> Rắn NaOH
+ HÓA đỏ -> dd H3PO4 -> Rắn P2O5
+ Không đổi màu quỳ -> dd NaCl -> rắn NaCl
b) - Dùng quỳ tím:
+ Hóa đỏ -> dd HCl
+ Hóa xanh -> dd KOH
+ Không đổi màu -> H2O và dd KCl.
- Dùng AgNO3 làm thuốc thử:
+ Có kt trắng AgCl -> Nhận biết KCl.
+ Không có kt trắng -> H2O
PTHH: AgNO3 + KCl -> KNO3 + AgCl
b)
- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Hóa xanh: KOH
+) Không đổi màu: KCl và nước
- Đổ dd AgNO3 vào 2 lọ còn lại
+) Xuất hiện kết tủa: KCl
PTHH: \(AgNO_3+KCl\rightarrow AgCl\downarrow+HNO_3\)
+) Không hiện tượng: H2O
Cho hỗn hợp X gồm CuO và NaOH có tỉ lệ số mol 1:1 tác dụng vừa đủ với dung dịch hỗn hợp HCl 1M và H2SO4 0,5M thu được dung dịch Y chỉ chứa m gam hỗn hợp muối trung hòa. Điện phân dung dịch Y với điện cực trơ màng ngăn xốp cường độ I = 2,68A đến khi khối lượng dung dịch giảm 20,225 gam mất t giây thì dừng lại, thu được dung dịch Z. Cho m gam Fe vào Z, sau khi phản ứng kết thúc thu được 0,9675m gam hỗn hợp hai kim loại. Giá trị của t là
A. 11523
B. 10684
C. 12124
D. 14024
(2) CrO3 là oxit lưỡng tính.
(3) Dung dịch hỗn hợp K2Cr2O7 và H2SO4 có tính oxi hóa mạnh.
(4) Ở nhiệt độ cao, Cr tác dụng với dung dịch HCl và Cr tác dụng với Cl2 đều tạo thành CrCl2.
(5) Cr(OH)3 vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH.
(6) Crom là kim loại có tính khử yếu hơn sắt.
Số phát biểu sai là:
A. 2
B. 3
C. 4
D. 5
Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.
1.Hoà tan V lít khí HCL vào nước thành 200ml dung dịch X. Trung hoà 100ml dung dịch X cần vừa hết 0,05 lít dung dịch NaOH 1M. Hỏi V có giá trị là bao nhiêu?
2.Hoà tan 34,8 gam MnO2 vào dung dịch HCL đặc, sau phản ứng thu được V lít khi clo. Hỏi giá trị của V là bao nhiêu?
3. Sục khí clo dư vào bình chứa NaBr, NaI đến phản ứng hoàn toàn thu được 23,4 gam muối NaCl. Số mol hỗn hợp ban đầu là bao nhiêu?
4.Kim loại X tác dụng với clo cho muối B, cũng kim loại X như trên cho tác dụng với dung dịch HCL cho muối C. Cho kim loại X tác dụng với dung dịch muối B ta được muối C. Hỏi X là kim loại nào?
Các bạn giải gấp hộ mik nhé. T3 mik kiểm tra rồi
1. HCl + NaOH => NaCl + H2O (1)
nNaOH = 0,05.1 = 0,05 (mol)
(1) => nHCl = nNaOH = 0,05 (mol)
Trong 100 ml dd X có 0,05 mol HCl
=> Trong 200 ml dd X có 0,1 mol HCl
VHCl = 0,1.22,4 = 2,24 (l)
2. MnO2 + 4HClđ=>MnCl2 + Cl2 +2H2O(2)
nMnO2 = \(\frac{34,8}{87}=0,4\left(mol\right)\)
(2) => nCl2 = nMnO2 = 0,4 (mol)
=> VCl2 = 0,4.22,4 = 8,96 (l)
3. Cl2 + 2NaBr => 2NaCl + Br2 (3)
Cl2 + 2NaI => 2NaCl + I2 (4)
nNaCl = \(\frac{23,4}{58,5}=0,4\left(mol\right)\)
(3),(4) => nhỗn hợp ban đầu = nNaCl = 0,4 (mol)
4. X + Cl2 => B
X + HCl => C
X + B => C
=> X : Fe
Cho 1,6g CuO tác dụng với 11,76g dung dịch H2SO4 có nồng độ 25%. Xác định nồng độ % của các chất thu được trong dung dịch sau phản ứng.
CuO+ H2SO4------------>CuSO4+ H2O
nCuO=0.02 mol
nH2SO4=\(\dfrac{11.76\cdot25\%}{98}\)=0.03 mol
Xét tỉ lệ nCuO/1<nH2SO4/1
=>CuO hết, H2SO4 dư tính theo CuO
Theo PTHH nH2SO4=nCuSO4=nCuO=0.02 mol
mdd=1.6+11.76=13.36(g)
Do đó %mH2SO4 dư=\(\dfrac{\left(0.03-0.02\right)\cdot98\cdot100}{13.36}\)=7.33%
%mCuSO4=\(\dfrac{0.02\cdot160\cdot100}{13.36}\)=23.95%
Cho 150 cm3 dung dịch NaOH 7M tác dụng với 100cm3 dung dịch Al2(SO4)3 1M. Hãy xác định nồng độ mol của NaOH trong dung dịch sau phản ứng.
A. 0,8M
B. 1,2M
C. 1M
D. 0,75M
Đáp án C
Ta có: nNaOH = 7.0,15 = 1,05 mol; nAl2(SO4)3= 1.0,1 = 0,1 mol
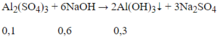
Vì NaOH dư nên:
Al(OH)3 + NaOH → Na[Al(OH)4]
Sau phản ứng có 0,2 mol Na[Al(OH)4] và 0,25 mol NaOH dư.
Nồng độ mol của Na[Al(OH)4]
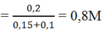
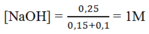
Cho m gam hỗn hợp X gồm hai amino axit A và B (MA < MB) có tổng số mol là 0,05; chỉ chứa tối đa 2 nhóm -COOH (cho mỗi chất). Cho m gam hỗn hợp X trên tác dụng với 56 ml dung dịch H2SO4 0,5M. Sau phản ứng phải dùng 6 ml dung dịch NaOH 1M để trung hòa hết với H2SO4 dư. Nếu lấy 1/2 hỗn hợp X tác dụng vừa đủ với 25 ml dung dịch Ba(OH)2 0,6M; cô cạn dung dịch sau phản ứng thu được 4,26 gam muối. Thành phần phần trăm (khối lượng) của amino axit B trong m gam hỗn hợp X là
A. 52,34
B. 32,89.
C. 78,91.
D. 24,08.