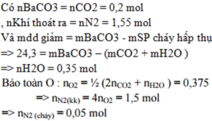Đốt cháy hoàn toàn 9g một chất hữu cơ A có tp là C H N bằng 1 lượng không khí vừa đủ , thu dc 94,08l khí T gồm Co2 H2O N2. Dẫn T lần lượt qua bình chứa Ca(Oh)2 dư xuất hiện 40g kết tủa, khối lượng dd giảm 13,4g, bình 2 tăng 3,6g.Tìm CTPT

Những câu hỏi liên quan
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 2. CTPT của X là A. C2H4N2 B. C2H8N C. C2H7N2 D. C2H7N
Đọc tiếp
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2< 2. CTPT của X là
A. C2H4N2
B. C2H8N
C. C2H7N2
D. C2H7N
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 2. CTPT của X là A. C2H7N B. C3H9N C. C3H6N2 D. C2H4N2
Đọc tiếp
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 < 2. CTPT của X là
A. C2H7N
B. C3H9N
C. C3H6N2
D. C2H4N2
Đốt cháy hoàn toàn m gam chất hữu cơ A cần 2,24 lít khí oxi(đktc) rồi dẫn toàn bợ sản phẩm cháy gồm (CO2, H2O) vào bình đựng dd Ca(OH)2 dư thấy khối lượng bình tăng 4,2g đồng thời xuất hiện 7,5g kết tủa. Tính m
\(n_{CaCO_3}=\dfrac{7,5}{100}=0,075\left(mol\right)\)
=> nC = 0,075 (mol)
Có \(n_{CO_2}=n_C=0,075\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{4,2-0,075.44}{18}=0,05\left(mol\right)\)
=> nH = 0,1 (mol)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Bảo toàn O: \(n_{O\left(A\right)}=0,075.2+0,05-0,1.2=0\left(mol\right)\)
=> A chứa C, H
mA = mC + mH = 0,075.12 + 0,1.1 = 1 (g)
Đúng 4
Bình luận (3)
\(m_{tăng}=m_{H_2O}+m_{CO_2}=4,2\left(g\right)\\ n_{CaCO_3}=\dfrac{7,5}{100}=0,075\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,075 0,075
\(\rightarrow m_{CO_2}=0,075.44=3,3\left(g\right)\\ \rightarrow m_{H_2O}=4,2-3,3=0,9\left(g\right)\\ \rightarrow n_{H_2O}=\dfrac{0,9}{18}=0,05\left(mol\right)\\ \rightarrow n_{O\left(sau.pư\right)}=0,05+0,075.2=0,1\left(mol\right)\\ n_{O\left(trong.O_2\right)}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \rightarrow\left\{{}\begin{matrix}n_C=0,075\left(mol\right)\\n_H=0,05.2=0,1\left(mol\right)\\n_O=0,1-0,1=0\left(mol\right)\end{matrix}\right.\)
=> mA = 0,075.12 + 0,1.1 + 0 = 1 (g)
đốt cháy hoàn toàn 0,59g hợp chất Q ( CxHyN ) bằng 1 lượng không khí vừa đủ(giả thiết trong không khí có 20%O2 và 80%N2)thu được hỗn hợp A gồm CO2,H2O,N2 . dẫn toàn bộ hỗn hợp A vào bình đựng dung dịch Ca(OH)2 dư thu dược 3 gam kết tủa và có 4,816 lít khí (đktc) duy nhất thoát ra khỏi bình . xác định công thức phân tử của Q
đốt cháy hoàn toàn 0,59g hợp chất Q ( CxHyN ) bằng 1 lượng không khí vừa đủ giả thiết trong không khí có 20%O2 và 80%N2 thu được hỗn hợp A gồm CO2,H2O,N2 . dẫn toàn bộ hỗn hợp A vào bình đựng dung dịch Ca(OH)2 dư thu dược 3 gam kết tủa và có 4,816 lít khí (dktc) duy nhất thoát ra khỏi bình . xác định công thức phân tử Q
\(n_{N_2\left(tổng\right)}=\dfrac{4,816}{22,4}=0,215\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{3}{100}=0,03\left(mol\right)\)
=> nCO2 = 0,03 (mol)
=> \(n_{C_xH_yN}=\dfrac{0,03}{x}\left(mol\right)\)
=> \(M_{C_xH_yN}=\dfrac{0,59}{\dfrac{0,03}{y}}=\dfrac{59}{3}x\left(mol\right)\)
=> 12x + y + 14 = \(\dfrac{59}{3}x\)
=> \(\dfrac{-23}{3}x+y=-14\) (1)
Bảo toàn H: \(n_{H_2O}=\dfrac{0,03y}{2x}\left(mol\right)\)
Bảo toàn N: \(n_{N_2\left(kk\right)}=\dfrac{0,215.2-\dfrac{0,03}{x}}{2}=0,215-\dfrac{0,015}{x}\left(mol\right)\)
Mà nN2 = 4.nO2
=> \(n_{O_2}=0,05375-\dfrac{0,00375}{x}\left(mol\right)\)
Bảo toàn O: \(0,1075-\dfrac{0,0075}{x}=0,06+\dfrac{0,03y}{2x}\)
=> \(0,03y+0,015=0,095x\) (2)
(1)(2) => x = 3; y = 9
CTPT: C3H9N
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 14,6g hợp chất hữu cơ Y thu được CO2 , H2O, và N2 . Dẫn toàn bộ sản phẩm thu được qua bình đưng dung dịch Ca(OH)2 dư thu được 80g kết tủa , khối lượng bình tăng 55g đồng thời có 2,24(lit) khí (đktc) thoát ra khỏi bình . tìm công thức phân tử của Y biết tỉ khối hơi của Y so với H2 là 36,5. Tìm công thức phân tử của Y ?
Y + O2 --> CO2 + H2O + N2
Cho sản phẩm cháy vào bình đựng Ca(OH)2 thì nito không bị hấp thụ, thoát ra khỏi bình . Khối lượng bình tăng = mCO2 + mH2O
nCO2 = nCaCO3 = 80/100 = 0,8 mol
=> mH2O = 55 - 0,8.44 = 19,8 gam
<=> nH2O = 19,8/18 = 1,1 mol
nN2 = 2,24/22,4 = 0,1 mol
mC + mH + mN = 0,8.12 + 1,1.2 + 0,2.14 = 14,6gam = mY
=> Trong Y có C; H và N , không có O
Gọi CTĐGN của Y là CxHyNz => x:y:z = nC:nH:nN = 0,8 : 2,2 : 0,2 = 4:11:1
=> CTPT của Y có dạng (C4H11N)n
MY = 36,5 .2 = 73(g/mol) => 73n = n
<=> n = 1 và CTPT của Y là C4H11N
Đúng 4
Bình luận (0)
20. Đốt cháy hoàn toàn 15g một hợp chất hữu cơ chứa ( C,H,O,N) bằng V lít ko khí vừa đủ ( 80% N2 , 20% O2 về thể tích). Dẫn toàn bộ sản phẩm cháy lần lượt lội qua bình đựng dd H2SO4 đặc , bình 2 đựng dd Ca(OH)2 dư thì còn lại 42,56 lít một khí X ko bị hấp thụ . Biết rằng khối lượng bình 1 tăng thêm 9 gam , khối lượng bình 2 tăng thêm 17,6g . Công thức đơn giản nhất của hợp chất trên là?
Đọc tiếp
20. Đốt cháy hoàn toàn 15g một hợp chất hữu cơ chứa ( C,H,O,N) bằng V lít ko khí vừa đủ ( 80% N2 , 20% O2 về thể tích). Dẫn toàn bộ sản phẩm cháy lần lượt lội qua bình đựng dd H2SO4 đặc , bình 2 đựng dd Ca(OH)2 dư thì còn lại 42,56 lít một khí X ko bị hấp thụ . Biết rằng khối lượng bình 1 tăng thêm 9 gam , khối lượng bình 2 tăng thêm 17,6g . Công thức đơn giản nhất của hợp chất trên là?
Đốt cháy hoàn toàn amin đơn chức E bằng khí
O
2
vừa đủ. Dẫn toàn bộ sản phẩm cháy (gồm
C
O
2
,
H
2
O
và
N
2
) qua bình đựng dung dịch
B
a
(
O
H
)
2
dư, khối lượ...
Đọc tiếp
Đốt cháy hoàn toàn amin đơn chức E bằng khí O 2 vừa đủ. Dẫn toàn bộ sản phẩm cháy (gồm C O 2 , H 2 O và N 2 ) qua bình đựng dung dịch B a ( O H ) 2 dư, khối lượng bình tăng 7,78 gam và có 27,58 gam kết tủa; chất khí thoát ra khỏi bình có thể tích 0,224 lít (đktc). Công thức phân tử của E là
A. C 6 H 7 N
B. C 2 H 7 N
C. C 3 H 9 N
D. C 7 H 9 N
Đốt cháy hoàn toàn hợp chất hữu cơ Y cần dùng 16,8(lit) O2 thu được CO2, H2O ,N2 . Cho hoàn toàn sản phẩm thu được qua dung dịch Ca(OH)2 dư thu được 60g kết tủa đồng thời khối lượng bình giảm 21g và có 2,24(lit) khí thoát ra khỏi bình (đktc).
Tìm công thức phân tử của Y biết công thức phân tử trùng với công thức đơn giản nhất.
\(Đăt:n_{CO_2}=a\left(mol\right),n_{H_2O}=b\left(mol\right)\)
\(BTNTO:\\ 2n_{O_2}=2n_{CO_2}+n_{H_2O}\\ \Leftrightarrow2a+b=0.75\left(1\right)\)
\(m_{bìnhgiảm}=m_{CaCO_3}-\left(m_{CO_2}+m_{H_2O}\right)=21\left(g\right)\)
\(\Leftrightarrow44a+18b=60-21=39\left(g\right)\left(2\right)\)
Bạn xem lại đề nha
Đúng 1
Bình luận (0)
\(n_{CO_2} = n_{CaCO_3} = 0,6(mol)\)
\(m_{tăng} = n_{CO_2} + m_{H_2O} - m_{CaCO_3}\\ \Rightarrow n_{H_2O} = \dfrac{60-21-0,6.44}{18} = 0,7(mol)\)
\(n_{N_2} = n_{khí\ thoát\ ra} = 0,1(mol)\)
\(n_{O_2} =0,75(mol)\)
BTNT với C,H,O và N :
\(n_C = n_{CO_2} = 0,6\\ n_H = 2n_{H_2O} = 0,7.2 = 1,4(mol)\\ n_N = 2n_{N_2} = 0,2(mol)\\ n_O = 2n_{CO_2} + n_{H_2O} -2n_{O_2}= 0,4(mol)\)
Ta có :
\(n_C : n_H : n_O : n_N = 0,6 : 1,4 : 0,4 : 0,2 = 3 : 7 :2 : 1\)
Vậy CTPT của Y :C3H7O2N
Đúng 1
Bình luận (0)