Dung dịch Ba(OH)2 có pH=13, dung dịch HNO3 có pH=1.
a) Phải trộn chúng theo thể tích là bao nhiêu để thu được dung dịch trung tính.
b) Khi trộn 2,75 lít dung dịch Ba(OH)2 với 2,25 lít dung dịch HNO3. Tính nồng độ mol của dung dịch thu được.
Help me
Dung dịch Ba(OH)2 có pH=13 (ddA), dung dịch HCl có pH=1 (dd B). Trộn 2,75 lít A với 2,25 lít dd B. Nồng độ mol/l của các chất có trong dung dịch sau phản ứng là:
A. 0,0225M; 5.10-3M
B. 0,1125M; 0,025M
C. 0,02M; 5.10-3M
D. 0,1125M; 0,02M
Đáp án A
nOH- = 2,75.10-1 = 0,275 mol; nH+ = 2,25.10-1 = 0,225 mol
H+ + OH- → H2O
0,225 0,275
nOH- dư = 0,05 mol; nCl- = nHCl = 0,225 mol; nBa2+ = 0,1375 mol
Dung dịch sau phản ứng có chứa BaCl2: 0,1125 mol; Ba(OH)2 dư 0,025 mol
Nồng độ mol của BaCl2 là 0,1125/5 = 0,0225M
Nồng độ mol của Ba(OH) 2 dư là 0,025/5 = 5.10-3M
Dung dịch A gồm HCl 0,2M ; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M, Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH=13?
A. 11:9
B. 9:11
C. 101:99
D. 99:101
Đáp án A
Gọi thể tích dung dịch A là V1 lít. Có nH+ = ( 0,2+0,3+0,1.2+0,3).V1 = V1 mol
Gọi thể tích dung dịch B là V2 lít. Có nOH- = ( 0,3+ 0,4+ 0,15.2).V2 = V2 mol
H+ + OH- → H2O
V1 V2
Dung dịch thu được có pH = 13 nên OH- dư
nOHdư = V2- V1 mol
[OH-]dư = (V2-V1)/(V2+ V1) = 10-1 suy ra V1: V2 = 11:9
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9.
B. 9 : 11.
C. 101 : 99.
D. 99 : 101.
Chọn B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
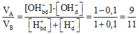
Dung dịch A gồm HCl 0,2M; HNO3 0,3M; H2SO4 0,1M; HClO4 0,3M, dung dịch B gồm KOH 0,3M; NaOH 0,4M; Ba(OH)2 0,15M. Cần trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch có pH = 13?
A. 11 : 9
B. 9 : 11
C. 101 : 99
D. 99 : 101
Đáp án B.
Nồng độ H+ ban đầu là: (0,2 + 0,3 + 0,1.2 + 0,3) = 1M.
Nồng độ OH- ban đầu là: (0,3 + 0,4 + 0,15.2) = 1M.
Dung dịch sau phản ứng có pH = 13, suy ra OH- dư, pOH = 1.
Nồng độ OH- dư là: 10-1 = 0,1M.
Áp dụng sơ đồ đường chéo cho trường hợp OH- dư, ta được:
VA/VB = (1-0,1)/(1+0,1) = 9/11
Câu 8. a. Cho 220ml dung dịch HCl có pH = 5 tác dụng với 180ml dung dịch NaOH có pH = 9 thì thu được dung dịch A. Tính pH của dung dịch A. b. Cho 2,75 lít dung dịch Ba(OH)2 có pH = 13 tác dụng với 2,25 lít
a, \(\left[H^+\right]=10^{-5}\Rightarrow n_{H^+}=0,22.10^{-5}\left(mol\right)\)
\(\left[OH^-\right]=10^{-5}\Rightarrow n_{OH^-}=0,18.10^{-5}\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=0,04.10^{-5}=4.10^{-7}\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{4.10^{-7}}{0,22+0,18}=10^{-8}\)
\(\Rightarrow pH=8\)
Giá trị pH của 1 lít dung dịch chứa 0,05 mol NaOH và 0,025 mol Ba(OH)2 là
A.12 B. 2 C. 13 D.1
2. Khi trộn những thể tích bằng nhau của dung dịch HNO3 0,04M và dung dịch Ba(OH)2 0,03M thì thu được dung dịch có giá trị pH bằng
A. 9. B. 12,3 C. 13 D.12
3. Trộn 400 ml dung dịch chứa Ba(OH)2 và NaOH có pH = 13 với 200 ml dung dịch gồm H2SO4 0,1M và HCl 0,03M thu được dung dịch X. Giá trị pH của dung dịch X là
A.12 B. 2 C. 13 D.1
Một dung dịch chứa a mol Al3+; 0,2 mol Mg2+; 0,2 mol Na + 0,4 mol Cl- và b mol SO42-. Tổng khối lượng muối có trong dung dịch là 50,3 gam. Giá trị của a và b lần lượt là
A. 0,06 và 0,19. B. 0,30 và 0,55. C. 0,20 và 0,40. D. 0,10 và 0,25
Một dung dịch chứa a mol Ca2+; b mol Mg2+; b mol Fe2+; 0,4 mol Cl- và 0,6 mol NO3-. Khối lượng chất tan trong dung dịch là
A. 91,4. B. 75,4. C. 67,4. D. 71,4
Trộn 120 ml dung dịch H2SO4 0,09M và HNO3 0,125M với 280 ml dung dịch NaOH và Ca(OH)2 có pH=13 thu dung dịch X. Giá trị pH của dung dịch X là
A. 1,67. B. 12,84. C. 1,56. D. 12,33
Dung dịch chất nào sau đây không làm đổi màu quỳ tím?
A. Ba(NO3)2 B. Ca(OH)2 C. H2S D. CH3COOH
Trộn 200 ml dung dịch gồm Ba(OH)2 0,16M và KOH 0,2M với 200 ml dung dịch gồm H2SO4 0,18M và HCl 0,15M thu được dung dịch X. Giá trị pH của dung dịch X là
A. 11,7 B. 2,3 C. 2,22 D. 12,18
Chất nào sau đây là hiđroxit lưỡng tính
A. Fe(OH)2 B. Mg(OH)2 C. NaHCO3 D. Zn(OH)2
Giá trị pH của 1 lít dung dịch chứa 0,05 mol NaOH và 0,025 mol Ba(OH)2 là
A.12 B. 2 C. 13 D.1
2. Khi trộn những thể tích bằng nhau của dung dịch HNO3 0,04M và dung dịch Ba(OH)2 0,03M thì thu được dung dịch có giá trị pH bằng
A. 9. B. 12,3 C. 13 D.12
3. Trộn 400 ml dung dịch chứa Ba(OH)2 và NaOH có pH = 13 với 200 ml dung dịch gồm H2SO4 0,1M và HCl 0,03M thu được dung dịch X. Giá trị pH của dung dịch X là
A.12 B. 2 C. 13 D.1
Một dung dịch chứa a mol Al3+; 0,2 mol Mg2+; 0,2 mol Na + 0,4 mol Cl- và b mol SO42-. Tổng khối lượng muối có trong dung dịch là 50,3 gam. Giá trị của a và b lần lượt là
A. 0,06 và 0,19. B. 0,30 và 0,55. C. 0,20 và 0,40. D. 0,10 và 0,25
Một dung dịch chứa a mol Ca2+; b mol Mg2+; b mol Fe2+; 0,4 mol Cl- và 0,6 mol NO3-. Khối lượng chất tan trong dung dịch là
A. 91,4. B. 75,4. C. 67,4. D. 71,4
Trộn 120 ml dung dịch H2SO4 0,09M và HNO3 0,125M với 280 ml dung dịch NaOH và Ca(OH)2 có pH=13 thu dung dịch X. Giá trị pH của dung dịch X là
A. 1,67. B. 12,84. C. 1,56. D. 12,33
Dung dịch chất nào sau đây không làm đổi màu quỳ tím?
A. Ba(NO3)2 B. Ca(OH)2 C. H2S D. CH3COOH
Trộn 200 ml dung dịch gồm Ba(OH)2 0,16M và KOH 0,2M với 200 ml dung dịch gồm H2SO4 0,18M và HCl 0,15M thu được dung dịch X. Giá trị pH của dung dịch X là
A. 11,7 B. 2,3 C. 2,22 D. 12,18
Chất nào sau đây là hiđroxit lưỡng tính
A. Fe(OH)2 B. Mg(OH)2 C. NaHCO3 D. Zn(OH)2
Cặp chất nào sau đây tạo thành chất điện li yếu
A. HCl + AgNO3 B. H2SO4 + Ba(NO)2
C. HNO3+NaOH D. NaOH+CuCl2
Trộn 100 ml dung dịch HNO3 1M với 50 ml dung dịch Ba(OH)2 1M thu được dung dịch có pH bằng bao nhiêu?
A. 0
B. 1
C. 7
D. 14
Đáp án C
Do nH+= nOH-= 0,1 mol nên dung dịch thu được có pH=7
Một dung dịch A chứa Ba(OH)2 có pH=13 trộn lẫn với dung dịch B chứa HCl có pH=2. Khi phản ứng xong thu được dung dịch C có pH=12. a) Tính tỉ lệ thể tích của dung dịch A với dung dịch B, cho biết sự trộn lẫn dung dịch không làm thay đổi thể tích dung dịch. b) Hỏi sau khi cô cạn 550 ml dung dịch C thì thu được bao nhiêu gam chất rắn khan, tính % khối lượng chất rắn khan
a, \(n_{OH^-}=10^{-1}.V_A\left(mol\right)\)
\(n_{H^+}=10^{-2}.V_B\left(mol\right)\)
\(n_{OH^-dư}=10^{-2}.\left(V_A+V_B\right)\left(mol\right)\)
Ta có: \(n_{OH^-}-n_{OH^-dư}=n_{H^+}\)
\(\Leftrightarrow10^{-1}.V_A-10^{-2}.\left(V_A+V_B\right)=10^{-2}.V_B\)
\(\Leftrightarrow0,09V_A=0,02V_B\)
\(\Rightarrow\dfrac{V_A}{V_B}=\dfrac{2}{9}\)
b, Ta có: \(\left\{{}\begin{matrix}V_A+V_B=0,55\\\dfrac{V_A}{V_B}=\dfrac{2}{9}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}V_A=0,1\left(l\right)\\V_B=0,45\left(l\right)\end{matrix}\right.\)
\(n_{BaCl_2}=\dfrac{1}{2}n_{Cl^-}=\dfrac{1}{2}n_{H^+}=\dfrac{1}{2}.10^{-2}.0,1=0,0005\left(mol\right)\Rightarrow m_{BaCl_2}=0,104\left(g\right)\)
\(n_{Ba\left(OH\right)_2}=\dfrac{1}{2}n_{OH^-dư}=\dfrac{1}{2}.10^{-2}.0,55=0,00275\left(mol\right)\Rightarrow m_{Ba\left(OH\right)_2}=0,047025\left(g\right)\)
\(\Rightarrow\%m_{Ba\left(OH\right)_2}=\dfrac{0,047025}{0,047025+0,104}.100\%=31,14\%\)
\(\Rightarrow\%m_{BaCl_2}=62,86\%\)