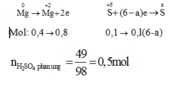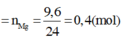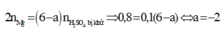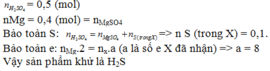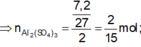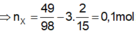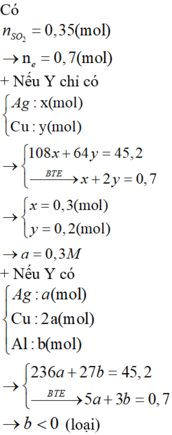Bài 1. Khi cho 9.6g Mg tác dụng hết với dung dịch H2SO4 đặc thấy có 49g H2SO4 than gia phản ứng tạo muối MgSO4,H2O và sản phẩm khử X. X là?
Bài2.cho hỗn hợp A gồm Cu và Mg vào dung dịch HCl dư thu được 5.6l khí đktc không màu và một chất rắn không tan B.dùng dung dịch H2SO4 đặc nóng để hòa tan chất rắn B thu được 2.24l khí SO2 đktc. Khối lượng hh A ban đầu là?