cho 11,2g Fe tác dụng với 3,2g S đun nóng , Tính Vml HCL 2M hòa tan chất rắn sau phản ứng

Những câu hỏi liên quan
Cho 11,2g Fe phản ứng với 3,2g S và đun nóng thu được hỗn hợp A. Hòa tan hỗn hợp A vào dung dịch H_2SO_4 (đ) 98% và đun nóng thu được khí B (đktc) và dung dịch Ca) Viết các ptb) Tính m_{ddH_2SO_4}c) Tính thể tích khí B (đktc)d) Cho dung dịch C phản ứng với dung dịch Baleft(OHright)_2. Lọc kết tủa dun trong không khí đến khối lượng không đổi thu được chất rắn D. Tính khối lượng dung dịch của D
Đọc tiếp
Cho 11,2g Fe phản ứng với 3,2g S và đun nóng thu được hỗn hợp A. Hòa tan hỗn hợp A vào dung dịch \(H_2SO_4\) (đ) 98% và đun nóng thu được khí B (đktc) và dung dịch C
a) Viết các pt
b) Tính \(m_{ddH_2SO_4}\)
c) Tính thể tích khí B (đktc)
d) Cho dung dịch C phản ứng với dung dịch \(Ba\left(OH\right)_2\). Lọc kết tủa dun trong không khí đến khối lượng không đổi thu được chất rắn D. Tính khối lượng dung dịch của D
\(Fe+S\rightarrow FeS\left(1\right)\)
TPT: 1 1 1 (mol)
TĐB: 0,2 0,2 0,2 (mol)
PƯ: 0,1 0,1 0,1 (mol)
Dư: 0,1 0 0 (mol)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
Tỉ lệ: \(\dfrac{n_{Fe}}{1}=\dfrac{0,2}{1}>\dfrac{n_S}{1}=\dfrac{0,1}{1}\)
Vậy hỗn hợp A gồm FeS và 0,1 mol Fe
\(2Fe_{\left(dư\right)}+6H_2SO_{4\left(đ,t^0\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\left(2\right)\)
TPT: 2 6 1 3 (mol)
TĐB: 0,1 0,3 0,05 0,15 (mol)
\(2FeS+10H_2SO_{4\left(đ,t^0\right)}\rightarrow Fe_2\left(SO_4\right)_3+9SO_2+10H_2O\left(3\right)\)
TPT: 2 10 1 9 10 (mol)
TĐB: 0,1 0,5 0,05 0,5 0,45 (mol)
\(m_{H_2SO_{4\left(1+2\right)}}=n.M\left(0,3+0,5\right).98=78,4\left(g\right)\)
\(m_{ddH_2SO_4}=\dfrac{m_{ct}.100\%}{C\%}=\dfrac{78,4.100\%}{98\%}=80\left(g\right)\)
c) \(V_{SO_{2\left(2+3\right)}}=n.22,4=\left(0,15+0,45\right).22,4=13,44\left(l\right)\)
d) \(Fe_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow2Fe\left(OH\right)_3+3BaSO_4\left(4\right)\)
TPT: 1 3 2 3 (mol)
TĐB: 0,1 0,3 0,2 0,3 (mol)
\(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\left(5\right)\)
TPT: 2 1 3 (mol)
TĐB: 0,2 0,1 0,3 (mol)
\(m_{Fe_2O_3}=n.M=0,1.160=16\left(g\right)\)
Đúng 4
Bình luận (0)
Đun nóng hh gồm 16,8g Fe và 3,2g S trong bình kín không có không khí thu được chất rắn A. Hòa tan A trong 0,5 lít dd HCl nồng độ x (mol/lít) dư thu được hh khí B và dd C
a) Tính % thể tích các khí trong B
b) Trung hòa HCl dư cần 100ml NaOH 2M. Tính CM của HCl đã dùng
(mk lm vt lại đầu bài😊😊)
a, PT: \(Fe+S\underrightarrow{t^o}FeS\)
Ta có: \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
\(n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,1}{1}\), ta được Fe dư.
Chất rắn A gồm Fe dư và FeS.
Theo PT: \(n_{Fe\left(pư\right)}=n_{FeS}=n_S=0,1\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2}=n_{Fe\left(dư\right)}=0,2\left(mol\right)\\n_{H_2S}=n_{FeS}=0,1\left(mol\right)\end{matrix}\right.\)
Ở cùng điều kiện nhiệt độ và áp suất, %V cũng là % số mol.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,2}{0,2+0,1}.100\%\approx66,67\%\\\%V_{H_2S}\approx33,33\%\end{matrix}\right.\)
b, Ta có: \(\Sigma n_{HCl\left(dadung\right)}=2n_{Fe}+2n_{FeS}=0,6\left(mol\right)\) (1)
PT: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Ta có: \(n_{NaOH}=0,1.2=0,2\left(mol\right)\)
\(\Rightarrow n_{HCl\left(dư\right)}=n_{NaOH}=0,2\left(mol\right)\) (2)
Từ (1) và (2) \(\Rightarrow\Sigma n_{HCl}=0,8\left(mol\right)\)
\(\Rightarrow C_{M_{ddHCl}}=\dfrac{0,8}{0,5}=1,6\left(M\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Đun nóng hỗn hợp Fe và S có khối lượng m (g) sau khi phản ứng kết thúc thu được chất rắn, hòa tan chất rắn trong HCl (dư) thu được 4,47l khí. Dẫn toàn bộ chất khí này vào dd Chì(ll)nitrat thu được 23,9g và thoát ra 1 chất khí. Xác định m
\(H_2S + Pb(NO_3)_2 \to PbS + 2HNO_3\\ n_{H_2S} = n_{PbS} = \dfrac{23,9}{239} = 0,1(mol)\\ \Rightarrow n_{H_2} = \dfrac{4,48}{22,4} - 0,1 = 0,1(mol)\\ Fe + 2HCl \to FeCl_2 + H_2\\ FeS + 2HCl \to FeCl_2 + H_2S\\ Fe + S \xrightarrow{t^o} FeS\\ n_{Fe} = n_{Fe} + n_{FeS} = n_{H_2} + n_{H_2S} = 0,2(mol)\\ n_S = n_{FeS} = n_{H_2S} = 0,1(mol)\\ \Rightarrow m = 0,2.56 + 0,1.32 = 14,4(gam) \)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 8,8g hỗn hợp 2 kim loại Cu,Fe vào dung dịch HCl dư, sau phản ứng thấy còn lại 3,2g chất rắn không tan và có V lít khí ko màu(đktc) thoát ra.Xác định giá trị của V
Còn 3,2g chất rắn không tan chính là khối lượng Cu.
\(m_{Cu}=3,2g\Rightarrow m_{Fe}=8,8-3,2=5,6g\)
\(\Rightarrow n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 8,8g hỗn hợp 2 kim loại Cu,Fe vào dung dịch HCl dư, sau phản ứng thấy còn lại 3,2g chất rắn không tan và có V lít khí ko màu(đktc) thoát ra.Xác định giá trị của V
\(m_{rắn}=m_{Cu}=3,2\left(g\right)\\ \Rightarrow m_{Fe}=8,8-3,2=5,6\left(g\right)\\ \Rightarrow n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
Ta có chất ko tan là Cu
=>m Fe=8,8-3,2=5,6g
=>n Fe=\(\dfrac{5,6}{56}\)=0,1 mol
Fe+HCl->FeCl2+H2
0,1---------------------0,1 mol
=>VH2=0,1.22,4=2,24l
Đúng 1
Bình luận (0)
đun nóng hỗn hợp gồm 16 8g bột fe và 6,4 g lưu huỳnh (điều kiện ko có kk)đến phản ứng hoàn toàn thu được chất rắn a hòa tan A bằng hcl thu đuộc hh khí B
Hòa tan hoàn toàn 6,5(g) Zn vào dung dịch HCl, ta thu được muối ZnCl2 và tháy có khí H2 thoát ra. Cho toàn bộ lượng khí H2 thu được qua 6(g) CuO đun nóng, sau phản ứng thu được 5,2(g) chất rắn. Tính hiệu suất phản ứng.
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.1.................................0.1\)
\(Đặt:n_{CuO\left(pư\right)}=x\left(mol\right)\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(x............x\)
\(m_{cr}=6-80x+64x=5.2\left(g\right)\)
\(\Rightarrow x=0.05\)
\(H\%=\dfrac{0.05}{0.075}\cdot100\%=66.67\%\)
Đúng 0
Bình luận (0)
Dẫn luồng khí H2 dư đi qua 39,2 gam hỗn hợp CuO và oxit sắt FexOy (chưa biết) đun nóng; sau phản ứng thu được 29,6 gam chất rắn A.a/ A gồm những chất gì? Tính thể tích H2 (đktc) đã phản ứng.b/ Hòa tan chất rắn A bằng dung dịch axit HCl dư, khi phản ứng kết thúc, thu được 6,72 lít khí H2 (đktc). - Xác định FexOy.- Tính khối lượng của mỗi oxit kim loại có trong hỗn hợp đầu.
Đọc tiếp
Dẫn luồng khí H2 dư đi qua 39,2 gam hỗn hợp CuO và oxit sắt FexOy (chưa biết) đun nóng; sau phản ứng thu được 29,6 gam chất rắn A.
a/ A gồm những chất gì? Tính thể tích H2 (đktc) đã phản ứng.
b/ Hòa tan chất rắn A bằng dung dịch axit HCl dư, khi phản ứng kết thúc, thu được 6,72 lít khí H2 (đktc).
- Xác định FexOy.
- Tính khối lượng của mỗi oxit kim loại có trong hỗn hợp đầu.
a) A gồm Cu, Fe
\(n_O=\dfrac{39,2-29,6}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\)
=> \(n_{H_2}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b)
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_xO_y}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + b(56x + 16y) = 39,2
=> 80a + 56bx + 16by = 39,2 (1)
nO = 0,6 (mol)
=> a + by = 0,6
=> 80a + 80by = 48 (2)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,3<-------------------0,3
=> nFe = bx = 0,3 (mol)
(2) - (1) => 64by - 56bx = 8,8
=> by = 0,4
Xét \(\dfrac{bx}{by}=\dfrac{x}{y}=\dfrac{0,3}{0,4}=\dfrac{3}{4}\)
=> CTHH: Fe3O4
Có: \(\left\{{}\begin{matrix}80a+232b=39,2\\a+4b=0,6\end{matrix}\right.\)
=> a = 0,2; b = 0,1
=> \(\left\{{}\begin{matrix}m_{CuO}=0,2.80=16\left(g\right)\\m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là A. 22,44 B. 28,0 C. 33,6 D. 25,2
Đọc tiếp
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là
A. 22,44
B. 28,0
C. 33,6
D. 25,2
Chọn đáp án B
Ta có
![]()
=0,2
![]()
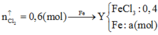
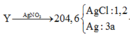
![]()
=>a=0,1(mol)
![]()
Đúng 0
Bình luận (0)























