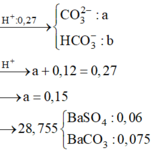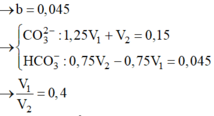cho 6 5 g zn tác dụng với v1 ml dung dịch hcl 1m thu được m (g) zncl2và v2 l khí h2 (đktc)

Những câu hỏi liên quan
Hòa tan m gam Fe vào 300 ml dung dịch H2SO4 0,5M thu được dung dịch X và V1 lít H2 ở đktc. Cho dung dịch X tác dụng vừa đủ với V2 ml dung dịch Ba(OH)2 1M thu được 41,7 gam kết tủa. Tính m, V1, V2.
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(FeSO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+Fe\left(OH\right)_2\downarrow\)
Ta có: \(n_{H_2SO_4}=0,3\cdot0,5=0,15\left(mol\right)=n_{Fe}=n_{H_2}=n_{Ba\left(OH\right)_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,15\cdot56=8,4\left(g\right)\\V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\\V_{Ba\left(OH\right)_2}=\dfrac{0,15}{1}=0,15\left(l\right)=150\left(ml\right)\end{matrix}\right.\)
*Bạn xem lại đề vì nếu FeSO4 p/ứ hết thì sẽ có nhiều hơn 41,7 gam kết tủa
Đúng 0
Bình luận (1)
Cho 13 gam Zn tác dụng vừa đủ với V1 lít dung dịch HCl 0,5M thu được dung dịch X và V2 lít khí H2 đo ở đktc.a. Tính giá trị của V1 và V2?b. Tính nồng độ mol dung dịch X?c. Cho 1/2 lượng khí H2 trên qua 32 gam bột CuO nung nóng thu được m gam hỗn hợp chất rắn Y. Biết các phản ứng xảy ra hoàn toàn, giá trị của m là?
Đọc tiếp
Cho 13 gam Zn tác dụng vừa đủ với V1 lít dung dịch HCl 0,5M thu được dung dịch X và V2 lít khí H2 đo ở đktc.
a. Tính giá trị của V1 và V2?
b. Tính nồng độ mol dung dịch X?
c. Cho 1/2 lượng khí H2 trên qua 32 gam bột CuO nung nóng thu được m gam hỗn hợp chất rắn Y. Biết các phản ứng xảy ra hoàn toàn, giá trị của m là?
a)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2--->0,4---->0,2--->0,2
\(V_2=0,2.22,4=4,48\left(l\right)\)
\(V_1=\dfrac{0,4}{0,5}=0,8\left(l\right)\)
b)
\(C_{M\left(ZnCl_2\right)}=\dfrac{0,2}{0,8}=0,25M\)
c)
\(n_{H_2}=0,1\left(mol\right)\); \(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,1}{1}\) => CuO dư, H2 hết
PTHH: CuO + H2 --to--> Cu + H2O
0,1<--0,1------>0,1
=> m = 32 - 0,1.80 + 0,1.64 = 30,4 (g)
Đúng 2
Bình luận (0)
Dung dịch X chứa K2CO3 0,6M và KHCO3 0,4M. Nhỏ từ từ V1 ml dung dịch X vào V2 ml dung dịch HCl 1M, sau các phản ứng, thu được dung dịch Y. Cho Y tác dụng hết với dung dịch nước vôi trong dư, thu được a mol kết tủa. Mặt khác, nhỏ từ từ V2 ml dung dịch HCl 1M vào V1 ml dung dịch X, sau các phản ứng, thu được 2,4a mol CO2. Tỉ lệ V1 : V2 là A. 5:8. B. 4:5. C. 5:6. D. 8:5.
Đọc tiếp
Dung dịch X chứa K2CO3 0,6M và KHCO3 0,4M. Nhỏ từ từ V1 ml dung dịch X vào V2 ml dung dịch HCl 1M, sau các phản ứng, thu được dung dịch Y. Cho Y tác dụng hết với dung dịch nước vôi trong dư, thu được a mol kết tủa. Mặt khác, nhỏ từ từ V2 ml dung dịch HCl 1M vào V1 ml dung dịch X, sau các phản ứng, thu được 2,4a mol CO2. Tỉ lệ V1 : V2 là
A. 5:8.
B. 4:5.
C. 5:6.
D. 8:5.
Dung dịch X chứa Na2CO3 0,5M và NaOH 0,75M; dung dịch Y chứa KHCO3 0,75M và K2CO3 1M. Trộn V1 lít dung dịch X với V2 lít dung dịch Y thu được dung dịch Z chỉ chứa các muối. Cho từ từ đến hết 200 ml dung dịch HCl 0,75M và H2SO4 0,3M vào dung dịch Z thu được 2,688 lít khí CO2 (đktc) và dung dịch G. Cho Ba(OH)2 dư vào dung dịch G thu được 28,755 gam kết tủa. Tỉ lệ V1 : V2 là A. 0,6 B. 0,5 C. 0,4 D. 0,75
Đọc tiếp
Dung dịch X chứa Na2CO3 0,5M và NaOH 0,75M; dung dịch Y chứa KHCO3 0,75M và K2CO3 1M. Trộn V1 lít dung dịch X với V2 lít dung dịch Y thu được dung dịch Z chỉ chứa các muối. Cho từ từ đến hết 200 ml dung dịch HCl 0,75M và H2SO4 0,3M vào dung dịch Z thu được 2,688 lít khí CO2 (đktc) và dung dịch G. Cho Ba(OH)2 dư vào dung dịch G thu được 28,755 gam kết tủa. Tỉ lệ V1 : V2 là
A. 0,6
B. 0,5
C. 0,4
D. 0,75
Cho 17,2 g hỗn hợp X gồm Al,Zn,Mg,Fe tác dụng với dung dịch Hcl dư thu V1 (lít) H2. Mặt khác để õi hóa hoàn toàn 17,2 g hỗn hợp X cần V2(lít) Cl2. Biết V2-V1=2,016.,các khí đều đo đktc.Tính phần trăm kl của Fe trong hỗn hợp X?
*Cho hỗn hợp tác dụng với HCl:
3nAl + 2nZn + 2nMg + 2nFe = 2* (V1/22,4) (1)
*Cho hỗn hợp tác dụng với Cl2:
3nAl + 2nZn + 2nMg + 3nFe = 2* (V2/22,4) (2)
(2) - (1) ta được nFe = 2* [(V2 - V1)/22,4] = 0,18 (mol)
%mFe/X = (0,18*56) / 17,2 = 58,60%
Đúng 0
Bình luận (0)
Cho 27,3 gam hỗn hợp X gồm Zn, Fe và Cu tác dụng với 260 ml dung dịch CuCl2 1M, thu được 28,48 gam chất rắn Y và dung dịch Z. Cho toàn bộ Y tác dụng với dung dịch HCl dư thu được 0,896 lít khí H2 (đktc). Cho Z tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 17,12. B. 14,08. C. 12,80. D. 20,90.
Đọc tiếp
Cho 27,3 gam hỗn hợp X gồm Zn, Fe và Cu tác dụng với 260 ml dung dịch CuCl2 1M, thu được 28,48 gam chất rắn Y và dung dịch Z. Cho toàn bộ Y tác dụng với dung dịch HCl dư thu được 0,896 lít khí H2 (đktc). Cho Z tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 17,12.
B. 14,08.
C. 12,80.
D. 20,90.
Cho 27,3 gam hỗn hợp X gồm Zn, Fe và Cu tác dụng với 260 ml dung dịch CuCl2 1M, thu được 28,48 gam chất rắn Y và dung dịch Z. Cho toàn bộ Y tác dụng với dung dịch HCl dư thu được 0,896 lít khí H2 (đktc). Cho Z tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 17,12. B. 14,08. C. 12,80. D. 20,90.
Đọc tiếp
Cho 27,3 gam hỗn hợp X gồm Zn, Fe và Cu tác dụng với 260 ml dung dịch CuCl2 1M, thu được 28,48 gam chất rắn Y và dung dịch Z. Cho toàn bộ Y tác dụng với dung dịch HCl dư thu được 0,896 lít khí H2 (đktc). Cho Z tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 17,12.
B. 14,08.
C. 12,80.
D. 20,90.
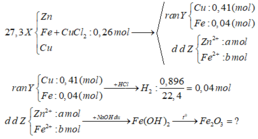
Các phản ứng xảy ra hoàn toàn, rắn Y + HCl giải phóng khí H2 => rắn Y gồm Cu và Fe dư
BT e : nFe dư = nH2 = 0,04 (mol)

Đáp án C
Đúng 0
Bình luận (0)
Cho 0,72 g một kim loại M tác dụng hết với dung dịch HCL dư thu được 672 ml khí H2 đktc . Xác định tên kim loại đó
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: 2M + 2nHCl → 2MCln + nH2
Mol: \(\dfrac{0,06}{n}\) 0,03
\(M_M=\dfrac{0,72}{\dfrac{0,06}{n}}=12n\)
Do M là kim loại nên có hóa trị I,ll,lll
| n | l | ll | lll |
| MM | 12 | 24 | 36 |
| Kết luận | loại | thỏa mãn | loại |
⇒ M là magie (Mg)
Đúng 3
Bình luận (0)
Câu 4: Cho m gam Fe vào 500 ml dung dịch HCl, phản ứng xảy ra vừa đủ thu được 3,36 lit khí H2 (Đktc). Tính m g Fe? Và CM của HCl
Câu 5: cho 8,3 gam hỗn hợp kim loại Fe, Al tác dụng với 500ml dung dịch HCl vừa đủ thu được 5,6 lit khí Hidro (Đktc). Xác định thành phần % mỗi kim loại trong hỗn hợp ban đầu
\(4.\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15.....0.3....................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.5}=0.6\left(M\right)\)
\(5.\)
\(Đặt:n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow a+1.5b=0.25\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%Fe=\dfrac{5.6}{8.3}\cdot100\%=67.47\%\)
\(\%Al=32.53\%\)
Đúng 2
Bình luận (1)