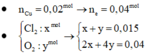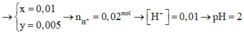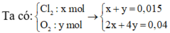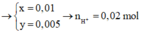Điện phân 200 ml dung dịch CuSO4 với I = 1,93 A tới khi catot bắt đầu có bọt khí thoát ra thì dừng lại, cần thời gian là 250 giây. Thể tích khí thu được ở anot (đktc) là

Những câu hỏi liên quan
Điện phân 200 ml dung dịch C u S O 4 với I = 1,93 A tới khi catot bắt đầu có bọt khí thoát ra thì dừng lại, cần thời gian là 250 giây. Thể tích khí thu được ở anot (đktc) là
A. 28 ml
B. 14 ml
C. 56 ml
D. 42 ml
Điện phân 200 ml dung dịch CuSO4 với I = 1,93 A tới khi catot bắt đầu có bọt khí thoát ra thì dừng lại, cần thời gian là 250 giây. Thể tích khí thu được ở anot (đktc) là
Tới khi catot có bọt khí (H2), CuSO4 đã bị điện phân hết vì khi đó nước bị điện phân. Khí thoát ra ở anot khi điện phân CuSO4 là O2.
\(CuSO_4+H_2O\underrightarrow{^{đpdd}}Cu+H_2SO_4+\frac{1}{2}O_2\)
Gọi x là mol Cu tạo thành
\(\Rightarrow64x=\frac{64.1,93.250}{2.96500}\)
\(\Rightarrow n_{Cu}=2n_{O2}=0,0025\left(mol\right)\)
\(\Rightarrow V_{O2}=\frac{0,0025.22,4}{2}=0,028\left(l\right)\)
Đúng 0
Bình luận (0)
Điện phân với điện cực trơ màng ngăn xốp dung dịch chứa 0,10 mol CuSO4 và 0,12 mol NaCl đến khi catot bắt đầu thoát khí thì dừng lại. Thể tích khí (dktc) thu được ở anot bằng : A. 1,792 B. 1,344 C. 0,448 D. 0,896
Đọc tiếp
Điện phân với điện cực trơ màng ngăn xốp dung dịch chứa 0,10 mol CuSO4 và 0,12 mol NaCl đến khi catot bắt đầu thoát khí thì dừng lại. Thể tích khí (dktc) thu được ở anot bằng :
A. 1,792
B. 1,344
C. 0,448
D. 0,896
Đáp án : A
Do ngừng đến khi catot xuất hiện khí nên :
Catot : Cu2+ + 2e à Cu
Anot : 2Cl- à Cl2 + 2e
2H2O 4H+ + O2 + 4e
Bảo toàn e : 2nCu2+ = nCl- + 4nO2 => nO2 = 0,02 mol
=> nkhí = nCl2 + nO2 = 0,08 mol => Vkhí = 1,792 lit
Đúng 0
Bình luận (0)
Dung dịch X chứa HCl,
C
u
S
O
4
,
F
e
2
(
S
O
4
)
. Lấy 400 ml dung dịch X đem điện phân với điện cực trơ, I 7,72A đến khi ở catot thu được 5,12 gam Cu thì dừng lại. Khi đó chỉ thu được 0,1 mol một chất khí duy nhất thoát ra ở anot. Thời gian điện phân và nồng độ [
F...
Đọc tiếp
Dung dịch X chứa HCl, C u S O 4 , F e 2 ( S O 4 ) . Lấy 400 ml dung dịch X đem điện phân với điện cực trơ, I = 7,72A đến khi ở catot thu được 5,12 gam Cu thì dừng lại. Khi đó chỉ thu được 0,1 mol một chất khí duy nhất thoát ra ở anot. Thời gian điện phân và nồng độ [ F e 2 + ] sau điện phân lần lượt là
A. 2300 s và 0,1M
B. 2500 s và 0,1 M
C. 2300 s và 0,15M
D. 2500 s và 0,15M
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là A. 12. B. 2. C. 13. D. 1.
Đọc tiếp
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là
A. 12.
B. 2.
C. 13.
D. 1.
Điện phân 2 lít dung dịch chứa hỗn hợp gồm NaCl và CuSO4 với điện cực trơ, có màng ngăn đến khi H2O bắt đầu điện phân ở cả hai cực thì dừng lại. Ở catot thu được 1,28 gam kim loại, đồng thời ở anot thu được 0,336 lít khí (đktc). Coi thể tích dung dịch không đổi, pH của dung dịch sau điện phân có giá trị là
A. 12
B. 2
C. 13
D. 1
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Giá trị của m là A. 50,87 gam. B. 53,42 gam. C. 55,34 gam. D. 53,85 gam.
Đọc tiếp
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Giá trị của m là
A. 50,87 gam.
B. 53,42 gam.
C. 55,34 gam.
D. 53,85 gam.
Đáp án C
Ở t giây ta thu được ở anot 0,12 mol hỗn hợp khí gồm Cl2 và O2.
Ở 2t giây ta thu được thể tích khí ở anot gấp 3 lần ở catot.
Goi số mol Cl2 và O2 ở t giây lần lượt là a, b
=> a+b=0,12
Bảo toàn e: n e = 2 a + 4 b
Lúc 2t giây: n e = 4 a + 8 b
Lúc này ở anot thu được Cl2 a mol và O2 → n O 2 = 4 a + 8 b - 2 a 4 = 0 , 5 a + 2 b
Do vậy ở catot thu được là H2 với số mol H2 = 0 , 5 a + 2 b + a 3 = 0 , 5 a + 2 b 3
Bảo toàn e:
n C u 2 + = 2 a + 4 ( 0 , 5 a + 2 b ) - 2 ( 0 , 5 a + 2 b 3 ) 2 = 1 , 5 a + 10 b 3 → 64 ( 1 , 5 a + 10 b 3 ) = 18 , 56
Giải hệ: a = b = 0,06 mol
Do vậy số mol KCl là 0,12 mol và CuSO4 là 0,29 mol.
m = 55,54 gam.
Đúng 0
Bình luận (0)
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KC1 bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Gia trị của m là: A. 55,34 gam B. 50,87 gam C. 53,42 gam D. 53,85 gam
Đọc tiếp
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KC1 bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Gia trị của m là:
A. 55,34 gam
B. 50,87 gam
C. 53,42 gam
D. 53,85 gam
Chọn đáp án A.
Đặt số mol của CuSO4 và KCl lần lượt là x, y.
Phương trình điện phân:
Catot: Cu2+ +2e → Cu
2H2O + 2e → 2OH- + H2
Anot: 2Cl- → Cl2 + 2e
2H2O → 4H+ + 4e + O2
Điện phân t giây:
0 , 5 y + n O 2 t = 2 , 688 22 , 4 = 0 , 12 m o l
⇒ n O 2 t = 0 , 12 - 0 , 5 y
=> nđiện phân = y + 4 . 0 , 12 - 0 , 5 y = 0 , 48 - y
Điện phân 2t giây:
nđiện phân = 2 . 0 , 48 - y mol
⇒ n O 2 2 t = 0 , 24 - 0 , 75 y mol
mcatot tăng = 64 x = 18 , 56 ⇒ x = 0 , 29
⇒ n H 2 = 019 - y
⇒ m = 160 x + 74 , 5 y = 55 , 34 g
Đúng 0
Bình luận (0)
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Giá trị của m là A. 50,87 gam. B. 53,42 gam. C. 55,34 gam. D. 53,85 gam.
Đọc tiếp
Điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, sau thời gian t giây, ở anot thoát ra 2,688 lít hỗn hợp khí (đktc). Nếu thời gian điện phân là 2t giây; thể tích khí thoát ra ở anot gấp 3 lần thể tích khí thoát ra ở catot (đo cùng điều kiện); đồng thời khối lượng catot tăng 18,56 gam. Giá trị của m là
A. 50,87 gam.
B. 53,42 gam.
C. 55,34 gam.
D. 53,85 gam.
Đáp án C
Ở t giây ta thu được ở anot 0,12 mol hỗn hợp khí gồm Cl2 và O2.
Ở 2t giây ta thu được thể tích khí ở anot gấp 3 lần ở catot.
Goi số mol Cl2 và O2 ở t giây lần lượt là a, b => a + b = 0,12
Bảo toàn e: n e = 2a + 4b
Lúc 2t giây: n e = 4a + 8b
Lúc này ở anot thu được Cl2 a mol và O2
Do vậy ở catot thu được là H2 với số mol H2
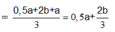
Bảo toàn e: n C u 2 +
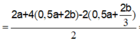
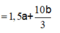
![]()
Giải hệ: a = b = 0,06 mol
Do vậy số mol KCl là 0,12 mol và CuSO4 là 0,29 mol.
m = 55,54 gam.
Đúng 0
Bình luận (0)