Đốt cháy 2,4 gam Mg bằng một lượng vừa đủ khí clo thu được magie clorua. Hòa tan magie clorua vào 190,5 gam nước. Nồng độ % của dung dịch thu được là
A. 4,750%.
B. 12,600%.
C. 0,0475%.
D. 0,1260%.
Câu 3: Hòa tan 2,4 gam Magie (Mg) vào 200 gam dung dịch axit clohiđric (HCl). Tính:
a) Nồng độ phần trăm dung dịch axit clohiđric đã dùng.
b) Khối lượng muối kẽm clorua thu được.
c) Thể tích khí hiđro thu được (đktc).
(Mg = 24 ; H = 1 ; Cl = 35,5)
C 4: Hòa tan 3,25 gam kẽm (Zn) vào 200 ml dung dịch axit clohiđric (HCl). Tính:
a) Nồng độ phần mol dung dịch axit clohiđric đã dùng.
b) Khối lượng muối kẽm clorua thu được.
c) Thể tích khí hiđro thu được (đktc).
(Zn = 65 ; H = 1 ; Cl = 35,5) ( Có lời giải và tóm tắt chi tiết em sẽ cho 5 sao )
Câu `3:`
`n_[Mg]=[2,4]/24=0,1(mol)`
`Mg + 2HCl -> MgCl_2 + H_2 \uparrow`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`a)C%_[HCl]=[0,2.36,5]/200 . 100=3,65%`
`b)m_[MgCl_2]=0,1.95=9,5(g)`
`c)V_[H_2]=0,1.22,4=2,24(l)`
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
Câu `4:`
`n_[Zn]=[3,25]/65=0,05(mol)`
`Zn + 2HCl -> ZnCl_2 + H_2 \uparrow`
`0,05` `0,1` `0,05` `0,05` `(mol)`
`a)C%_[HCl]=[0,1.36,5]/200 .100=1,825%`
`b)m_[ZnCl_2]=0,05.136=6,8(g)`
`c)V_[H_2]=0,05.22,4=1,12(l)`
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là:
A. 51,72%
B. 76,70%
C. 53,85%
D. 56,36%
Chọn C
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%
Hòa tan hết 6 gam magie (Mg) vào dung dịch axit clohiđric (HCl) thu được magie clorua (MgCl2) và khí hiđro (H2). a) Tính thể tích khí hiđro thu được ở đktc. b) Cho khí hiđro vừa thu được qua đồng (II) oxit (CuO) đun nóng thu được kim loại đồng (Cu) và nước (H2O). Xác định khối lượng đồng thu được.
\(n_{Mg}=\dfrac{6}{24}=0,25(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ a,n_{H_2}=n_{Mg}=0,25(mol)\\ \Rightarrow V_{H_2}=0,25.22,4=5,6(l)\\ b,PTHH:CuO+H_2\xrightarrow{t^o}Cu+H_2O\\ \Rightarrow n_{Cu}=n_{H_2}=0,25(mol)\\ \Rightarrow m_{Cu}=0,25.64=16(g)\)
3. Cho 2,4 gam magie tác dụng vừa đủ với dung dịch axit clohidric (HCl), thu được magie clorua (MgCl2) và khí hidro (H2) .
a. Tính khối lượng HCl đã dùng. c. Tính thể tích khí hidro thu được (đktc)
b. Tính khối lượng MgCl2
(Cho H = 1, Mg = 24, Cl = 35.5)
a) \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
_____0,1--->0,2------->0,1---->0,1
=> mHCl = 0,2.36,5 = 7,3(g)
b) mMgCl2 = 0,1.95 = 9,5 (g)
c) VH2 = 0,1.22,4 = 2,24(l)
pĐốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợ khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là
A. 51,72%
B. 53,85%
C. 56,36%
D. 76,70%
Đáp án : B
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích :
2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O
=> nO = 1 2 nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
Sau đó phản ứng với AgNO3 tạo :
(2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> % V C l 2 X = 53,85%
Đốt cháy hết 12gam kim loại magie (Mg) trong bình chứa đầy khí clo CL2, thu được 47,5 gam magie clorua MgCL2 A)viết công thức của phản ứng xảy ra B)tính khối lượng khí clo đã phản ứng
P/ứng hóa học: \(Mg+Cl_2->MgCl_2\)
Công thức của p/ứng có phải CT về khối lượng không nhỉ? Mình chưa hiểu lắm. Nếu là CT về kh lượng thì:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
* Khối lượng khí clo đã p/ứ:
Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\\ =>12g+m_{Cl_2}=47,5g\\ =>m_{Cl_2}=47,5g-12g=35,5g\)
Vậy có 35,5g khí Clo tham gia p/ứng.
Đốt cháy hỗn hợp gồm 2,6 gam Zn và 2,24 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 1M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 28,345 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là
A. 56,36%.
B. 51,72%.
C. 53,85%.
D. 76,70%.
Đáp án C
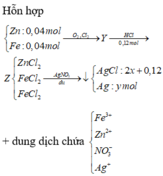
Khi tác dụng với HCl chỉ có các oxit bị hòa tan
→ nHCl = 4nO2 → nO2 = 0,03 mol
Gọi số mol của Cl2 và Ag lần lượt là x, y mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCL2 + nHCl = 2. x + 0,12
→ 143,5( 2. x + 0,12) + 108y = 28,345
Bảo toàn electron cho toàn bộ quá trình 3nFe + 2nZn = 2nCl2 + 4nO2 + nAg
→ 3. 0,04 + 2.0,04 = 2.x + 4. 0,03 + y
Giải hệ → x= 0,035 và y = 0,01
![]()
Đốt cháy hỗn hợp gồm 2,6 gam Zn và 2,24 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 1M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 28,345 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là
A. 56,36%.
B. 51,72%.
C. 53,85%.
D. 76,70%.
![]()
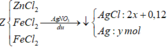

Khi tác dụng với HCl chỉ có các oxit bị hòa tan
→ nHCl = 4nO2 → nO2 = 0,03 mol
Gọi số mol của Cl2 và Ag lần lượt là x, y mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCL2 + nHCl = 2. x + 0,12
→ 143,5( 2. x + 0,12) + 108y = 28,345
Bảo toàn electron cho toàn bộ quá trình 3nFe + 2nZn = 2nCl2 + 4nO2 + nAg
→ 3. 0,04 + 2.0,04 = 2.x + 4. 0,03 + y
Giải hệ → x= 0,035 và y = 0,01
%Cl2 = 0 , 035 0 , 035 + 0 , 03 . 100% = 53,85%.
Đốt cháy hỗn hợp gồm 2,6 gam Zn và 2,24 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 1M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 28,345 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là
A. 56,36%.
B. 51,72%.
C. 53,85%.
D. 76,70%.

Khi tác dụng với HCl chỉ có các oxit bị hòa tan
→ nHCl = 4nO2 → nO2 = 0,03 mol
Gọi số mol của Cl2 và Ag lần lượt là x, y mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCL2 + nHCl = 2. x + 0,12
→ 143,5( 2. x + 0,12) + 108y = 28,345
Bảo toàn electron cho toàn bộ quá trình 3nFe + 2nZn = 2nCl2 + 4nO2 + nAg
→ 3. 0,04 + 2.0,04 = 2.x + 4. 0,03 + y
Giải hệ → x= 0,035 và y = 0,01
%Cl2 = 0 , 035 0 , 035 + 0 , 03 100% = 53,85%.
Đáp án C