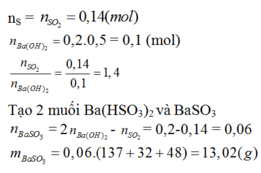Đốt cháy hoàn toàn 4,48 g lưu huỳnh rồi cho sản phẩm cháy hấp thụ hoàn toàn vào 200 ml
dung dịch Ba(OH)2 0,5M. Lượng chất kết tủa thu được sau phản ứng là:
A. 10,85 g
B. 16,725 g
C. 21,7 g
D. 13,02 g

Những câu hỏi liên quan
Đốt cháy hoàn toàn 4,48g lưu huỳnh rồi cho sản phẩm cháy hấp thụ hoàn toàn vào 200ml dung dịch Ba(OH)2 0,5M. Lượng chất kết tủa thu được sau phản ứng là:
A. 10,85g
B. 21,7g
C. 13,02g
D. 16,725g
Đốt cháy hoàn toàn m gam lưu huỳnh trong oxi dư, rồi hấp thụ hết lượng khí sản phẩm vào 200 ml dung dịch Ca(OH)2 0,3M thu được 6 gam kết tủa. Tính m
Đốt cháy hoàn toàn m gam FeS2 rồi cho toàn bộ sản phẩm khí tạo thành hấp thụ hết vào 200 ml dung dịch Ba(OH)2 0,75M thấy tạo ra 21,7 gam kết tủa. Tính m
\(n_{BaSO_3}=\dfrac{21.7}{217}=0.1\left(mol\right)\)
\(BTBa:\)
\(n_{Ba\left(HSO_3\right)_2}=0.2\cdot0.75-0.1=0.05\left(mol\right)\)
\(BTS:\)
\(n_{FeS_2}=\dfrac{0.1+0.05\cdot2}{2}=0.1\left(mol\right)\)
\(m_{FeS_2}=0.1\cdot120=12\left(g\right)\)
Đúng 2
Bình luận (0)
$n_{Ba(OH)_2} = 0,2.0,75 = 0,15(mol)$
$n_{BaSO_3} = 0,1(mol)$
TH1: $Ba(OH)_2$ dư
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Bảo toàn nguyên tố với S :
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,05(mol)$
$m = 0,05.120 = 6(gam)$
TH2 : Có tạo muối axit
Ba(OH)2 + SO2 → BaSO3 + H2O
0,1..............0,1.........0,1........................(mol)
Ba(OH)2 + 2SO2 → Ba(HSO3)2
0,05.............0,1........................................(mol)
$n_{SO_2} = 0,2(mol)$
$n_{FeS_2} = \dfrac{1}{2}n_{SO_2} = 0,1(mol)$
$m = 0,1.120 = 12(gam)$
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 6,6 gam hỗn hợp X gồm HCOOC3H7, C2H5COOCH3 rồi hấp thụ hoàn toàn sản phẩm cháy vào
m
1
gam dung dịch Ba(OH)2 dư. Sau phản ứng thu được m gam kết tủa. Lọc, tách kết tủa thu được
m
2
gam dung dịch nước lọc. Giá trị (m1 − m2) là A. 45,90 B. 53,70 C. 54,45 D. 40,50
Đọc tiếp
Đốt cháy hoàn toàn 6,6 gam hỗn hợp X gồm HCOOC3H7, C2H5COOCH3 rồi hấp thụ hoàn toàn sản phẩm cháy vào m 1 gam dung dịch Ba(OH)2 dư. Sau phản ứng thu được m gam kết tủa. Lọc, tách kết tủa thu được m 2 gam dung dịch nước lọc. Giá trị (m1 − m2) là
A. 45,90
B. 53,70
C. 54,45
D. 40,50
Chọn đáp án D
Các chất trong X đều có CTPT là C4H8O2 và M = 88. nX = 0,075 mol.
Sơ đồ đốt: C4H8O2 → 4CO2 + 4H2O.
n C O 2 = n H 2 O = 4 n X = 0 , 3 m o l
m = 0,3.197 = 59,1 gam.
∆m = mdd sau = mdd trước = m2 - m1 = m C O 2 + m H 2 O – m
= 0,3.(44 + 18) – 59,1
= –40,5
Đúng 0
Bình luận (0)
Hỗn hợp khí A chứa một ankan và một monoxicloankan. Tỉ khối của A đối với hiđro là 25,8. Đốt cháy hoàn toàn 2,58 g A rồi hấp thụ hết sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 g kết tủa. Công thức phân tử của các chất trong hỗn hợp A là: A. C4H8 và C3H6 B. C4H10 và C3H8 C. C4H8 và C3H8 D. C4H10 và C3H6
Đọc tiếp
Hỗn hợp khí A chứa một ankan và một monoxicloankan. Tỉ khối của A đối với hiđro là 25,8. Đốt cháy hoàn toàn 2,58 g A rồi hấp thụ hết sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 g kết tủa. Công thức phân tử của các chất trong hỗn hợp A là:
A. C4H8 và C3H6
B. C4H10 và C3H8
C. C4H8 và C3H8
D. C4H10 và C3H6
Đáp án C
nCO2 = nBaCO3 = 35,46/197 = 0,18 mol; nA= 2,58/51,6 = 0,05 mol
mH = 2,58 – 0,18.12 = 0,42 gam
=> nH2O = 0,21 mol; nankan = 0,21 – 0,18 = 0,03 mol => nxicloankan = 0,02 mol;
CTPT của ankan và xicloankan lần lượt là: CnH2n+2 và CmH2m
ta có: 0,02n + 0,03m = 0,18 => 2n + 3m = 18 => n = 3 và m = 4.
Đúng 0
Bình luận (0)
Trộn đều 11.5 g hỗn hợp X gồm axit CH3COOH và 1 ancol B CnH2n+1OH(số mol hai chất bằng nhau)rồi chia thành 2 phầnPhần 1 cho tác dụng với 5,1 g kim loại Na(có dư) sau phản ứng thấy khối lượng chất rắn thu được nhiều hơn hỗn hợp axit và ancol(phần 1) là 5,0gPhần 2 đem đốt cháy hoàn toàn trong oxi dư rồi hấp thụ toàn bộ sản phẩm cháy vào Ca(OH)2 thu được 12,5 g kết tủa và dung dịch D.Nung kĩ dung dịch D lại thu thêm 5,0 g kết tủaViết các phương trình hóa học xảy raXác định công thức cấu tạo của an...
Đọc tiếp
Trộn đều 11.5 g hỗn hợp X gồm axit CH3COOH và 1 ancol B CnH2n+1OH(số mol hai chất bằng nhau)rồi chia thành 2 phần
Phần 1 cho tác dụng với 5,1 g kim loại Na(có dư) sau phản ứng thấy khối lượng chất rắn thu được nhiều hơn hỗn hợp axit và ancol(phần 1) là 5,0g
Phần 2 đem đốt cháy hoàn toàn trong oxi dư rồi hấp thụ toàn bộ sản phẩm cháy vào Ca(OH)2 thu được 12,5 g kết tủa và dung dịch D.Nung kĩ dung dịch D lại thu thêm 5,0 g kết tủa
Viết các phương trình hóa học xảy ra
Xác định công thức cấu tạo của ancol B.biết các phản ứng xảy ra hoàn toàn
Gọi a, a là mol CH3-COOH , R-OH trong mỗi phần 5,75 g
Phần 1: có a mỗi chất CH3-COOH , R-OH ==> rắn gồm muối CH3-COONa , R1-ONa và Na dư
CH3-COOH + Na --> CH3-COONa + 0,5 H2
a------------------a-------------a-----------0,5a
R-OH + Na ----> R-ONa + 0,5 H2
a----------a----------a--------0,5a
2a mol X cho 2a mol muối có khối lượng tăng 22*2a
m rắn tăng = m muối tăng + mNa dư = 22*2a + (5,1 - 23*2a) = 5 mX ==> a = 0,05
Khối lượng phần 1: m1 = 60*0,05 + 0,05(14n+18) = 3,9 + 0,7n. (1)
Phần 2: có ak mol mỗi chất C2H4O2 và CnH2n+2O
CO2 + Ca(OH)2 --> CaCO3 + H2O
0,125-------------------0,125
2 CO2 + Ca(OH)2 --> Ca(HCO3)2
0,1---------------------------0,05
Ca(HCO3)2 ---> CaCO3 + CO2 + H2O
0,05------------------0,05
mol CO2= 2*ka + nka = ka(2+n) = 0,225
=> k(2+n) = 4,5 (2)
Khối lượng phần 2: m2 = 11,5 - m1 = 3,9 - 0,7n = 7,6 - 0,7n
Nếu
n = 1: (2) => k = 1,5 , từ (1) và (3) => m1 = 4,6 => m2 = 6,9 => m2/m1 = 1,5 = k: thỏa
n = 2: (2) => k = 1,125 , từ (1) và (3) => m1 = 5,3 => m2 = 6,2 => m2/m1 = 1,16 khác k = 1,125 ==> loại
Vậy ancol B là CH3-OH
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn (m) gam một cacbohiđrat (X) cần 13,44 lít O2 (đktc) sau đó đem hấp thụ hoàn toàn sản phẩm cháy trong 200 ml dung dịch chứa đồng thời NaOH 1,75M và Ba(OH)2 1M thu được kết tủa có khối lượng là A. 9,85 gam B. 39,4 gam C. 19,7 gam D. 29,55 gam
Đọc tiếp
Đốt cháy hoàn toàn (m) gam một cacbohiđrat (X) cần 13,44 lít O2 (đktc) sau đó đem hấp thụ hoàn toàn sản phẩm cháy trong 200 ml dung dịch chứa đồng thời NaOH 1,75M và Ba(OH)2 1M thu được kết tủa có khối lượng là
A. 9,85 gam
B. 39,4 gam
C. 19,7 gam
D. 29,55 gam
CTTQ của X là Cn(H2O)m. Khi đốt cháy: Cn(H2O)m + nO2 → nCO2 + mH2O
=> nCO2 = nO2 = 0,6 mol
nOH- = 2nBa(OH)2 + nNaOH = 0,75 mol
Do nCO2 < nOH- <2nCO2 => CO2 hòa tan 1 phần kết tủa
=> n kết tủa = nOH- - nCO2 = 0,15 mol m BaCO3 = 29,55g
=>D
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm rượu có dạng CnH2n+1OH(A) và hidrocacbon có dạng CmH2m (B), hấp thụ hết sản phẩm cháy vào 200ml dung dịch Ba(OH)2 1M thu được 19,7 g kết tủa và khối lượng dung dịch sau phản ứng tăng 0,7 g. Đun nóng dung dịch thấy xuất hiện thêm kết tủa. Xác định công thức phân tử của A và B, biết A có thể được tạo thành trực tiếp từ B.
nBa(OH)2=0,2 mol
nBaCO3=19,7/197=0,1 mol=nCO2
Ba(OH)2+CO2=>BaCO3+H2O
0,1 mol<=0,1 mol<=0,1 mol
Ba(OH)2+2CO2=>Ba(HCO3)2
0,1 mol=>0,2 mol
mdd tăng=mCO2+mH2O-mktủa
=>0,7=0,3.44+mH2O-19,7=>mH2O=7,2g
=>nH2O=0,4 mol
n ancol=nH2O-nCO2=0,4-0,3=0,1 mol
A có thể tạo thành trực tiếp từ B=>A có số Cacbon trong ptử bằng B=>m=n và n>=2
=>ta có nCO2= 0,1n+xn=0,3=>n=<3
chọn n=2=>x=0,05 mol(tm)
Sáng mình có giải mấy bài bạn hỏi từ hôm qua, bạn xem lại nhé, chúc bạn thi tốt!
Đúng 0
Bình luận (0)
Crackinh m gam hỗn hợp X gồm ba ankan sau một thời gian thu được hỗn hợp Y chỉ chứa các hiđrocacbon. Chia Y thành hai phần. Phần 1 dẫn qua dung dịch Br2 0,2M thấy mất màu tối đa 350 ml, khí thoát ra chiếm 44% thể tích phần 1. Phần 2 đốt cháy hoàn toàn, hấp thụ toàn bộ sản phẩm cháy vào 500 ml dung dịch Z gồm Ba(OH)2 0,5M và KOH 1,29M thì thu được 39,4 gam kết tủa, khối lượng dung dịch tăng 22,16 gam. Đốt cháy hoàn toàn m gam X rồi hấp thụ sản phẩm cháy vào 600 ml dung dịch Z thì thấy khối lượng...
Đọc tiếp
Crackinh m gam hỗn hợp X gồm ba ankan sau một thời gian thu được hỗn hợp Y chỉ chứa các hiđrocacbon. Chia Y thành hai phần. Phần 1 dẫn qua dung dịch Br2 0,2M thấy mất màu tối đa 350 ml, khí thoát ra chiếm 44% thể tích phần 1. Phần 2 đốt cháy hoàn toàn, hấp thụ toàn bộ sản phẩm cháy vào 500 ml dung dịch Z gồm Ba(OH)2 0,5M và KOH 1,29M thì thu được 39,4 gam kết tủa, khối lượng dung dịch tăng 22,16 gam. Đốt cháy hoàn toàn m gam X rồi hấp thụ sản phẩm cháy vào 600 ml dung dịch Z thì thấy khối lượng dung dịch tăng m1 gam. Giá trị (m + m1) gần nhất với
A. 75
B. 68.
C. 80.
D. 70