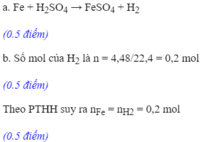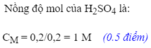Cho 8,4 gam Sắt tác dụng hết với 0,05 lít dung dịch axit sunfuric. a. Viết phương trình hóa học b. Tính nồng độ mol của dung dịch H2SO4 đã dùng

Những câu hỏi liên quan
Cho 8,4gam sắt (iron) tác dụng hết 50ml dung dịch axit sunfuric (sulfuric acid) a) viết phương trình hóa học b) tính nồng độ mol của dung dịch axit sunfuric (sulfuric acid) đã dùng
a) $Fe + H_2SO_4 \to FeSO_4 + H_2$
b) Theo PTHH : $n_{H_2SO_4} = n_{Fe} = \dfrac{8,4}{56} = 0,15(mol)$
$C_{M_{H_2SO_4}} = \dfrac{0,15}{0,05} = 3M$
Đúng 1
Bình luận (0)
Cho 8,4gam sắt (iron) tác dụng hết 50ml dung dịch axit sunfuric (sulfuric acid) a) viết phương trình hóa học b) tính nồng độ mol của dung dịch axit sunfuric (sulfuric acid) đã dùng Tóm tắt bài làm
Cho 11,2 gam sắt tác dụng với 50ml dung dịch axít sunfuric thu được muối sắt (II) sunfat và khí hidro a) viết phương trình hóa học đã xảy ra b) tính khối lượng muối thu được sau phản ứng c) tính nồng độ mol của dung dịch h2so4 đã dùng
Sửa đề : 11.2 g sắt
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.2....0.2.................0.2\)
\(m_{FeSO_4}=0.2\cdot152=30.4\left(g\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{0.2}{0.05}=4\left(M\right)\)
Đúng 2
Bình luận (1)
\(m_{Fe}=\dfrac{11}{56}=0.19\left(mol\right)\)
\(Fe+H_2SO_4->FeSO_4+H_2\)
0.19 0.19 0.19 (mol)
\(m_{FeSO_4}=0.19\cdot152=28.28\left(g\right)\)
\(Cm=\dfrac{0.19}{0.05}=3.8M\)
Đúng 0
Bình luận (1)
PTHH:Fe+H2SO4→FeSO4+H2Fe+H2SO4→FeSO4+H2
TPT: 1 1 1 1 1 1 1 MOL
TĐ: 0,2 0,2 0,20 2 0,2 0,2 0,2 MOL
nFe=11.256=0.2(mol)
mFeSO4=0,2⋅152=30,4(g)
Đúng 0
Bình luận (0)
cho 11,2 gam sắt tác dụng với dung dịch loãng có chứa 24,5 gam axit sunfuric H2SO4 a, viết phương trình hóa học xảy ra
b, tính thể tích khid hidro thu đc ( ở đktc)
c, dung dịch sau phản ứng có những chất nào . tính nồng độ % của các dung dịch sau phản ứng , biết dung dịch sau phản ứng có khối lượng là 190 gam
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\
n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\
pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(LTL:\dfrac{0,2}{1}< \dfrac{0,25}{1}\)
=> H2SO4 dư
\(n_{H_2}=n_{H_2SO_4\left(p\text{ư}\right)}=n_{Fe}=0,2\left(mol\right)\\
V_{H_2}=0,2.22,4=4,48l\\
m_{H_2SO_4\left(d\right)}=\left(0,25-0,2\right).98=4,9g\)
Đúng 1
Bình luận (0)
Cho 5,6g Fe tác dụng với 200ml dung dịch H2SO4 thu được dung dịch FeSO4 và khí H2.
a. Viết phương trình hóa học?
b. Tính thể tích khí H2 (đktc)?
c. Tính nồng độ mol/lít của dung dịch H2SO4 cần dùng?
d. Tính nồng độ mol/lít của dung dịch muối thu được sau phản ứng?
a,\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1 0,1 0,1
b,\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c,\(C_{M_{ddH_2SO_4}}=\dfrac{0,1}{0,2}=0,5M\)
d,\(C_{M_{ddFeSO_4}}=\dfrac{0,1}{0,2}=0,5M\)
Đúng 1
Bình luận (2)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ a.Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ b.0,1.......0,1..........0,1...........0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ c.C_{MddH_2SO_4}=\dfrac{0,1}{0,2}=0,5\left(M\right)\\ d.C_{MddFeSO_4}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Đúng 1
Bình luận (0)
Cho một lượng kim loại sắt tác dụng với 100ml dung dịch h2so4 loãng sinh ra 5,6l khí h2 ở dktc a) hãy viết phương trình hóa học xảy ra b) tính khối lượng sắt đã tham gia phản ứng c) tính nồng độ mol của dung dịch h2so4 đã dùng CẦN GẤP LẮM RỒI MỌI NGƯỜI GIÚP ĐỠ CHO EM VỚI
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.25....0.25.......................0.25\)
\(m_{Fe}=0.25\cdot56=14\left(g\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{0.25}{0.1}=2.5\left(M\right)\)
Đúng 2
Bình luận (1)
a. PTHH: Fe+H2SO4-->FeSO4+H2
b. Có nH2=\(\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
Theo pthh trên, nFe=nH2=0.25mol
=> mFe=0.25*56=14g
c. Theo pthh trên, nH2=nH2SO4=0.25mol
Đổi 100ml=0.1l
=> \(C_M=\dfrac{0.25}{0.1}=2.5M\)
Đúng 2
Bình luận (1)
Cho một lượng bột sắt dư vào 200ml dung dịch axit H 2 S O 4 . Phản ứng xong thu được 4,48 lít khí hiđrô (đktc)
a. Viết phương trình phản ứng hoá học
b. Tính khối lượng sắt đã tham gia phản ứng
c. Tính nồng độ mol của dung dịch axit H 2 S O 4 đã dùng
Cho 1,6 gam đồng (II) oxit tác dụng với 100 gam dung dịch axit sunfuric có nồng độ 200/0
a) Viết phương trình hóa học
b) Tính nồng độ phần trăm của các chất có trong dung dịch sau khi phản ứng kết thúc
\(n_{CuO}=\dfrac{1.6}{80}=0.02\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{100\cdot20\%}{98}=\dfrac{10}{49}\left(mol\right)\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(1...........1\)
\(0.02..........\dfrac{10}{49}\)
\(LTL:\dfrac{0.02}{1}< \dfrac{10}{49}\Rightarrow H_2SO_4dư\)
\(m_{\text{dung dịch sau phản ứng}}=1.6+100=101.6\left(g\right)\)
\(C\%_{CuSO_4}=\dfrac{0.02\cdot160}{101.6}\cdot100\%=3.15\%\)
\(C\%_{H_2SO_4\left(dư\right)}=\dfrac{\left(\dfrac{10}{49}-0.02\right)\cdot98}{101.6}\cdot100\%=17.75\%\)
Đúng 4
Bình luận (2)
Cho 15,8 gam kali sufit tác dụng vừa đủ với 200 ml axit H2SO4
a)Viết phương trình phải ứng
b)Tính nồng độ SO2 thoát ra ở (đktc)
tính nồng độ mol dung dịch axit đã dùng
nK2SO3=15.8\158=0.1(mol)
K2SO3+H2SO4→K2SO4+SO2+H2O
0.1...........................0.1..........0.1
VSO2=0.1⋅22.4=2.24(l)
CMK2SO4=0.1\0.2=0.5(M)
Đúng 1
Bình luận (4)