Bài 1:
a) tính số gam Cu và thể tích oxi để điều chế 12,8 gam đồng (2) oxit
b) tính số gam kali clorat cần dùng để có được lượng oxi cần dùng cho phản ứng trên
đốt cháy 7,44 gam Photpho trong khí oxi ,thu được điphotpho pentaoxit a) Tính thể tích khí oxi đã phản ứng (ở đktc)? b) cần dùng bao nhiêu gam Kali clorat để điều chế được khí Oxi dùng cho phản ứng trên?
4P + 5O2 ----> 2P2O5
0,24 -> 0,3 ---> 0,12 (mol)
nP = \(\dfrac{7,44}{31}\)= 0,24 (mol)
VH2 = 0,3 . 22,4 = 6,72 (l)
2KClO3 ---> 2KCl + 3O2
0,2 <------------- 0,3 (mol)
mKClO3 = 0,2 . (39 + 35,5 + 16.3)
= 24,5 (g)
Vui lòng kiểm tra lại kết quả dùm, thank you.
nP = 7,44 : 31 = 0,24 ( mol)
pthh : 4P + 5O2 -t--> 2P2O5
0,24->0,3 (mol)
=> VO2 =0,3 . 22,4 = 6,72 (l)
pthh : 2KClO3 -t--> 2KCl + 3O2
0,2<-------------------0,3 (mol)
=> mKClO3 = 0,2 .122,5 = 24,5 (g)
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 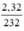 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
Trong phòng thí nghiệm người ta dùng oxi oxi hoá sắt ở nhiệt độ cao để điều chế được 11,6 gam oxit sắt từ (Fe3O4 ).
a. Tính số gam sắt và thể tích oxi cần dùng ở (đktc) để điều chế được Fe3O4 trên?
b. Tính số gam Kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên.
a, Ta có: \(n_{Fe_3O_4}=\dfrac{11,6}{232}=0,05\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
___0,15__0,1____0,05 (mol)
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
b, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
________0,2________________________0,1 (mol)
\(\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
Bạn tham khảo nhé!
4. Khi đốt cháy sắt trong oxi ở nhiệt độ cao thu được oxit sắt từ Fe3O4. a) Tính khối lượng sắt và thể tích khí oxi (đktc) cần dùng để điều chế được 6,96 gam Fe3O4 . b) Tính khối lượng kali clorat KClO3 cần dùng để điều chế được lượng oxi dùng cho phản ứng trên.
a. \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -to-> Fe3O4
0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
b. PTHH : 2KCl + 3O2 -> 2KClO3
0,06 0,04
\(m_{KClO_3}=0,04.122,5=4,9\left(g\right)\)
4
n Fe3O4=\(\dfrac{6,96}{232}=0,03mol\)
3Fe+2O2-to>Fe3O4
0,09---0,06-----0,03 mol
=>m Fe=0,09.56=5,04g
=>VO2=0,06.22,4=1,344l
b)
2KClO3-to>2KCl+3O2
0,04----------------------0,06 mol
=>m KClO3=0,04.122,5=4,9g
\(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ n_{Fe}=3.0,03=0,09\left(mol\right);n_{O_2}=0,03.2=0,06\left(mol\right)\\ a,\Rightarrow m_{Fe}=0,09.56=5,04\left(g\right);V_{O_2\left(đktc\right)}=0,06.22,4=1,344\left(l\right)\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,06}{3}=0,04\left(mol\right)\\ \Rightarrow b,m_{KClO_3}=122,5.0,04=4,9\left(g\right)\)
\(4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ n_{O_2} = \dfrac{5}{4}n_P = \dfrac{5}{4}.\dfrac{3,72}{31} = 0,15(mol)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,1(mol)\\ \Rightarrow m_{KClO_3} = 0,1.122,5 = 12,25(gam)\)
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)
trong phòng thí nghiệm , người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhieeyj độ cao
a) tính số gam sắt và số gam khí oxi cần dùng để điều chế 4,46 g oxit sắt từ
b) tính số gam KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên
Sửa đề: 4,46 (g) → 4,64 (g)
a, \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
Theo PT: \(n_{Fe}=3n_{Fe_3O_4}=0,06\left(mol\right)\Rightarrow m_{Fe}=0,06.56=3,36\left(g\right)\)
\(n_{O_2}=2n_{Fe_3O_4}=0,04\left(mol\right)\Rightarrow m_{O_2}=0,04.32=1,28\left(g\right)\)
b, \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=2n_{O_2}=0,08\left(mol\right)\Rightarrow m_{KMnO_4}=0,08.158=12,64\left(g\right)\)
Câu 7. Đốt cháy hết 2,76 gam kim loại Natri trong bình đựng khí oxi (phản ứng vừa đủ).
a) Tính khối lượng natri oxit thu được.
b) Tính khối lượng Kali clorat cần để điều chế lượng oxi dùng cho phản ứng trên.
c) Đốt cháy hoàn toàn 8,22 gam một kim loại X hóa trị II thì cần vừa đủ lượng oxi trên. Xác định tên và KHHH của kim loại.
Cho Mik Xin Luôn Câu Trả Lời , Mai Cô Gíao Kiểm Tra , Thanks !
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi.
a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này.
b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.
c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
2KClO3-to\xt->2KCl+3O2
0,1------------------0,1
n KClO3=\(\dfrac{12,25}{122,5}\)=0,1 mol
=>m KCl=0,1.74,5=7,45g
H=\(\dfrac{6,8}{7,45}.100\)=91,275%
b)
2KClO3-to\xt->2KCl+3O2
0,2-------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
H=85%
=>m KClO3=0,2.122,5.\(\dfrac{100}{85}\)=28,82g
c)
2KClO3-to\xt->2KCl+3O2
0,2------------------------0,3
n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
H=80%
=>m O2=0,3.32.\(\dfrac{80}{100}\)=10,4g