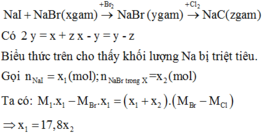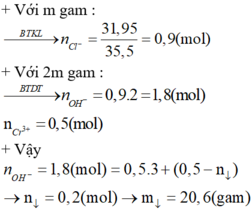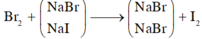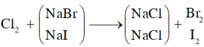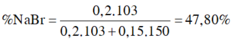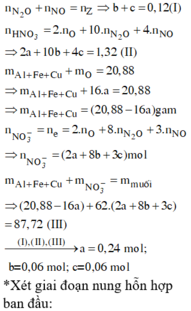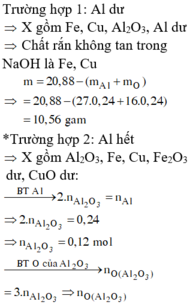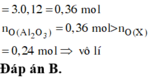Hòa tan hoàn toàn x gam hỗn hợp gồm NaI và NaBr vào nước thu được dung dịch X . Cho Br2 dư vào X được dung dịch Y. Cô cạn dung dịch thu được y gam chất rắn khan.Hòa tan y gam chất rắn khan đó vào nước thu được dung dịch Z. Cho Cl2 dư vào dung dịch Z thu được dung dịch T. Cô cạn T thu được z gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn và 2y = x + z. Phần trăm khối lượng của NaBr trong hỗn hợp đầu là

Những câu hỏi liên quan
Hòa tan hoàn toàn x (g) hỗn hợp: NaI và NaBr vào nước thu được dung dịch X. Cho Br2 dư vào X được dung dịch Y. Cô cạn Y thu được y (g) chất rắn khan. Tiếp tục hòa tan y (g) chất rắn khan trên vào nước thu được dung dịch Z. Cho Cl2 dư vào Z thu được dung dịch T. Cô cạn T được z (g) chất rắn khan. Biết các phản ứng xảy ra hoàn toàn và 2y x + z. Phần trăm khối lượng NaBr trong hỗn hợp đầu bằng: A. 7,3% B. 4,5% C. 3,7% D. 6,7%
Đọc tiếp
Hòa tan hoàn toàn x (g) hỗn hợp: NaI và NaBr vào nước thu được dung dịch X. Cho Br2 dư vào X được dung dịch Y. Cô cạn Y thu được y (g) chất rắn khan. Tiếp tục hòa tan y (g) chất rắn khan trên vào nước thu được dung dịch Z. Cho Cl2 dư vào Z thu được dung dịch T. Cô cạn T được z (g) chất rắn khan. Biết các phản ứng xảy ra hoàn toàn và 2y = x + z. Phần trăm khối lượng NaBr trong hỗn hợp đầu bằng:
A. 7,3%
B. 4,5%
C. 3,7%
D. 6,7%
1. Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m + 28,4) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ hết dung dịch Z vào 0,4 lit dung dịch AlCl3 1,25M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là2. Hòa tan hoàn toàn 10g hỗn hợp Al, Mg trong dung dịch HCl dư, thu được dung dịch X. Cho X tác dụng với dung dịch NaOH dư. Lọc lấy kết tủa, đem nung trong khôn...
Đọc tiếp
1. Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m + 28,4) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ hết dung dịch Z vào 0,4 lit dung dịch AlCl3 1,25M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là
2. Hòa tan hoàn toàn 10g hỗn hợp Al, Mg trong dung dịch HCl dư, thu được dung dịch X. Cho X tác dụng với dung dịch NaOH dư. Lọc lấy kết tủa, đem nung trong không khí đến khối lượng không đổi được 6g chất rắn. Phần trăm khối lượng của Mg trong hỗn hợp ban đầu là
3. Để hòa tan hoàn toàn 6,4g hỗn hợp gồm kim loại R (chỉ có hóa trị II) và oxit của nó cần vừa đủ 400ml dung dịch HCl 1M. R có thể là kim loại nào sau đây
B3:
Bài 3 người ta cho các kim loại sau đây là những kim loại nào thế?
Đúng 0
Bình luận (0)
B2:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\\ MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\\ Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+H_2O\\ Mg\left(OH\right)_2\rightarrow\left(t^o\right)MgO+H_2O\\ Đặt:n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+24b=10\\40b=6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=\dfrac{32}{135}\\b=0,15\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,15.24}{10}.100\%=36\%\)
Đúng 1
Bình luận (0)
1. Gọi chung cho hai kim loại Na và K là R
* m(g) hh X + HCl :
BTNT Cl : \(\rightarrow\)\(n_{HCl_{pứ}}=n_{Cl_{muoi}}=\dfrac{\left(m+28,4\right)-m}{35,5}=0,8\left(mol\right)\)
\(2R+2HCl\rightarrow2RCl+H_2\) (1)
(1) \(\rightarrow n_R=n_{HCl}=0,8\left(mol\right)\)
* 2m(g) hh X + H2O -> ddZ
\(2R+2H2O\rightarrow2ROH+H2\) (2)
(2) \(\rightarrow n_{ROH}=n_R=1,6\left(mol\right)\)
\(n_{AlCl_3}=0,4.1,25=0,5\left(mol\right)\)
\(3ROH+AlCl_3\rightarrow Al\left(OH\right)_3+3RCl\)
Trước pứ : 1,6 0,5 (mol)
Pứ : 1,5 <- 0,5 -> 0,5 1,5 (mol)
Sau pứ : 0.1 0 0,5 1,5 (mol)
Do ROH dư : \(ROH+Al\left(OH\right)_3\rightarrow RAlO_2+2H_2O\)
Trước pứ : 0,1 0,5 (mol)
Pứ : 0,1 -> 0,1 0,1 (mol)
Sau pứ : 0 0,4 (mol)
\(\rightarrow m_{kettua}=0,4.78=31,2\left(g\right)\)
\(\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là A. 54,0 gam. B. 20,6 gam. C. 30,9 gam. D. 51,5 gam.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là
A. 54,0 gam.
B. 20,6 gam.
C. 30,9 gam.
D. 51,5 gam.
Đáp án B
DVới m (g) X: nX= nCl= 31,95:35,5= 0,9 mol
Với 2m (g) X:

Đúng 0
Bình luận (0)
Hoà tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m + 31,95) gam hỗn hợp chất rắn khan. Hoà tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch
CrCl
3
1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là A. 54,0 gam B. 20,6 gam C. 30,9 gam D. 51,5 gam
Đọc tiếp
Hoà tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y thu được (m + 31,95) gam hỗn hợp chất rắn khan. Hoà tan hoàn toàn 2m gam hỗn hợp X vào nước thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0,5 lít dung dịch CrCl 3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là
A. 54,0 gam
B. 20,6 gam
C. 30,9 gam
D. 51,5 gam
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y, cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0.5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là: A.54,0 gam B.20,6 gam C. 30,9 gam D.51,5 gam
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Na và K vào dung dịch HCl dư thu được dung dịch Y, cô cạn dung dịch Y thu được (m+31,95) gam hỗn hợp chất rắn khan. Hòa tan hoàn toàn 2m gam hỗn hợp X thu được dung dịch Z. Cho từ từ đến hết dung dịch Z vào 0.5 lít dung dịch CrCl3 1M đến phản ứng hoàn toàn thu được kết tủa có khối lượng là:
A.54,0 gam
B.20,6 gam
C. 30,9 gam
D.51,5 gam
Cho hỗn hợp X gồm NaBr và NaI tan trong nước thu được dung dịch Y. Nếu cho Brom dư vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn, cô cạn thì thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí Clo dư vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thì thấy khối lượng muối khan giảm 22,625 gam. Thành phần phần trăm khối lượng của một chất trong hỗn hợp X là A. 35,9% B. 47,8% C. 33,99% D. 64,3%
Đọc tiếp
Cho hỗn hợp X gồm NaBr và NaI tan trong nước thu được dung dịch Y. Nếu cho Brom dư vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn, cô cạn thì thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí Clo dư vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thì thấy khối lượng muối khan giảm 22,625 gam. Thành phần phần trăm khối lượng của một chất trong hỗn hợp X là
A. 35,9%
B. 47,8%
C. 33,99%
D. 64,3%
Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
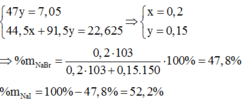
Đúng 0
Bình luận (0)
Giúp emHòa tan hỗn hợp gồm NaBr và NaI vào nước được dung dịch A. Cho brom dư vào dung dịch khuấy kĩ cho phản ứng xong, cô cạn dung dịch thu được chất rắn khan có khối lượng giảm m gam so với hỗ hợp bạn đầu. Hòa tan chất rắn vào nước, sau đó dẫn khí clo dư đi qua. Lại làm bay hơi nước thấy khối lượng chất rắn khan thu được lại giảm m gam nữa so với hỗn hợp ban đầu. Tính phần trăm khối lượng của NaBr trong hỗn hợp ban đầu
Đọc tiếp
Giúp em
Hòa tan hỗn hợp gồm NaBr và NaI vào nước được dung dịch A. Cho brom dư vào dung dịch khuấy kĩ cho phản ứng xong, cô cạn dung dịch thu được chất rắn khan có khối lượng giảm m gam so với hỗ hợp bạn đầu. Hòa tan chất rắn vào nước, sau đó dẫn khí clo dư đi qua. Lại làm bay hơi nước thấy khối lượng chất rắn khan thu được lại giảm m gam nữa so với hỗn hợp ban đầu. Tính phần trăm khối lượng của NaBr trong hỗn hợp ban đầu
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
Đúng 0
Bình luận (1)
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
Đúng 0
Bình luận (1)
Hỗn hợp X gồm NaBr và NaI. Cho hỗn hợp X tan trong nước thu được dung dịch A. Nếu cho brom dư vào dung dịch A, sau phản ứng hoàn toàn, cô cạn thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí clo dư vào dung dịch A, phản ứng hoàn toàn, cô cạn dung dịch thấy khối lượng muối khan giảm 22,625 gam. Thành phần % khối lượng của một chất trong hỗn hợp X là: A. 64,3%. B. 39,1%. C. 47,8%. D. 35,9%
Đọc tiếp
Hỗn hợp X gồm NaBr và NaI. Cho hỗn hợp X tan trong nước thu được dung dịch A. Nếu cho brom dư vào dung dịch A, sau phản ứng hoàn toàn, cô cạn thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí clo dư vào dung dịch A, phản ứng hoàn toàn, cô cạn dung dịch thấy khối lượng muối khan giảm 22,625 gam. Thành phần % khối lượng của một chất trong hỗn hợp X là:
A. 64,3%.
B. 39,1%.
C. 47,8%.
D. 35,9%
Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm NaBr và NaI. Cho hỗn hợp X tan trong nước thu được dung dịch A. Nếu cho brom dư vào dung dịch A, sau phản ứng hoàn toàn, cô cạn thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí clo dư vào dung dịch A, phản ứng hoàn toàn, cô cạn dung dịch thấy khối lượng muối khan giảm 22,625 gam. Thành phần % khối lượng của một chất trong hỗn hợp X là: A. 64,3% B. 39,1%. C. 47,8% D. 35,9%
Đọc tiếp
Hỗn hợp X gồm NaBr và NaI. Cho hỗn hợp X tan trong nước thu được dung dịch A. Nếu cho brom dư vào dung dịch A, sau phản ứng hoàn toàn, cô cạn thấy khối lượng muối khan thu được giảm 7,05 gam. Nếu sục khí clo dư vào dung dịch A, phản ứng hoàn toàn, cô cạn dung dịch thấy khối lượng muối khan giảm 22,625 gam. Thành phần % khối lượng của một chất trong hỗn hợp X là:
A. 64,3%
B. 39,1%.
C. 47,8%
D. 35,9%
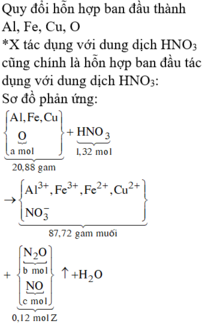
Nung nóng 20,88 gam hỗn hợp gồm Al, Fe2O3 và CuO trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Cho X vào dung dịch NaOH dư, thấy lượng NaOH phản ứng là 9,6 gam, thu được m gam chất rắn không tan. Nếu hòa tan hoàn toàn X trong dung dịch chứa 1,32 mol HNO3 thu được dung dịch Y chỉ chứa các muối nitrat của kim loiaj và 0,12 mol hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y thu được 87,72 gam muối khan. Giá trị của m là: A.10,80. B.10,56. C.8,64. D.14,40.
Đọc tiếp
Nung nóng 20,88 gam hỗn hợp gồm Al, Fe2O3 và CuO trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Cho X vào dung dịch NaOH dư, thấy lượng NaOH phản ứng là 9,6 gam, thu được m gam chất rắn không tan. Nếu hòa tan hoàn toàn X trong dung dịch chứa 1,32 mol HNO3 thu được dung dịch Y chỉ chứa các muối nitrat của kim loiaj và 0,12 mol hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y thu được 87,72 gam muối khan. Giá trị của m là:
A.10,80.
B.10,56.
C.8,64.
D.14,40.